Nat Metabo:程文文等绘制控制饮食的后脑神经元图谱,助力开发更好的减肥药物
时间:2022-10-13 15:55:17 热度:37.1℃ 作者:网络
肥胖是由于长期热量摄入超过能量消耗促进了体内能量储存过多(主要是甘油三酯),进而导致肥胖。如今,肥胖已成为全球范围内的大流行病,它增加了糖尿病、高血压、心血管疾病和癌症等重大慢性疾病的风险;同时还影响了生活质量和预期寿命。
通常,美味的食物总让人欲罢不能,那种尝过后的记忆无论过去多少年,当再次品尝时依然能瞬间识别出来,在感慨“是熟悉的味道”的同时,也会不自觉地暴饮暴食。长此以往,美食导致体重增加;而那些特别难吃的食物也会给人留下深刻印象,以至于再次看到时会令人生厌,甚至引起胃肠道不适,进而降低了食欲。
上述规律让我们不难发现:美味的食物容易使人发胖;而难吃的食物会抑制食欲,有助于减轻体重。
普遍观点也是认为,体重增加主要归因于对美食的自控力较差。然而,各种遗传和实验数据表明,体重/体脂是由生物学决定的。生理系统以类似控制血压的方式动态调节能量储存。
此前,科学家们对调节血压的生理过程已经有了充分的了解,并因此开发出许多有效的降压药物。同样,充分了解控制食物摄入和体重的生理系统,将有助于科学家识别和开发出更有效治疗肥胖的药物。
2022年7月25日,美国密歇根大学安娜堡分校的 Martin G. Myers Jr. 实验室(程文文为第一作者)发表在 Nature 子刊 Nature Metabolism 上发表了题为:Hindbrain circuits in the control of eating behaviour and energy balance 的综述论文。
这篇综述回顾了对控制进食的后脑神经元理解的最新见解,并据此建立了相关后脑回路模型,以预测哪些神经元可以像吃到难吃的食物那样抑制食欲。这些信息为在生理条件或药物刺激下产生厌恶反应以长期控制食物摄入提供了重要的新见解。
此前,科学家们已经发现许多器官系统参与控制能量稳态,但大脑在其中发挥着最关键的作用。大脑中有大量神经回路,它们不断评估和整合代谢、胃肠、内分泌和神经元信号,并通知一个匹配能量摄入和消耗的系统,以维持长期的能量稳态。此外,全基因组关联研究(GWAS)揭示了影响身体质量指数(BMI)的基因在大脑中表达,并表明人群中 BMI 的显着差异主要是由大脑功能的改变引起的。
在中枢神经系统中,瘦素系统和黑素皮质系统已被发现在控制能量稳态方面发挥着重要作用。而且,由于瘦素调节回路位于下丘脑,因此,许多能量稳态相关的研究也着重关注了下丘脑。
然而,最近的研究发现,上述生物因素并不能直接控制进食行为。相反,调节食物摄入和能量稳态的下丘脑回路靶向的是后脑背侧迷走神经复合体的关键组成部分。
背侧迷走神经复合体(DVC,见下图)是一个位于脑干的区域,它将胃肠道的感觉信息与协调食物摄入的节律模式整合在一起,包括进食后的饱腹感(或恶心感)。DVC 中有几个对控制食物摄入至关重要的核,包括极后区(AP)、孤束核(NTS)和迷走神经背侧运动核(DMV),以及反映肠道状态信息进入大脑的主要入口点。
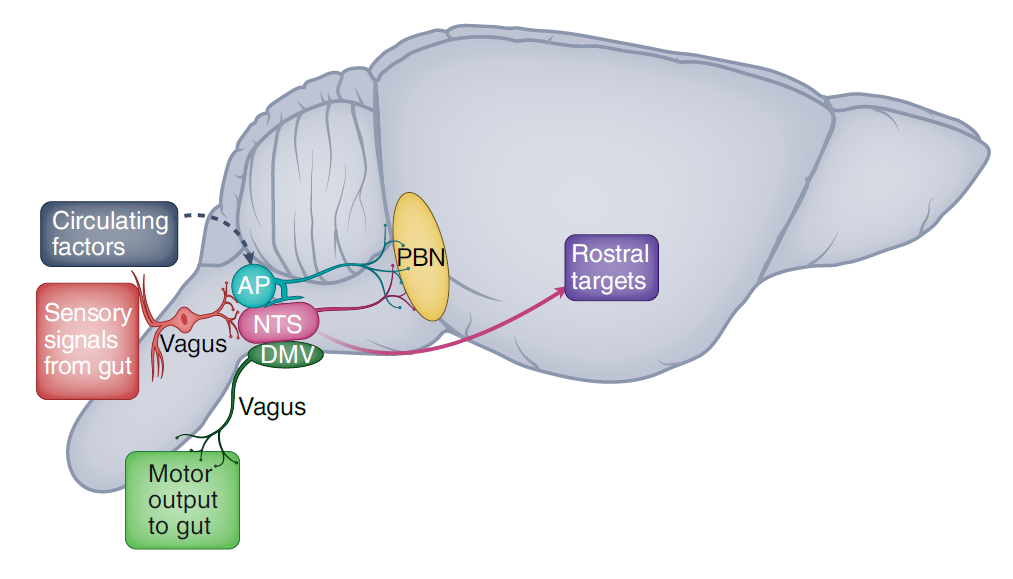
该论文的通讯作者 Martin G. Myers Jr. 表示,下丘脑所做的一切最终都会汇聚到脑干。脑干在控制进食方面非常重要,因为它从你的肠道中获取各种信息,包括胃扩张,是否摄入了营养素,并将这些信息与下丘脑关于营养需求的信息整合,然后将这些信息传递给控制食物摄入的自主节律模式。
极后区会接收一些迷走神经的输入信号,但该结构位于血脑屏障之外,因此具有独特感知血液传播信号的能力,包括来自肠道的各种与摄入相关的体液信号。
Myers 实验室此前的一篇小鼠研究建立了迷走神经背侧运动核的单细胞图谱,并揭示两种不同类型的孤束核(AP)神经元调节食物摄入:一种会导致恶心和厌恶感;而另一种不会。
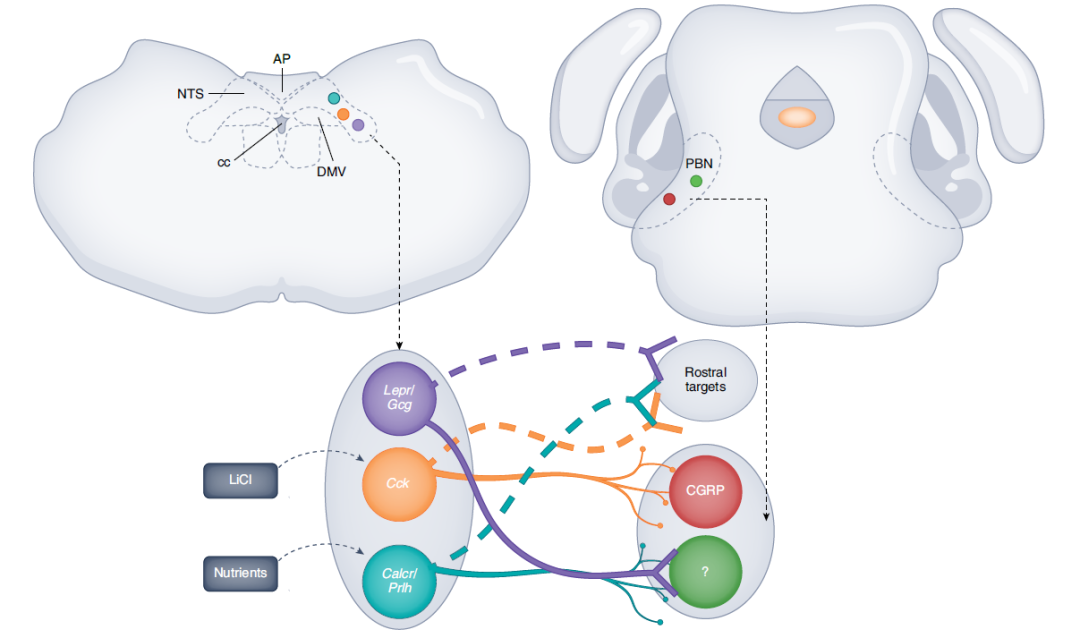
这篇综述将这些发现与其他最近发表的文献结合起来,在此基础上,建立了一个新的脑干神经回路图谱,可以预测哪组神经元控制食物摄入或引起胃肠道反应,如恶心或厌恶感;并讨论了如何利用这些信息来确定更有效治疗肥胖的方法。
他们指出的神经元中有许多都是新的且有效的减肥药物靶点,例如,一类称为 GLP1 受体激动剂的糖尿病药物可以降低血糖并有助于减少饮食摄入。鉴于孤束核神经元之间的广泛串扰,研究人员推测孤束核相关神经元也可能介导了 GLP-1 产生抑制食欲的作用。
Myers 表示,脑干中有一群 GLP1 神经元,如果你打开它们,它们就会让你停止进食,但同时会导致严重的副作用。但也许还有另一组可以让你停止进食的神经元,而且它不会让你感觉不好。有了这些神经元的详细图谱并了解这些潜在靶点的作用,可以帮助开发出副作用更少的减肥药物。
总之,这篇综述回顾了控制进食的后脑神经元的最新研究进展,尤其是位于极后区和孤束核的神经元。研究人员将这些信息与脑干神经回路图谱联系了起来,并建立了控制食物摄入和能量稳态的后脑回路模型,从而为进一步研究和开发治疗肥胖且副作用更少的药物提供了重要线索。
原始出处:
Cheng, W., Gordian, D., Ludwig, M.Q. et al. Hindbrain circuits in the control of eating behaviour and energy balance. Nat Metab 4, 826–835 (2022). https://doi.org/10.1038/s42255-022-00606-9.


