基因缺陷导致的口腔真菌感染诊疗(附慢性黏膜皮肤念珠菌病诊疗流程图)
时间:2022-10-27 17:59:28 热度:37.1℃ 作者:网络
前言
慢性黏膜皮肤念珠菌病(Chronicmucocutaneous candidiasis,CMC))是一种少见的特殊类型的念珠菌感染,其特征是患者的皮肤、黏膜和指甲对念珠菌属(Candidaspp.)和皮肤癣菌易感性增加[1]。CMC发生于患有各种获得性或遗传性免疫缺陷疾病的患者中。信号转导和转录蛋白激活因子1(signaltransducer and activator of transcription 1, STAT 1)的功能获得性突变(Gainof function GOF)呈常染色体显性遗传,是CMC最常见的遗传学病因。信号转导和转录蛋白激活因子(STAT)家族是干扰素(IFN)、细胞因子、生长因子和激素下游的关键信号分子。大多数STAT1GOF突变位于STAT1的卷曲螺旋结构域结构(coiled-coil-domains)和DNA结合结构域(DNA-bindingdomains),发生在DNA连接区(Linkerdomains)的突变文献中报告很少[2]。STAT1GOF突变患者的临床表现具有异质性,但几乎所有患者都表现出CMC的症状,且常与其他感染性疾病(细菌、真菌或病毒感染)和非感染性疾病(自身免疫/炎症、动脉瘤和肿瘤)相关[3]。
CMC最常见的表现即口腔念珠菌病,由于念珠菌长期慢性感染,且患者存在免疫缺陷,疾病常发病早且迁延不愈。慢性增殖型念珠菌病是由念珠菌感染导致的黏膜的增生性病变,具有潜在恶性风险,属于口腔念珠菌病的少见和严重类型,却为CMC患者的常见局部表现。由于临床表现具有不典型性,且临床医生对CMC认识不足,且其发病机制相对复杂,诊断和治疗较为棘手,因此常延误病情,导致患者发生口腔黏膜癌变、全身潜在其他严重感染的风险增加,严重者甚至能够危及生命。
案例经过
患者,男,19岁,以舌部裂纹伴发硬5年,出现疼痛感1年为主诉于2021年12月来口腔黏膜科就诊。患者既往5年多次以舌部裂纹为主诉看病,均被误诊为沟纹舌,未予以治疗。
临床口腔检查发现患者舌部有深浅不一沟纹,舌部明显增生肿大,呈结节样,质地硬(图A)。取患者唾液标本送至检验科行真菌培养,结果显示白色念珠菌+,菌落数>200个/mL(图B),提示诊断口腔念珠菌病。后经舌背部取病理显示上皮黏膜慢性炎症,上皮增生,表面有微脓肿形成,PAS染色可见念珠菌菌丝侵入上皮内,病理诊断为慢性增殖型念珠菌病(图C)。患者检查全血细胞分析、甲状腺功能、生化、免疫球蛋白、传染病四项等均无异常,且患者无全身系统性疾病,亦没有外来诱因,因此考虑患者有存在真菌感染相关基因缺陷的可能性。因此对患者外周血进行了二代基因外显子测序,筛查潜在的致病基因位点,结果显示患者存在STAT1基因linker区域(c.1666C>T,p.Leu556Phe)突变,该突变位点在国内外尚属首次发现。进一步取无真菌感染的父母唾液标本作为对照进行了一代测序验证,证实该基因的杂合突变是导致患者慢性念珠菌感染发生的原因(图D),因此该患者最终诊断为慢性黏膜皮肤念珠菌病。
我们首先对患者进行了抗真菌(口服氟康唑胶囊+制霉素片)治疗2个月,舌部病损基本消退,但舌背中部仍有结节,此时取患者唾液标本送至检验科行真菌培养,结果显示未见念珠菌生长。我们后续采用了ALA-PDT(光动力)对舌背残余病损进行了治疗,即将20%的5-氨基酮戊酸(ALA)敷于残余病损处2小时,之后使用光动力激光治疗仪进行照射(LH-600型,635mm,600mW,每1.5分钟1个光斑,光斑直径为1cm,光源距离病损约1.5cm),舌部结节已基本消退(图E、F)。后给予患者2~4%碳酸氢钠漱口液漱口预防疾病复发,目前还在进一步随访中。

图A 患者口腔检查舌部病损表现(初诊)
微生物检查:检验科收到唾液标本(真菌培养基鉴定)
沙氏培养基结果:念珠菌+,>200个/mL;科马嘉培养基鉴定结果:白色念珠菌。
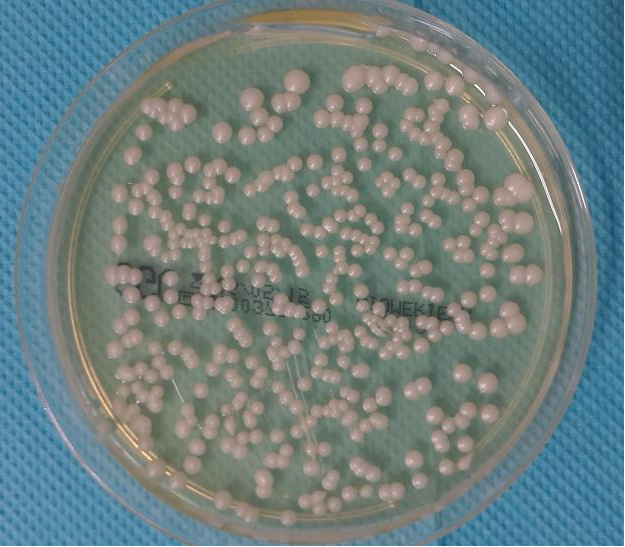
图B 唾液真菌培养检查
病理检查:舌背部取病理显示上皮黏膜慢性炎症,上皮增生,表面有微脓肿形成,PAS染色可见念珠菌菌丝侵入上皮内,病理诊断为慢性增殖型念珠菌病。
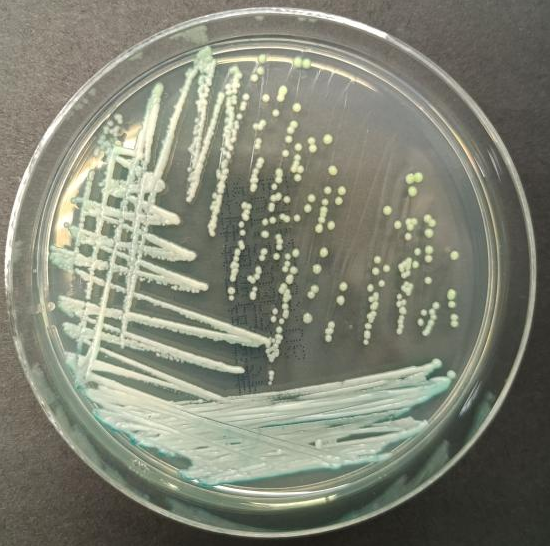
图C 舌部病理检查结果(PAS染色)
一代测序检查验证结果:以其无真菌感染的父母做对照,患者存在STAT1基因linker区域(c.1666C>T,p.Leu556Phe)杂合突变。

图D 一代测序验证结果
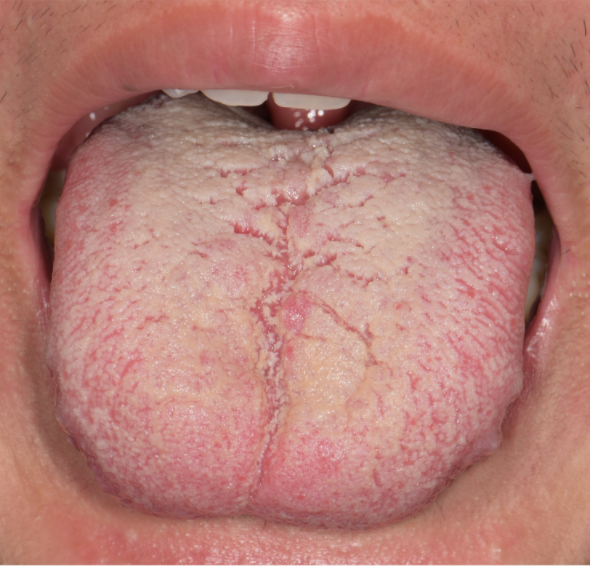
图E 舌部临床表现(抗真菌治疗后)
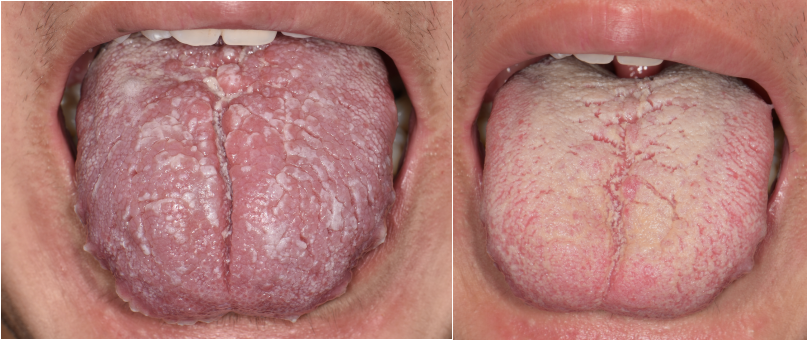
图F 治疗前后对比图
案例分析
临床案例分析
在慢性黏膜皮肤念珠菌病患者中常发生的慢性增殖型念珠菌病的治疗挑战和策略?
慢性增殖型念珠菌病虽较为少见,但属于口腔念珠菌病中最严重且具有癌变风险的类型。该种类型可伴有不同程度上皮异常增生,部分病例可发展为口腔鳞状细胞癌。2017年世界卫生组织(WHO)头颈部肿瘤分类中,将慢性念珠菌病列为口腔潜在恶性疾患。慢性增殖型念珠菌病的抗真菌治疗周期长且容易复发,为临床诊断和治疗带来了巨大挑战。
目前尚无关于慢性增殖型念珠菌病的理想治疗方法。主要包括去除可能的易感因素(如吸烟),抗真菌治疗,局部应用维甲酸,以及手术治疗等。抗真菌治疗是常见的一种治疗慢性增殖型念珠菌病的方法,但其治疗效果常不理想。因该病存在癌变风险,且临床上常见因抗真菌治疗效果不佳的迁延病例,也有采用光动力(PDT)、激光、冷冻等疗法,对抗真菌治疗抵抗的残留病损进行有效治疗。
在本例患者中,由于其存在的基因缺陷不能去除,因此在积极治疗后,在病损消退的基础上,还应采用一些预防措施,预防增殖型念珠菌病的复发。如采用2%~4%碳酸氢钠漱口液漱口、给予胸腺肽等提高自身免疫的药物等。
检验案例分析
慢性黏膜皮肤念珠菌病的进一步检查和诊断?
慢性黏膜皮肤念珠菌病是与念珠菌感染相关的一组少见的特殊类型的综合征,典型表现为皮肤、指/趾甲和黏膜的长期不愈或反复发作的念珠菌病,绝大多数由白色念珠菌引起,患者多伴有内分泌系统疾病或免疫缺陷。慢性黏膜皮肤念珠菌病的诊断需结合病史、临床表现、实验室检查和活体组织检查。
基本的实验室检查包括:真菌学检查(口腔脱落细胞10%KOH涂片镜检、唾液或含漱液念珠菌培养鉴定)、全血细胞分析、生化、抗HIV抗体检测、免疫球蛋白定量等;再根据可能的临床分型进一步检查血清电解质、内分泌指标(甲状腺功能、甲状旁腺素、皮质醇等)并可进行基因检测等。另慢性黏膜皮肤念珠菌病的口腔中常表现为慢性增殖型念珠菌病,其典型组织病理表现可见上皮增生明显,中性粒细胞浸润形成微脓肿,PAS染色可检出角化层中侵入的菌丝。
知识扩展
慢性黏膜皮肤念珠菌病的的诊疗流程
慢性黏膜皮肤念珠菌病是与念珠菌感染相关的一组少见的特殊类型的综合征,典型表现为皮肤、指/趾甲和黏膜的长期不愈或反复发作的念珠菌病。发病机制目前认为主要是由免疫缺陷引起,某些患者与遗传因素有关。由于其诊断需结合病史、临床表现、实验室检查和活体组织检查,而慢性黏膜皮肤念珠菌病患者常出现的慢性增殖型念珠菌病属于难治性念珠菌感染,因此该病诊疗是临床医生面临的重大挑战。我科在口腔念珠菌病诊断与治疗方面属于国内外先进地位,曾发表多篇论文阐述其诊疗方法[4,5],并将该病诊疗方法总结为了诊疗流程图,以期进一步规范该病的诊疗[6]。

慢性黏膜皮肤念珠菌病诊疗流程图[6]
光动力疗法的抗微生物作用
光动力疗法是一种非侵入性的新技术,其作用是基于局部或系统应用光敏剂。光敏剂可在病变组织中大量积累,之后应用一种特定波长的光对目标部位进行照射并激活光敏剂,激发态的光敏剂把能量传递给周围的氧,继而生成活性很强的单态氧,单态氧和相邻的生物大分子发生氧化反应,产生细胞毒性作用,进而导致细胞受损乃至死亡。
光动力疗法目前被公认为是一种有效杀灭病原微生物的精准靶向疗法,因其对病原微生物具有灭活作用,又被称为抗菌光动力疗法(aPDT)。目前关于光动力疗法治疗增殖型念珠菌病的临床应用,国际上报道很少,我院口腔黏膜科2020年申请开展了新技术新疗法项目,探索了光动力疗法辅助治疗慢性增殖型念珠菌病的有效性安全性单臂临床试验,研究结果显示通过光动力治疗慢性增殖型念珠菌病可有效消退抗真菌治疗抵抗的病损、改善病损表面增生等特征,减小病损面积[7]。本病例采用ALA-PDT治疗亦取得了良好的治疗效果,患者的结节增生病损基本消退,目前还在进一步随访中。
案例总结
本例病例为青年男性,临床主要表现为舌部裂纹和结节增厚,由于患者发病年龄小、全身情况良好,临床表现又类似口腔黏膜良性疾病沟纹舌的表现,易被误诊为良性疾病沟纹舌,延误诊断和治疗。慢性黏膜皮肤念珠菌病的确诊需要结合临床病史、临床表现、实验室检查和活体组织检查。本例患者首先由临床医生发现了可疑结节增厚,怀疑口腔念珠菌病,之后做了唾液真菌培养发现白色念珠菌,诊断口腔念珠菌病;又结合临床表现对舌部取病理,诊断为口腔念珠菌病中最为少见的类型,即慢性增殖型念珠菌病;进而结合基础检验项目未发现异常,且患者无全身系统性疾病,亦没有外来诱因的情况,对患者进行基因检测,通过测序和验证发现患者存在STAT1基因linker区域(c.1666C>T,p.Leu556Phe)的杂合突变,该突变位点在国内外尚属首次发现。患者最终诊断了慢性黏膜皮肤念珠菌病。在对患者进行了抗真菌剂基础治疗后,对残留病损采用了ALA-PDT(光动力)治疗,并采取了必要的措施预防复发。
该病例提示我们,年轻患者如果从儿童、青少年时期即出现舌部裂纹,有逐渐增厚发硬的表现,即使没有症状,也应引起重视,不可直接诊断良性口腔黏膜疾病沟纹舌,应进行病理检查排除慢性增殖型念珠菌病的可能,进而通过基因测序筛查可能的基因突变,以确定有无发生慢性黏膜皮肤念珠菌病的可能,并应给予患者相应的治疗措施,针对慢性增殖型念珠菌病可采取抗真菌剂联合PDT的治疗方案,并对患者提供遗传及疾病预防的咨询和指导。
专家点评
孙志强副主任医师,北京大学口腔医院检验科
慢性黏膜皮肤念珠菌病是与念珠菌感染相关的一组少见的特殊类型的综合征,由于几乎100%的患者患有长期或反复的口腔念珠菌病,因此常首诊于口腔科。但目前口腔科医师对该病的认识不足,且该病的诊断常依赖临床医生和检验科、病理科医生的联合,因此常常造成该病的误诊或漏诊,延误病情。而慢性黏膜皮肤念珠菌病患者口腔常发生慢性增殖型念珠菌病,后者是由念珠菌感染导致的黏膜的增生性病变,具有潜在恶性风险,因此延误诊断及治疗后果严重。
本病例中临床医生能够准确识别口腔念珠菌病的少见类型,即增殖型念珠菌病的不典型临床表现,并通过进一步进行微生物学筛查、病理诊断做出准确诊断,实属难得。除此之外,对本例患者基因筛查发现的STAT1基因linker区域(c.1666C>T,p.Leu556Phe)杂合突变在国内外均未曾报告,属于创新性新发现。临床医生采取了新颖的治疗方法,即抗真菌剂联合ALA-PDT对增殖型念珠菌病的临床表现进行治疗,及时控制病情,给予了患者预防复发的措施,为临床医生对该类患者的治疗和预防提供了重要参考。
本病例提示临床医生在临床工作中应注重与检验科、病理科医生的融合和交流,共同对疾病的诊疗做出决策,减少该病的漏诊和误诊。
参考文献:
1. Martinot M, Korganow AS, Wald M, et al. Case Report: A New Gain-of-Function Mutation of STAT1 Identified in a Patient With Chronic Mucocutaneous Candidiasis and Rosacea-Like Demodicosis: An Emerging Association[J]. Frontiers in Immunology, 2021, 12:760019.
2. Zhang W, Chen X, Gao G, et al. Clinical Relevance of Gain- and Loss-of-Function Germline Mutations in STAT1: A Systematic Review[J]. Frontiers in Immunology, 2021, 12:654406.
3. Depner M, Fuchs S, Raabe J, et al. The Extended Clinical Phenotype of 26 Patients with Chronic Mucocutaneous Candidiasis due to Gain-of-Function Mutations in STAT1[J]. Journal of Clinical Immunology, 2016, 36(1):73-84.
4. 刘宣玲, 华红. 慢性皮肤粘膜念珠菌病[J]. 北京口腔医学, 2006, 14(1):3.
5. Liu X, Hua H. Oral manifestation of chronic mucocutaneous candidiasis: seven case reports[J]. Journal of Oral Pathology & Medicine, 2007, 36(9):528-532.
6. 华红,高岩. 口腔黏膜病病例精粹80例[M].第一版. 北京:北京大学医学出版社,2019.
7. 张文卿.口腔慢性增殖型念珠菌病的回顾性队列研究及光动力疗法辅助治疗有效性与安全性的探索性单臂临床试验[D].北京大学. 2022.


