ICU中的氧疗目标:保守氧疗?还是自由氧疗?
时间:2023-07-31 17:24:42 热度:37.1℃ 作者:网络
1 背景
我们的地球诞生于大约48亿年前。在起初的早期阶段,地球的大气层不含氧气。在地球诞生大约10亿年后,经过复杂的生物进化出现了生命,蓝藻是地球上最早的生命形式之一,它通过光合作用产生了氧气,导致大气中氧气的增加。在几十亿年后的1774年,Joseph Priestly确定了氧气是维持地球生命的气体。一个多世纪后的1885年,George Holtzaple报道了通过给氧治疗肺炎的情况。Lorraine Smith首次报道了氧对实验小鼠造成的急性毒性作用。他指出,随着体内血氧水平的升高,氧的毒性效应逐渐增加。
2 什么是高氧血症?
高氧血症是指机体在细胞和组织水平上暴露于高于正常水平的氧分压。通常,许多临床医生倾向于采用自由氧疗方法作为预防意外低氧血症的措施。使问题变得复杂的是,连续脉搏血氧监测仪却无法识别出高氧血症。在一项来自内-外科综合ICU的观察性队列研究中,在机械通气的第一周,平均时间加权PaO2为144 mmHg;此外,在持续机械通气期间的80%时间内,PaO2>80 mmHg。有多种不同的高氧血症的定义;PaO2在100–125 mmHg之间,被认为是轻度高氧血症,而大于200 mmHg则是重度高氧血症。
3 高氧血症的生理后果是什么?
Lorraine Smith首先报道了过度给氧引起的潜在害处,并在实验小鼠中描述了高氧血症相关的急性肺改变。氧分子具有作为“电子受体”的独特性质。然而,新接受的电子仍然是不成对的,此时的氧分子被称为氧自由基。参与生物反应的氧自由基称为活性氧(ROS)。ROS在清除突变的细胞或受损细胞中起着重要的生理作用。这一过程被称为细胞凋亡,能够产生新的细胞来取代突变或受损的细胞。高氧血症可能导致ROS水平升高。通常情况下,抗氧化剂(包括超氧化物歧化酶、过氧化氢酶以及维生素C和E)可以清除过量的ROS。然而,面对高氧血症,抗氧化机制被迅速催垮,导致过量的ROS破坏正常细胞,对不同器官产生有害影响(图1)。表1总结了高氧血症的临床效果。

图1. ROS在通过细胞凋亡,在清除突变或受损细胞中发挥生理作用。过量的ROS被抗氧化剂清除。在高氧血症状态下,ROS水平上升过高,抗氧化机制迅速被催垮。正常细胞的破坏随之而来。
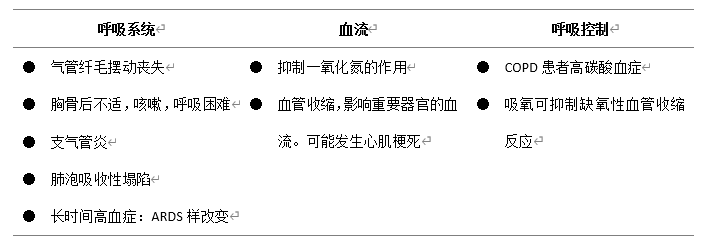
表1.过度给氧的临床影响
3.1 肺
气管纤毛摆动丧失,导致气管炎是高氧血症肺部早期中毒表现之一,其临床特点有胸骨后不适,咳嗽,以及呼吸困难。氮气,不易被吸收,存留在肺泡内起到“夹板固定”作用,保持肺泡处于开放状态。过度氧疗,肺泡内氧含量上升,氧气的吸收较氮气快,就容易发生肺泡塌陷。高FiO2水平导致肺部的病理生理变化,与急性呼吸窘迫综合征(ARDS)时发生的变化相似。胸片和胸部CT图像所见,通常与ARDS中观察到的放射学改变难以区分(表1)
3.2 血管收缩剂效应
一氧化氮是一种天然的血管舒张剂,氧气对其有抑制作用。在高血氧水平状态下,一氧化氮被抑制,从而产生血管收缩效应,导致重要器官的血流受损。冠状动脉血管收缩可能会导致急性心肌缺血。
3.3 呼吸的控制
高FiO2给氧通常会导致高碳酸血症的进展,尤其是在慢性阻塞性肺病(COPD)急性加重的患者中。通常认为高碳酸血症是缺氧所引起呼吸驱动被抑制的结果。高FiO2水平在起初可能导致分钟通气量的减少和PaCO2水平的上升。然而,在相同的高FiO2水平下持续氧疗超过15分钟,起初的分钟通气量减少则显著减弱。氧诱导的缺氧性肺血管收缩机制的失功,是高碳酸血症发展的更恰当的解释。高FiO2水平会导致肺部缺氧区域的血管舒张,血液流向通气不良的区域,从而导致肺内分流和高碳酸血症。此外,随着FiO2水平的升高,血红蛋白的氧饱和度也会增加。氧饱和度的升高通过反向荷尔登效应导致血红蛋白在肺部不易与二氧化碳结合。然而,如果通气量仍然很低,就像COPD患者经常发生的那样,二氧化碳的清除就会受损,导致高碳酸血症。
4 临床实践中的研究证据有何提示?
已有许多试验针对不同PaO2和氧饱和度水平作为氧疗目标的临床效果进行了研究(表2)。
表2. 评估危重患者自由与保守氧疗目标的主要研究
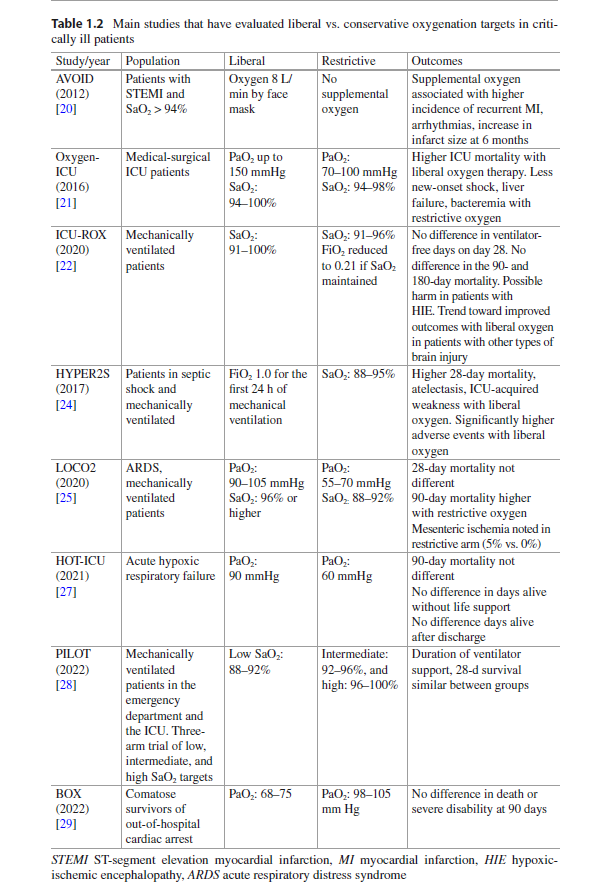
4.1 ST段抬高型心肌梗死(STEMI)的氧疗:AVOID试验
大多数急性心肌梗死患者都接受了氧疗。这种治疗干预的前提是给氧可以改善氧输送并减少对缺血心肌的损伤。然而,在血氧正常的STEMI患者中给氧是否能改善临床结果?
AVOID研究是由澳大利亚墨尔本的救护车服务机构进行的一项多中心、非盲随机对照试验(RCT)。该研究纳入的是STEMI且基线血氧饱和度>94%的患者。干预组通过面罩以8L/min的速度进行氧疗;对照组未接受氧疗。所有患者均由护理人员给药口服阿司匹林300mg。持续抗血小板治疗、抗凝选择和经皮介入治疗均按照当地的方案来进行。在本研究中,氧疗并未使STEMI患者有临床获益。相反,在接受氧疗的患者中,6个月时的磁共振成像显示心肌梗死面积增加。此外,吸氧后复发性心肌梗死和心律失常的发生率也较高。
4.2 Oxygen-ICU 研究
最近发表的几项随机对照试验评估了血氧水平对ICU机械通气患者的影响。OXYGEN-ICU研究,是一项单中心RCT,在意大利的一家内-外科ICU中进行,旨在评估氧疗的影响。该研究纳入的是预计ICU住院时间超过72小时的患者。在保守氧疗组中,目标PaO2水平设定在70至100 mmHg之间,氧饱和度水平设定在94%至98%之间。在自由氧疗(常规治疗)组中,遵循标准治疗。在自由氧疗组中,最高的PaO2水平允许达到150 mmHg,血氧饱和度达97%至100%之间。自由氧疗组和保守氧疗组的平均每日时间加权PaO2水平存在显著差异(102 mmHg,IQR:88-116 vs. 87 mmHg,IQR:79-97)。这项研究显示,自由氧疗的ICU死亡率显著高于保守氧疗(20.2% vs. 11.6%,p=0.01)。此外,保守氧疗组中的新发休克、肝衰竭和菌血症的发生率也较低。
4.3 ICU-ROX研究
澳大利亚-新西兰重症学会临床研究组进行了一项多中心研究(ICU-ROX研究),纳入的是预计入组后需要机械通气的患者。随机分成保守氧疗组和自由氧疗组,保守氧疗组的氧饱和度保持在91%和96%之间。如果氧饱和度超过该范围,则将FiO2水平降低至目标水平。如果一直都可达到目标氧饱和度水平,则FiO2水平逐步降低至21%。在自由氧疗(常规治疗)组中,没有进行特定的干预来限制FiO2水平,氧饱和度保持在91%至100%之间。两组在第28天的非机械通气天数上并没有显著差异(保守氧疗组 vs. 自由氧疗组:21.3天 vs. 22.1天)。此外,两组间90天和180天死亡率也没有显著差异。在亚组分析中发现,对于缺氧缺血性脑病(HIE)患者,自由氧疗可能带来有害的效果。接受自由氧疗的HIE患者,在180天时非机械通气天数更少,180天死亡率更高,格拉斯哥结果量表上的不良结果发生率也更高。在其他类型脑损伤的患者中,事后分析发现,自由氧疗与预后的改善相关。对脓毒症患者的事后分析显示,自由氧疗有提高90天生存率的趋势。然而,这些发现是假设产生的,需要在未来的对照研究中进一步评估。
4.4 HYPERS2S研究
这是法国的一项多中心研究,在接受机械通气的感染性休克患者中把保守氧疗和自由氧疗进行了比较。在自由氧疗组中,机械通气的首个24小时FiO2水平维持在100%。在保守氧疗组,血氧饱和度维持 在88-95%之间。由于对100%浓度给氧的安全性产生了担忧,该研究提前停止。在研究停止时,接受100%浓度给氧的患者28天死亡率更高。100%浓度吸氧后,严重不良事件的总体发生率也显著增加。自由氧疗组的ICU获得性虚弱发生率是保守氧疗组的两倍;肺不张的发生率也明显升高。
4.5 LOCO2试验
LOCO2试验是在法国的13家ICU中进行的多中心RCT。研究纳入的是符ARDS柏林定义并接受机械通气的患者。在保守氧疗组中,目标PaO2水平在55-70 mmHg,氧饱和度维持在88-92%。在自由氧疗组中,目标PaO2水平在90-105 mmHg,氧饱和度≥96%。在第28天,任何原因的死亡(主要结果)均未观察到差异。在次要结果中,保守氧疗组的90天死亡率高于自由氧疗组。重要的是,保守氧疗组的肠系膜缺血发生率明显升高(5% vs. 0)。基于这一不良结局的发现,出于安全考虑,在第205名患者入组后,该研究停止了。
4.6 HOT-ICU试验
HOT-ICU试验纳入的是来自35家ICU的急性低氧性呼吸衰竭危重症患者。患者通过开放系统以10L/min的最小流速接受氧疗,或通过封闭系统以最小50%的FiO2接受氧疗(包括有创和无创通气),预计需要氧疗至少24小时。保守氧疗组的目标PaO2设定为60mmHg,而自由氧疗组为90mmHg。保守组和自由组的90天死亡率(主要结果)没有显著差异(42.9% vs. 42.4%,p=0.64)。在次要结果中,两组间不需生命支持的存活天数和出院后的存活天数也没有显著差异。本研究支持在急性低氧血症性呼吸衰竭患者中,较低的PaO2目标值为60 mmHg,而不是90 mmHg,且没有不良临床结局出现。
4.7 PILOT试验
PILOT是单中心集群随机试验,在急诊和ICU接受机械通气的患者中评估低氧饱和度(88-92%),中等氧饱和度(92-96%),和高氧饱和度(96-100%)之间的影响。试验纳入了2987名患者;其中2541例纳入初步分析。三组中,28天的非机械通气天数(主要结局)相似。低中高氧饱和度三组患者的非机械通气天数中位数分别为20 (IQR: 0–25), 21 (IQR: 0–25),和 21 (IQR: 0–26),p = 0.81。三组患者的28天死亡率也相似。PILOT试验表明,与中等或高氧饱和度目标相比,以90%或更低的低氧饱和度为目标,并不能缩短呼吸机支持的持续时间或提高生存率。
4.8 缺氧缺血性脑病患者的氧合目标
BOX试验没有证实ICU-ROX研究的亚组分析结果,ICU-ROX研究表明,缺氧缺血性脑病患者的氧合目标越高,预后越差。在BOX试验这项单中心研究中,对院外心脏骤停昏迷幸存者的保守氧疗目标(PaO2 68–75)和自由氧疗目标(PaO2 98–105 mm Hg)进行了比较。研究结果发现保守的氧疗策略与自由的氧疗策略在90天时的死亡或严重残疾(主要结果)方面不存在显著性差异。
要点
● 有强有力的临床证据表明,过度氧疗会产生不良后果,包括死亡率增加。
● 氧疗的安全限度尚不清楚。其安全范围可能因原发病不同而存在差异。缺氧缺血性脑病可能会加剧过度氧疗不良反应的脆弱性。
● 在大多数临床情况下,机械通气患者的氧饱和度目标在91-96%之间可能是足够的。
● 应根据氧饱和度目标来下调FiO2水平,而不是任意调定一个较低的FiO2。
● 我们必须把氧气当作一种药物来对待,并理性地使用;毫无节制地给氧会产生不良影响。
● 危重病患者的目标氧饱和度水平应通过医嘱加以设定,并相应地调整滴定FiO2水平。


