Nature子刊:中山大学赵绮毅/苏士成/廖建友发现机械转导信号调节癌症干细胞的新机理
时间:2023-01-19 15:01:05 热度:37.1℃ 作者:网络
新出现的证据表明,需要生物力学环境来支持癌症干细胞(CSCs),这些干细胞在耐药性中起着至关重要的作用。然而,机械转导信号如何调节CSCs及其临床意义尚不清楚。
2023年1月16日,中山大学赵绮毅、苏士成及廖建友共同通讯在Nature Communications 在线发表题为“Niche stiffness sustains cancer stemness via TAZ and NANOG phase separation”的研究论文,该研究表明生态位刚度通过TAZ和NANOG相分离维持癌症干性。通过对患者病变的临床超声弹性成像和对手术样本的原子力显微镜,作者揭示了基质刚度的增加与乳腺癌患者对新辅助化疗反应差、预后差和CSC丰富有关。
机制上,生物力学激活的TAZ通过与NANOG相分离增强CSC性能。TAZ-NANOG相分离依赖于NANOG N端激活域的酸性残基,促进SOX2和OCT4的转录。在治疗上,靶向NANOG或TAZ可减少CSCs并增强体内的化学敏感性。总的来说,这项研究证明了多能性转录因子的相分离将生态位中的机械线索与CSCs的命运联系起来。

生态位中的组织力和机械信号决定了干细胞和祖细胞的命运,并在组织发育和稳态中发挥关键作用。多能干细胞受到机械力的严格调控,以动态控制其自我更新和分化,这是维持正常结构和功能所必需的。在张力稳态中的有效性可能改变细胞命运,启动细胞转化,促进致瘤性病变的后期发展。响应细胞外生物力学力的机械响应传感器与细胞内生化信号通路耦合,然后调节细胞行为。
肿瘤干细胞(CSCs)表现出自我更新的特性,并在肿瘤起始和耐药中发挥关键作用。作为干细胞,CSCs也存在于一个生态位中,这个生态位保持了CSCs的主要特性,保持了它们的表型可塑性,并保护它们免受药物和免疫反应的影响。研究表明,生态位中的基质细胞通过细胞因子、膜蛋白和细胞外囊泡中的非编码RNAs等生化因子诱导和维持CSC的干性和耐化学药性。
最近的证据表明,机械破坏在调节癌症茎秆中起着重要作用。Hippo通路的转录共激活因子TAZ是一种重要的机械传感器,与多种疾病的发病机制有关(包括癌症)。然而,关于CSCs的机械生态位是否驱动患者肿瘤进展的直接临床证据仍然缺乏。更重要的是,生态位刚度如何介导CSCs特性的潜在机制在很大程度上尚不清楚。
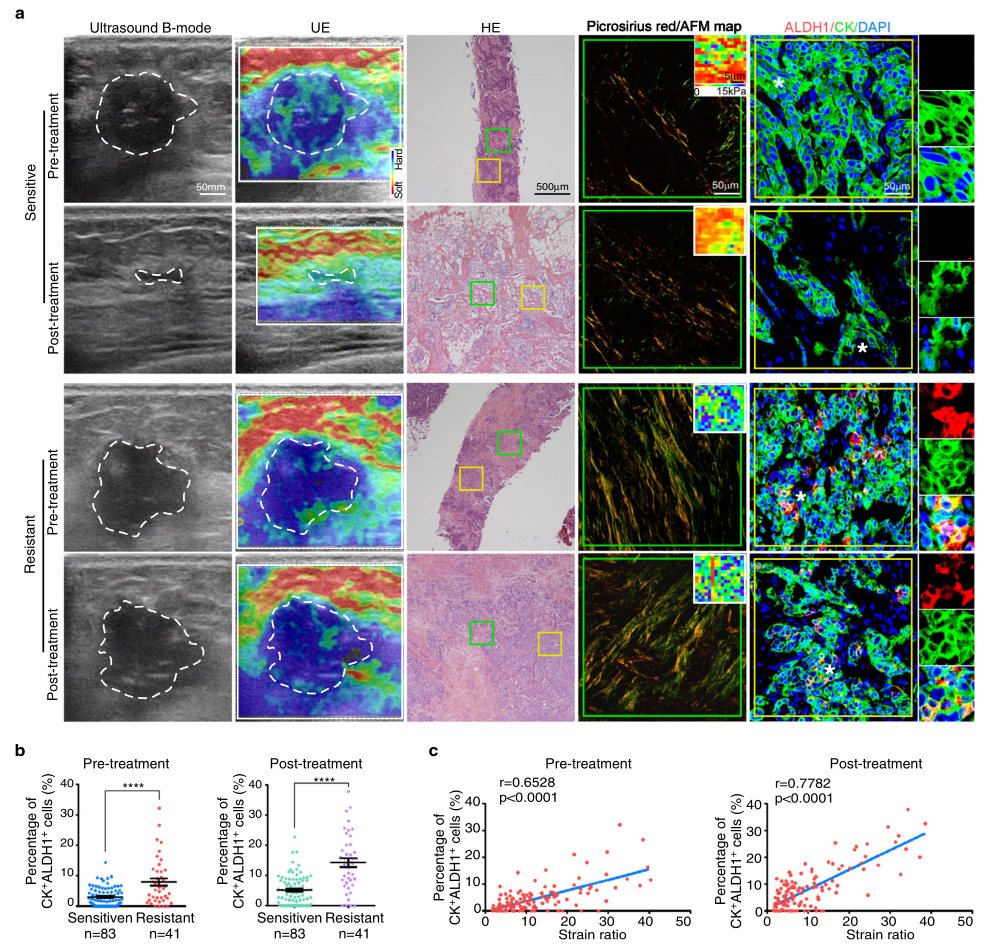
基质刚度与人乳腺癌CSC丰度相关(图源自Nature Communications )
新辅助(术前)全身治疗的使用目前正在增加,因为它有助于保乳手术和测量体内对全身治疗的反应。然而,先前的研究报道了新辅助化疗(NAC)是比较治疗期间肿瘤微环境变化的理想临床评价模型,因为可以从同一患者中获得配对的治疗前诊断活检和治疗后手术切除的样本。使用临床实践超声弹性成像(UE)对患者的病变和原子力显微镜(AFM)对手术标本,可以分别测量组织和细胞水平的基质刚度。
总之,该研究揭示了液-液相分离作为CSCs中生态位刚度和多能性因子转录活性之间的信号纽带的作用。这些发现扩展了CSC研究的重点,并表明生物力学线索是CSC新治疗策略的一个有吸引力的靶点。
原文链接:
https://www.nature.com/articles/s41467-023-35856-y


