ICU细菌和真菌感染管理:诊断、治疗和预防建议
时间:2023-08-11 21:42:45 热度:37.1℃ 作者:网络
摘要
细菌和真菌感染是重症监护病房(ICU)的常见问题。大型跨国点患病率调查发现,任何时候都有高达50%的ICU患者诊断为细菌或真菌感染。
ICU感染有其自身挑战,致病生物通常具有内在和获得性耐药机制,使得经验性和针对性抗菌药物选择具有挑战性。ICU感染与患者较差的临床结局相关。我们回顾了ICU细菌和真菌感染的流行病学,讨论了感染的危险因素、诊断和管理方法,以及预防感染的常用策略。
前言
细菌和真菌感染是ICU的常见诊断。2017年Vincent等人报告了88个国家,1150个中心的24h点患病率调查,在可获得感染数据的15,165例患者中,8135例(54%)确诊或疑似感染,10,640例(70%)接受了至少一种抗菌药物治疗,ICU继发感染1760例/8135例(22%);5259例具有临床意义的微生物学感染以革兰氏阴性菌为主(3540/5259;67%),真菌感染占16%(864/5259)。这些数据与之前的多国点流行病学研究类似,如2009年进行的EPIC II,报告中51%的患者认为感染,71%开具抗生素,其中革兰氏阴性细菌感染占62%,真菌感染占19%。
ICU细菌或真菌感染死亡率高于未感染患者。ICU感染患者住院死亡率约为30%。继发性细菌或真菌感染和耐药感染的存在是死亡独立危险因素,与社区获得性感染相比,死亡几率增加(OR:1.32;95%CI 1.10-1.60)。ICU感染通常由耐药细菌和越来越多的耐药真菌引起。这些感染称为抗菌素耐药(AMR),已对住院患者产生重大影响。
全球范围内,抗菌素耐药性比率因区域而异。革兰氏阴性菌面临的主要挑战包括产生广谱β -内酰胺酶(ESBL)的肠杆菌、阻遏AmpC(头孢菌素酶)菌、产生碳青霉烯酶的肠杆菌(CPE)、耐碳青霉烯的鲍曼不动杆菌(CRAB)和耐碳青霉烯的细菌铜绿假单胞菌。革兰氏阳性挑战包括耐甲氧西林金黄色葡萄球菌(MRSA)和耐糖肽肠球菌(GRE)。
尤其是考虑到ICU高死亡率,以及相对地无法快速诊断和提供有效抗菌治疗,抗真菌耐药和耐药真菌感染成为一种新出现的威胁。在真菌病原体中,多重耐药耳念珠菌的出现和全球蔓延,已导致数次医疗机构爆发事件。据报道,非白念珠菌的血流感染,对包括唑类和棘白菌素在内的一线抗真菌药物敏感性降低。这方面的例子包括对氟康唑和棘白菌素耐药的光滑假丝酵母菌,以及最近出现对氟康唑耐药的近平滑念珠菌。已证明,近平滑念珠菌在新生儿和成人重症监护病房中持续存在并导致爆发。
在丝状真菌中,最常见的呼吸道真菌烟曲霉,对三唑类抗真菌药物的耐药性具有重要临床意义。由唑类抗药性菌株引起的曲霉菌感染,在初次使用唑类和长期接受唑类药物治疗的患者中均可见到,相关死亡率增加,对诊断和治疗构成了明显的挑战。对一种或多种抗真菌剂具有内在抗药性的霉菌引起的感染数量正在增加,值得注意的例子包括毛霉菌属、镰刀菌属、塞多孢霉属和多育节荚孢霉。
入住ICU与发生医院感染的许多危险因素有关,包括呼吸机/医院获得性肺炎(VAP/HAP)、导管相关性血流感染、手术部位感染和尿路感染(UTI)。使用中心静脉导管、有创机械通气、镇静和瘫痪、复杂的手术、广谱抗菌药物使用以及患者免疫状况,都增加了继发感染的风险。对于那些在ICU经历继发性细菌和真菌感染,并给医疗服务带来重大经济负担的人,预后往往更差。
最近新冠肺炎大流行期间,突显了ICU患者细菌和真菌感染的挑战。总体而言,新冠肺炎中细菌和真菌的混合感染很少见,但在ICU中的发病率很高。感染预防和控制措施的崩溃、广谱抗菌剂的使用增加以及新冠肺炎带来的医院环境变化,可能导致了此期间ICU多药耐药细菌感染的暴发。
季节性流感和新冠肺炎疫情都导致更大比例的危重患者面临继发真菌联合感染的风险。已观察到的导致新冠肺炎患者合并感染的真菌病原体包括曲霉菌、毛霉菌和念珠菌。强调新冠肺炎真菌混合感染发病机制的流行病学、临床和宿主危险因素、免疫学机制和代谢反应是复杂的,Hoenigl等人对此进行了广泛综述。
本综述将探讨ICU细菌和真菌感染的诊断、管理和预防策,并将阐述目前和未来对ICU中疑似细菌和真菌感染患者的诊断和管理方法,以及围绕预防继发感染的证据基础。
ICU细菌和真菌感染诊断面临的挑战
ICU患者感染的诊断可能具有挑战性。器官支持可能掩盖传统的诊断因素,例如全身炎症反应综合征(SIRS)的特征,包括低血压或发热,以及特定器官感染的临床特征。临床病史和检查可能是有限的,与作出治疗决策的紧迫性相比,诊断往往需要很长的时间。虽然已经开发了预测工具来支持脓毒症的早期发现,但在许多情况下的总体表现仍然有限。
目前指南建议,脓毒症诊断基于临床判断,而不是依赖更客观的决策支持工具。当怀疑有脓毒症时,及早识别、调查和适当的处理对于优化临床结局至关重要。
细菌和真菌感染的危险因素
表1概述了与ICU频繁感染综合征相关细菌和真菌感染的常见危险因素。感染风险因微生物病原菌、感染部位、患者和局部因素而异。与医院一般人群相比,ICU细菌和真菌感染率通常明显更高。与感染风险增加相关的常见因素包括内在因素,例如免疫抑制、合并症和危重疾病。可改变的危险因素包括器官支持,例如机械通气、血液滤过和全肠外营养(TPN);外科手术;以及需要延长住ICU时间。
表1重症监护室发生细菌和真菌感染的危险因素
诊断
内在因素
可改变因素
念珠菌血流感染
● 念珠菌定植
● 糖尿病
● 胃肠穿孔
● 年龄较大(>65 岁)
● 胰腺炎
● 脓毒症/严重疾病
● 血液/实体器官恶性肿瘤
● 肝衰竭/肝硬化
● 胎龄(新生儿)
● APGAR 评分低
● 透析
● 全身使用广谱抗生素
● 中心静脉导管
● 皮质类固醇和免疫抑制剂
● 近期胃肠道手术
● 左心室辅助装置的使用
● 长期入住 ICU
● 长时间机械通气
● 全肠外营养
● 体外膜肺氧合 (ECMO)
● 静脉注射药物
侵袭性曲霉菌病
● 长期或严重中性粒细胞减少症
● 血液系统恶性肿瘤
● 严重疾病
● 创伤和烧伤
● 潜在呼吸道疾病(例如囊性纤维化)
● 糖尿病
● 心血管疾病
● 严重流感
● 严重COVID-19
● 细胞介导的免疫缺陷
●pentraxin-3、TLR-3、TLR-4 和 dectin-1 的多态性
● 全身使用皮质类固醇和其他免疫抑制剂
● 化疗
● 造血干细胞移植(同种异体)
● 嵌合抗原受体 T 细胞治疗
● 实体器官移植
● 移植物抗宿主病
● 免疫治疗(例如酪氨酸激酶抑制剂和 TNF-α 抑制剂)
● 延长住ICU时间
毛霉菌病
● 糖尿病控制不佳
● 代谢性酸中毒
● 长期或严重中性粒细胞减少症
● 创伤和烧伤
● 血液系统恶性肿瘤
● 严重 COVD-19
● 全身使用皮质类固醇
● 造血干细胞移植
● 器官移植
● 去铁胺治疗(铁螯合疗法)
● 营养不良
● 静脉注射吸毒
肺孢子菌肺炎
● 遗传性免疫缺陷
● 获得性免疫缺陷(HIV/AIDS)
● 免疫抑制(例如皮质类固醇)
耐药/耐受真菌感染
● 囊性纤维化
● 血液/肿瘤恶性肿瘤
● 危重患者
● 腹腔念珠菌感染
● 广谱预防性抗真菌治疗
● 广谱经验性抗真菌治疗
呼吸机/医院获得性肺炎
● 男性
● 年龄较大
● 已有肺部疾病
● 昏迷/低GCS
● 烧伤
● 获得性免疫缺陷综合征(艾滋病)
● 头部外伤
● 多器官系统衰竭
● 既往使用过抗菌药物
● 机械通气
● 神经外科手术
● 颅内压监测
● 重新插管
● 离开 ICU
血流感染
● 病情严重程度
● 肝脏疾病
● 手术表现
● 侵入性装置(例如 CVC)
● 侵入性操作
● 入院期间进行手术
手术部位感染
● 病原微生物定植(例如金黄色葡萄球菌)
● 年龄增长
● 合并症(糖尿病、肥胖)
● 手术过程
● 抗菌药物预防
● 手术室规范
尿路感染
● 病情严重
● 紧急置管
多重耐药细菌
● 先前定植耐多药病原体
● 长期护理要求/住院治疗
● 疾病严重程度
● 慢性呼吸道疾病
● 心血管疾病
● 先前接触过抗菌药物
● 延长 ICU 住院时间(>7 天)
● 机械通气/气管切开术
缩写:SPP,物种;APGAR,外表、脉搏、面容、活动、呼吸评分;ICU,重症监护病房;TLR,肿瘤坏死因子;HIV/AIDS,人类免疫缺陷病毒/获得性免疫缺陷综合征;GCS,格拉斯哥昏迷评分;CVC,中心静脉导管
耐药菌感染的流行病学可能因地域而异,但对于面临携带和感染多重耐药(MDR)生物体风险的人,应考虑常见危险因素。对于多耐药细菌,常见危险因素包括长期居住在护理机构、最近入院、既往使用广谱抗菌药物、已知定植以及最近前往高流行地区。抗真菌耐受性和耐药真菌感染是ICU一个新出现的问题,其危险因素包括已知定植、长期抑制性或预防性使用抗真菌药物,以及既往接受过抗真菌治疗(例如血液学、囊性纤维化、长期入住ICU患者)。
传统诊断途径
细菌和真菌感染的传统实验室诊断途径依赖于培养的方法,这些方法可以得到临床评估、放射学研究和生物标志物信息支持。图1概述了支持细菌和真菌感染决策的常见诊断方法。该图强调诊断决策从来都不是单一事件。医生必须对特定诊断测试提供的信息有基本了解,并有信心解释这些信息。一般来说,诊断可用于支持抗菌治疗的开始、靶向、个体化和停止。表2总结了决策路径各个阶段各种诊断方式的优缺点。
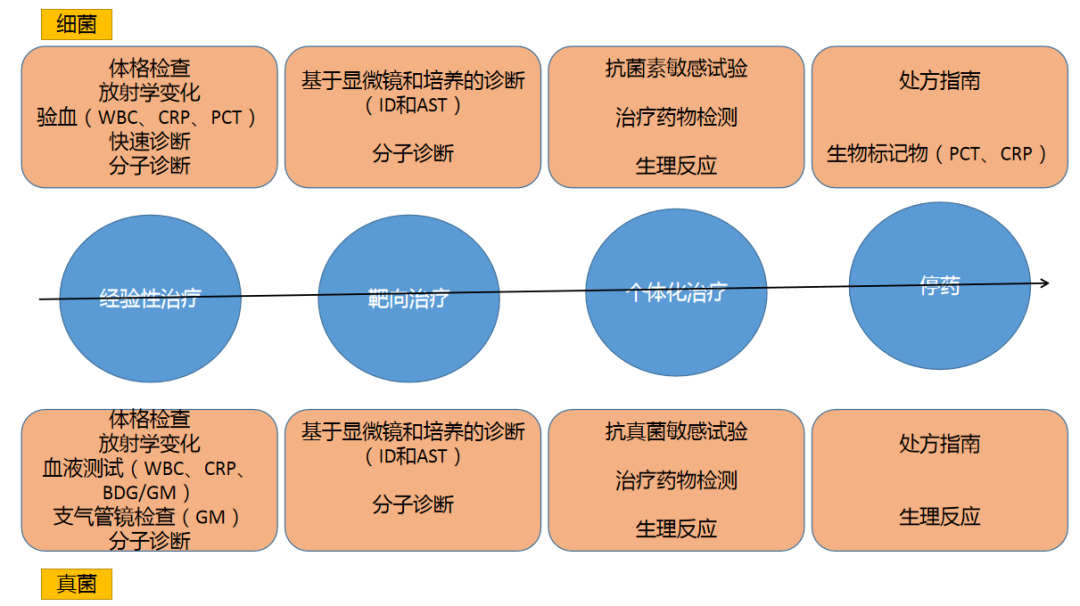
图1不同阶段影响抗菌决策的常见因素
缩写:WBC:白细胞计数;CRP:C-反应蛋白;PCT:降钙素原;ID:微生物识别;AST:抗菌药物敏感性试验;BDG:β-D-葡聚糖;GM:半乳甘露聚糖。
表2 支持抗细菌和真菌感染决策的常见诊断方法
诊断方式
特征
在抗菌药物决策地诊断性应用
经验性治疗
靶向治疗
优化
停药
血培养(细菌)
诊断能力提高*:
● 20mL; 65-76% 灵敏度
● 40mL; 80-89% 灵敏度
● 60mL; 95-98% 灵敏度
不适用
● 有针对性的抗菌药物选择。
● 感染性微生物的已知表型
●最低抑菌浓度指导给药
●促进基于证据的治疗持续时间
细菌PCR
多重 PCR:
●更高水平的微生物检测,如细菌培养
● 抗菌药物耐药基因鉴定
根据等待时间,可能会延迟开始治疗以等待结果
● 尽早转向有针对性的治疗(降级)
● 确诊/排除微生物的存在
不适用
不适用
降钙素原
细菌感染诊断:
● 敏感性88%
● 特异性81%
● 区分细菌与病毒感染
不适用
不适用
●可以减少抗生素的使用而不影响感染相关的结局
C反应蛋白
细菌感染诊断:
● 敏感性75%
● 特异性67%
● 可支持细菌感染的诊断
不适用
● 与药物暴露的联系,可能有助于抗菌药物药效学的体内评估
● 可以缩短抗菌治疗持续时间而不影响感染相关的结局
血培养(真菌)
诊断:
● 50% 播散性念珠菌病例呈阳性
不适用
● 有针对性地选择抗菌药物治疗。
● 感染性微生物的已知表型
● 最低抑菌浓度指导剂量
● 促进基于证据的治疗持续时间
半乳甘露聚糖
BAL 上的半乳甘露聚糖
● 敏感性82-89%
● 特异性96-99%
● 根据等待时间,可能允许延迟开始治疗
● 可以支持诊断和靶向治疗
● 与药物暴露的联系可能支持抗菌药效的体内评估
不适用
● 灵敏度:75%
● 特异性:85%
●阳性预测值较差,阴性预测值良好
● 容易出现假阳性
● 毛霉菌和隐球菌感染呈阴性
● 可以支持围绕侵袭性真菌感染诊断的决策
不适用
不适用
● 支持停止该行为的好处不明确
真菌PCR
念珠菌 PCR - 已证实、可能或可能的念珠菌病:
● 灵敏度 73%
● 特异性 95%
高出血培养的敏感性。
曲霉菌 PCR:
● 灵敏度 80.5%
● 特异性 78.5%
综合征多重检测可用于阳性血培养。具有高灵敏度/特异性的快速识别。
● 根据等待时间,可能会延迟开始治疗。
● 可以支持诊断和针对性治疗。
● 可检测新兴抗真菌耐药基因标记(例如CYP51A耐药)
不适用
T2 念珠菌组
血培养呈阳性:
● 敏感性 91%
● 特异性 99%
低流行率环境中的 PPV 较低(流行率 <1% 时为 15-31%)。
不适用
● 微生物鉴定
● 未报告敏感性数据
● 基于诊断的循证持续时间
注:*血培养瓶通常每瓶收集10ml,因此每套20ml(需氧和厌氧)。
缩写:N/A,不适用;MIC,最低抑菌浓度;PCR,聚合酶链式反应;C.F.,比较;PPV,阳性预测值;NPV,阴性预测值;ID,识别;CYP,细胞色素P45
重要的是考虑到诊断性测试在决策的不同阶段可能产生的影响。确保正确使用诊断性研究,有助于确保通过提供可靠和正确的信息做出最佳治疗决策。这一概念是诊断管理的关键组成部分,在确保诊断实验室能够以最佳方式支持临床决策方面很重要。这在一定程度上依赖于提出请求的医生对测试的敏感性、特异性和预测值的了解,以确保其结果能够得到适当的解释并应用于更广泛的决策环境。
诊断学研究进展
100多年来,微生物诊断主要依靠基于培养的方法来鉴定微生物和确定微生物的表型特征(图2)。基于培养的诊断,提供了一种表型抗菌药敏感性谱,允许根据生物体、药物药代动力学/药效学(PK/PD)和宿主因素有针对性地开出成功的抗菌药处方。传统基于培养的方法与等待时间慢、敏感性有限,并且在不同实验室之间存在差异。这意味着,通常在采集样本后48-72h才能获得微生物类别和抗菌药敏感性报告。这导致了靶向和个体化治疗的延迟,并提供了不适当的治疗窗口,无论是错误的治疗范围还是不必要的广谱治疗。
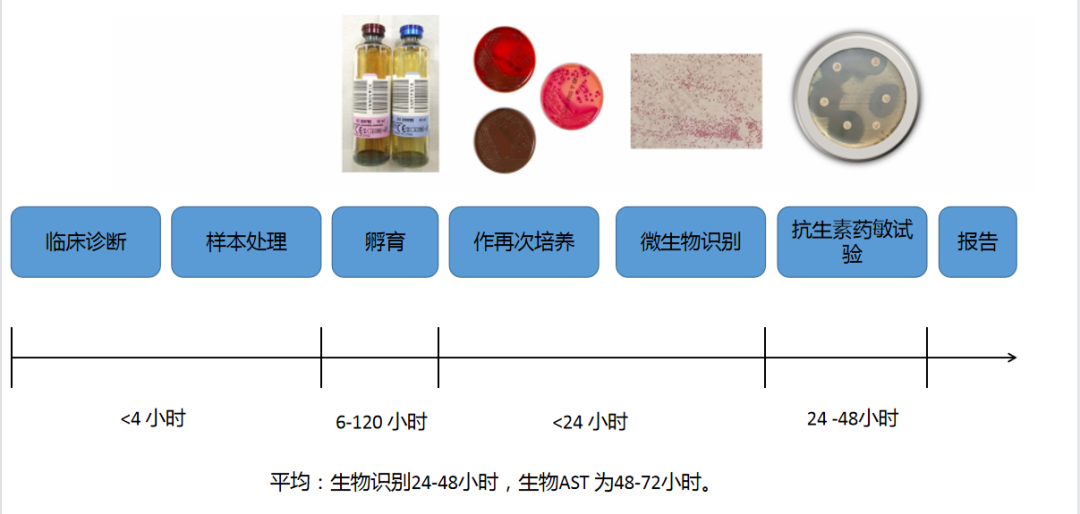
图2 血液培养传统诊断方法
最近的技术发展旨在缩短生物识别和敏感性报告的周转时间。这包括改进微生物实验室样品的收集和输送, 开发快速抗菌药敏 (AST)方法, 以及采用新技术进行微生物鉴定和 AMR检测。
基质辅助激光解吸电离飞行时间质谱(MALDI-TOF MS) 是一种技术示例,可促进快速鉴定生物体,并在某些情况下检测抗菌药物耐药性,例如区分甲氧西林敏感与耐甲氧西林金黄色葡萄球菌。使用MALDI-TOF MS,通过样品直接识别方案,可以进一步缩短等待时间,该方案已证明具有合理水平的敏感性和特异性,可以更快地进行生物体识别,从而实现靶向抗菌治疗。
分子诊断工具的开发提供了一种额外的诊断方式,协助ICU感染管理的最佳抗菌决策。分子诊断旨在绕过诊断途径中的培养步骤,直接从临床标本中快速检测和识别生物体。分子诊断还可以提供一种检测已知基因型抗菌药物耐药性的机制。ICU即时检测将分子样本部署到答案平台,将生物体识别和靶向抗菌治疗的时间缩短至24小时。迄今为止,支持分子诊断应用的临床试验数据还很缺乏。这些临床试验往往无法根据所做诊断对决策的影响,来合理定义结局的衡量标准。其中一个例子是一项多中心随机对照试验,该试验将与降钙素原相关的呼吸多重PCR平台用于诊断ICU住院COVID-19患者的细菌感染。该试验未能证明抗生素处方的影响,但确实证明了这种基于非培养的方法在经验性抗生素使用率高的人群中,微生物鉴定的敏感性有所提高。这项研究中,在微生物采样前接受经验性抗菌治疗的大多数患者(83%),多重PCR细菌鉴定结果提升2倍。
阳性血培养可以使用标准的实验室方法或自动化系统进行快速AST。在当前随机对照试验中,这些工具显示了更好的抗菌素管理目标(既减少了有效治疗时间,也减少了不适当的治疗),但未能证明改善包括死亡率在内的临床结局。例如,一项研究随机选择了革兰氏阴性菌血症患者的阳性血培养,以自动商业方法进行常规与快速AST检测,主要终点为缩短有效治疗时间。快速AST不会影响这一时间,但确实明显缩短了转换至口服抗菌药物时间,并将住院时间缩短了两天。
ICU细菌和真菌感染的管理
作为系列干预措施的一部分,早期开始合理抗菌治疗是改善ICU继发性细菌或真菌感染患者临床结局的最有效手段之一。表3总结了ICU常见感染综合征的流行情况,并强调了现有国际治疗指南的例子。
表3 重症监护患者常见感染综合征的患病率、常见致病微生物和治疗建议
感染综合征
ICU感染综合征比例
常见病原体
特殊注意事项
治疗建议
呼吸机/医院获得性肺炎
60%
GN:肠杆菌、铜绿假单胞菌、不动杆菌、嗜麦芽窄食单胞菌
GP:金黄色葡萄球菌、链球菌
真菌:曲霉属,其他霉菌
GN:产超广谱β -内酰胺酶细菌、产头孢菌素酶细菌、产碳青霉烯酶细菌
GP: MRSA、VRE、产生毒素细菌
ERS/ESICM/ESCMID/ALAT
IDSA/ATS
中国指南
南非胸科学会
腹内感染
18%
GN:肠杆菌属
GP:米氏链球菌、肠球菌。
真菌:假丝酵母菌
源头控制
GN:产超广谱β -内酰胺酶细菌、产头孢菌素酶细菌、产碳青霉烯酶细菌
GP: MRSA、VRE、产生毒素细菌
WSES/GAIS/SOS-E/WSIS/ AAST
IDSA
外科感染学会
血流感染
15%
GP:金黄色葡萄球菌、链球菌、肠球菌。
NG:肠杆菌、铜绿假单胞菌、不动杆菌。
真菌:假丝酵母菌、隐球菌属、其他不常见的酵母菌、镰刀菌属
导管相关 (CLASBI)
静脉注射抗菌药物的持续时间
GN:产超广谱β -内酰胺酶细菌、产头孢菌素酶细菌、产碳青霉烯酶细菌
GP: MRSA、VRE、产生毒素细菌
IDSA
JAID/JSC guidelines
泌尿
生殖系11%
肾脏3%
GN:肠杆菌属
真菌:念珠菌。
源头控制
导管相关
GN:产超广谱β -内酰胺酶细菌、产头孢菌素酶细菌、产碳青霉烯酶细菌
CDC
NICE
皮肤软组织
6%
GP:金黄色葡萄球菌、链球菌。
GN:肠杆菌属
真菌:毛霉菌
GP: MRSA、VRE、产生毒素细菌
WSES/SIS-E
IDSA
缩写:GN,革兰氏阴性;GP,革兰氏阳性;Spp,物种;MRSA,耐甲氧西林金黄色葡萄球菌;ESBL:超广谱β -内酰胺酶;VRE,耐万古霉素肠球菌。
ICU管理感染时,重要的是要考虑可能影响治疗结果的宿主、抗菌素和生物体因素。假定感染部位可能需要具体考虑(表3),例如去除菌株或控制来源,并且生物体性质及其表型在抗菌剂的选择和治疗持续时间中起着重要作用。危重患者通常会有高度可变的药代动力学(PK),这使得剂量优化具有挑战性。环境因素往往意味着存在耐药/抗药性水平较高的微生物,使得选择和优化抗菌药物治疗变得困难。了解当地流行病学知识,对于确保做出最佳的经验性治疗决策和优化抗菌药效学(PD)非常重要。将抗菌药物决策与ICU感染的整体管理联系起来至关重要,包括液体复苏、血流动力学管理、机械通气和考虑其他治疗干预措施,包括血糖控制、皮质类固醇和限制性输血策略。
经验性抗菌治疗
经验性抗菌药选择旨在涵盖感染常见致病微生物,同时等待最终结果,以提供针对性治疗。经验性治疗的目的应该是为常见的致病微生物和流行的耐药表型提供适当的抗菌谱。对于可疑的感染部位和严重程度,应选择具有适当PK/PD特性的试剂。
ICU面临的一大挑战是更普遍的耐药感染,以及选择不适当的经验性治疗方案往往可能造成严重后果。这意味着往往需要具有抗假单胞菌谱的广谱抗菌药。在耐甲氧西林金黄色葡萄球菌的高流行地区,糖肽类药物通常是经验性联合用药。对于可疑真菌感染,疑似念珠菌血症建议使用棘白菌素开始治疗,两性霉素-B通常用于侵袭性霉菌感染。感染诊断通常需要考虑图1中的许多因素。根据综合征诊断(例如呼吸道、尿路、皮肤-软组织感染),制定指南时考虑到常见致病微生物和局部耐药模式。表3总结了常见致病微生物、特殊考虑因素和国家/国际指南,这些在ICU常见的综合征诊断中经常需要考虑。
作为经验性治疗的一部分,除了确保提供合理治疗范围外,还必须考虑优化给药。危重疾病是PK/PD变化的主要原因,特别是在脓毒症,这种变化与死亡风险增加有关。为了解决观察到的抗菌剂PK/PD变化,经常建议延长或持续输注β-内酰胺和糖肽抗生素,以确保达到最佳的靶向治疗目标。
靶向/个体化抗菌治疗
在感染性休克中,确诊后1h内抗菌药物治疗对于降低死亡率非常重要。在没有休克的患者中,目前指南支持在识别后3h内开始治疗。细菌或真菌感染的危重患者,基于培养的诊断结果出来前推迟经验性治疗不可行,即时分子诊断平台的发展可能提供更丰富的信息,以便更快地提供靶向治疗。例如Banerjee等人证明,当与血培养阳性患者的抗菌素管理支持联系起来时,多重分子诊断促进了快速生物体识别、靶向治疗和更快的降级治疗。
一旦基于培养的诊断提供了适当的微生物和敏感性结果,从广谱经验性治疗转向靶向治疗,可以减少患者潜在的不良事件并减少AMR的传播。尽管缺乏支持脓毒症早期抗菌药治疗安全性的随机对照试验数据,但已经观察到的数据证明早期抗菌素治疗是安全的,并且不影响死亡率。此外,一项对美国医院收治的17,000多名脓毒症患者进行的大型回顾分析发现,在这一队列中,不必要的广泛抗菌治疗增加了死亡风险。
治疗药物监测(TDM)确保危重患者最佳药物暴露的作用,现已得到承认。针对危重病患者的抗菌药TDM指导正在从β-内酰胺类抗生素以及治疗窗口狭窄的药物(如万古霉素和利奈唑胺等)中产生。抗细菌和抗真菌TDM对患者预后的总体影响仍有待确定,但这可能是确保在药代动力学高度可变的患者中实现最佳PK/PD目标的一个重要考虑因素。
源头控制和其他非抗菌因素的重要性
除了最佳的抗菌药选择,感染管理还必须尽可能确保充分的源头控制。源头控制目标是消除任何持续感染源,防止持续污染,尽可能恢复发病前的功能和解剖结构。源头控制可分为三大类:除了最佳抗菌药物选择外,感染管理还必须尽可能确保充分的源头控制。源头控制的目标是消除任何持续性感染源,防止持续污染,并尽可能恢复到既往的功能和解剖结构。源头控制可分为三大类:排出积液或脓肿、清创或移除受感染的装置,以及明确的控制措施。目前指南建议在安全的情况下及时进行源头控制,以确保个体患者获得最佳结果。
在ICU内,源头控制通常侧重于减少或消除不再需要的侵入性干预。虽然常规更换中心静脉导管不能降低感染风险,也不建议这样做,但应定期检查此类装置,不再需要时将其移除,或者如果怀疑存在导管相关感染予以更换。如果怀疑有感染,应将导管放置在新位置,并避免重新放置旧导管。每日维持镇静和自主呼吸试验认为是减少机械通气需求的一种手段,尽管这种方法并没有被一致地发现可以减少机械通气的持续时间。
ICU的感染预防
ICU继发性细菌和真菌感染,很大比例是可以预防的。表4总结了主要的感染预防措施,这些措施可以普遍应用于ICU内不同的综合征环境。
表4 重症监护病房常见感染防控方法总结
部位
措施
证据
参考文献
一般感染防控措施
手卫生
●改善对手卫生的依从性与医疗保健相关感染的直接减少有关。
●手卫生最佳策略尚无明确证据。
●依从性往往随着时间推移而下降。
(82、83)
环境卫生
●环境清洁措施可减少定植或医院相关感染。
●如果不采取清洁措施,患者感染病原体的可能性增加150-500%。
[130]
通风设备
●床边通风要求应与患者的免疫状态相适应,并足以降低患者可能携带的任何病原体经空气传播的风险。
[131]
筛选和隔离
●在有证据表明定植增加感染风险的地方,如MRSA,用抑制治疗或隔离筛查可能是有益的。
●在疫情暴发时可采用筛查和隔离措施,以阻断感染链。
[132]
选择性消化道杀菌
●减少机械通气患者的菌血症和VAP发生率。
●治疗期间无耐药迹象。
●关于长期SDD的生态影响及其在MDRO感染率高的地区的有效性的高质量证据有限。
[89]
监测
●与国家监测系统相连的医院监测与 HCAI 总体减少有关。
[81]
抗菌药物管理
● 抗菌药物管理干预可以显着减少耐药感染的选择和传播。
● 遵守抗菌药物管理政策可以减少 HCAI、耐药性感染和艰难梭菌感染等并发症。
[68]
患者安全指南/集束化管理
● 集束化管理包含 3-5 种循证实践,必须集体一致地提供这些实践,以改善患者某个方面的结局。
● 针对特定 IPC 挑战管理组合优于所包含的个人干预措施的总和
呼吸机/医院获得性感染
●使用集束化的方法(如“100K生命运动”)已显示出VAP发生率显著降低。
●集束化核心内容包括抬高床头(30-45°),每日镇静和拔管评估,声门下分泌物引流,避免频繁的通气回路改变。通常附加的干预措施包括手卫生、氯己定口腔护理、教育和培训、袖带压力控制、肠内喂养以及在可能的情况下避免应激性溃疡预防。
[94,95]
中心静脉相关的血流感染
●使用集束化方法(如“Matching Michigan”),包括标准化的技术和非技术干预措施,可显著降低CLASBI。
●集束化方法采用技术标准化,包括手卫生、PPE使用、皮肤准备/无菌、最大限度的无菌预防措施、最佳插入部位选择和日常中心静脉导管(CVC)维护/管道护理。非技术方面包括最低水平的培训、审核和反馈以及沟通技巧。
[92、93]
手术部位感染
●围手术期集束化管理后观察到的SSI减少。当存在证据水平较高的干预措施时,这些措施往往更有效。
●集束化包括术前准备(如鼻腔清洁和脱毛)、术中准备(如手卫生、无菌纱布、备皮、抗菌预防)和术后干预(如敷料、清洁和专业伤口护理服务的支持)。
[134,135]
导尿管相关性尿路感染
●减少不必要置入和延长导尿时间的干预措施可以显著降低CAUTI发生率。
●集束化干预措施侧重于选择需要导尿、无菌插入和插入后常规维护的合适患者。
●带有审核和反馈的监督和报告在支持遵守最佳实践方面发挥重要作用。
[126,136,137]
缩写:MRSA,耐甲氧西林金黄色葡萄球菌;SDD,选择性消化道杀菌;MDRO,耐多药微生物;VAP,呼吸机相关肺炎;HCAI,医疗保健相关感染;CLASBI,中心静脉相关血流感染;SSI,手术部位感染;CAUTI,导尿管相关性尿路感染。
ICU感染预防依赖于多模式方法,包括手卫生、环境卫生、筛查和隔离方法、监测、抗菌药物管理以及特定患者安全指南和集束化的实施。手卫生可能是最重要的感染预防措施。强有力证据表明,手卫生依从率与医院感染发生率之间存在联系。手卫生目的是减少医护人员在工作期间感染的短暂微生物。这些暂时性微生物很容易在与患者接触时传播,因此是院内病原体传播的主要途径。使用酒精类洗手液以及肥皂和水清洗是手卫生的主要手段。在COVID-19大流行期间,全球范围内观察到医院机构手卫生措施失效的影响,由于调整了保护医护人员的个人防护装备(PPE)政策,接触患者之间洗手和手套更换措施不利,导致纹状棒状杆菌等生物爆发。
选择基于传播的预防措施来减少耐药细菌(例如MRSA和GRE)传播常常存在争议。随机对照试验数据未能证明,在定植患者中实施屏障预防措施可显着减少传播。坚持手卫生可能对减少耐药微生物(例如GRE)的传播总体影响最大。对于在环境中持久存在的细菌,例如艰难梭菌孢子,手卫生、环境控制和适当屏障预防措施可以减少传播给其他患者的风险。
监测是一项持续挑战,可在地方、区域和国家各级开展。英国感染上报政策(如MRSA血流感染和中央静脉相关血流感染是强制性的),可以帮助推动安全和问责机制。筛选和报告抗菌素耐药性有助于确定疫情,并为制定当地抗菌素政策提供信息。
选择性消化道内杀菌(SDD)已建议用于降低有创机械通气患者发生呼吸机相关肺炎的风险。SDD将局部不可吸收的抗生素和抗真菌药物应用于上消化道,并结合短疗程静脉注射抗生素。最近一项SDD的大型随机试验显示,尽管没有降低死亡率,但菌血症发生率(5.6% vs 8.1%)和耐药感染数量(23.1% vs 34.6%)有所降低。随后对SDD研究进行的荟萃分析表明,可以降低死亡率、VAP和ICU获得性细菌感染。耐药感染率相对较低地区的观察数据表明,SDD虽然不会促进抗生素耐药性的发展,但关于在生态水平上意外影响的高质量数据仍有待研究。
在医院内部,包括重症监护室,IPC政策旨在实施多模式干预措施,促进对患者的安全、有效和高质量护理。除了一般的IPC措施外,人们还认识到,集束化护理措施可以降低一系列医院感染风险(表4)。集束化护理是一系列干预措施的集合,这些干预措施的综合实施比其中单个干预措施总和产生更大影响。用于预防中央静脉相关血流感染的“匹配密歇根”运动和用于呼吸机相关肺炎的“100,000生命运动”是集束化干预措施的例子,在实施后显著降低了感染率。拯救脓毒症运动是集束化干预的一个例子,证明可以降低脓毒症患者的死亡率。
结论
ICU细菌和真菌感染,是所有参与危重患者护理人员必须考虑的重要事件。通过实施和遵守多模式感染预防控制政策,很大一部分感染是可以预防的。感染诊断可能很复杂,并且随着更多信息的出现和时间的推移而演变。分子诊断和快速测定AST方法的出现,使我们能够更快地获得有关生物体特征的信息。这必须应用于更广泛的决策环境,以确保这些新技术为患者带来显著益处。


