导管相关性血流感染的诊治
时间:2023-04-02 17:10:48 热度:37.1℃ 作者:网络
导管相关血流感染:是指带有血管内导管或者拔除血管内导管48小时内的患者出现菌血症或真菌血症,并伴有发热(>38℃)、寒颤或低血压等感染表现,除血管导管外没有其他明确的感染源。(血管内导管、血流感染的临床表现、排除诊断)
周围静脉导管、中心静脉导管(CVC) 、经外周中心静脉导管(peripherally inserted central catheter,PICC)、动脉导管、血透管等 。大多数严重的导管相关血流感染(catheter-related bloodstream infection, CR-BSI)与中心静脉导管(CVC)有关
-
出口部位感染(exit-site infection)指出口部位2cm内的红斑、硬结和(或)触痛;或导管出口部位的渗出物培养出微生物,可伴有其他感染征象和症状,伴或不伴有血行感染。
-
隧道感染(tunnel infection) 指导管出口部位,沿导管隧道的触痛、红斑和(或)>2 cm的硬结,伴或不伴有血行感染。
-
皮下囊感染(pocket infection)指完全植入血管内装置皮下囊内有感染性积液;常有表面皮肤组织触痛、红斑和(或)硬结;自发的破裂或引流,或表面皮肤的坏死。可伴或不伴有血行感染。
-
导管相关血流感染(catheter related bloodstream infection,CRBSI)
发病机制
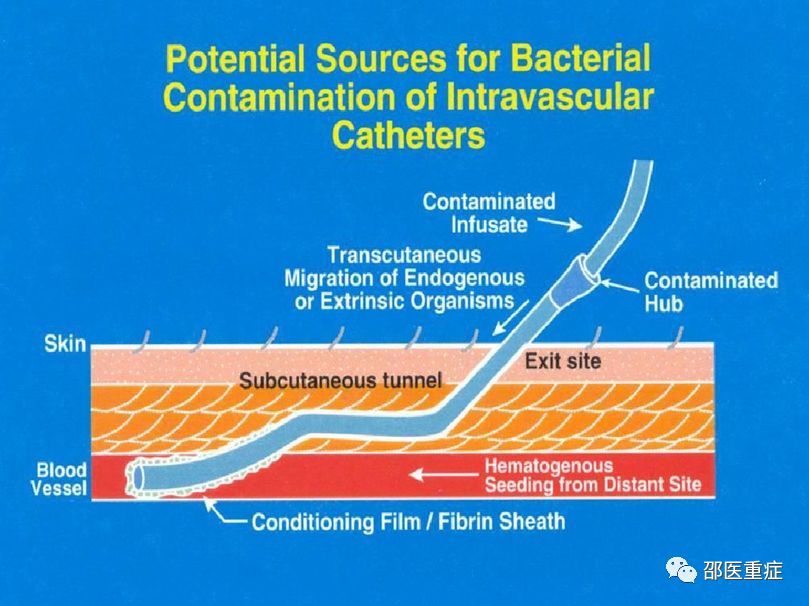
感染方式:
-
皮肤定植:皮肤表面的细菌在穿刺时或之后,通过皮下致导管皮内段至导管尖端的细菌定植,随后引起局部或全身感染;CVC相关感染的最常见来源是导管的皮内和血管内部分由患者皮肤的微生物定植,偶尔也来源于医务人员的手(插管过程或操作后)。
-
血源性播种:微生物从其他感染灶通过血行播散到导管,在导管上黏附定植,引起感染;血源性播种可能来源于另一个感染灶的血流感染期间,如胃肠道,这种情况最有可能发生在重症患者或长期导管患者。如果是原发病灶引起的反复血流感染,此时管尖和血流可能均有相同致病菌,此时很难区别原发病灶还是来自导管的血流感染。
-
直接污染:微生物污染导管接头和内腔,导致管腔内细菌繁殖,引起感染。输注液污染,如污染的血制品(库存血)、TPN、泵注液或肝素冲洗液等。
病原菌

诊断
血培养:当怀疑导管相关血行感染又不能拔除导管时,应同时取外周静脉与中心静脉导管血进行培养
-
与经皮采集血样的培养结果相比,经导管采集血样的培养结果假阳性率更高。因此,与培养经导管获得的血样相比,培养外周静脉血样的特异性和阳性预测值更高。
-
这两种类型的血样培养均有极好的阴性预测值。
-
在不能获得外周血样且无临床证据提示存在其他感染源的情况下,应假设经导管采集血样培养获得的阳性结果反映的是真正的感染。
实验室诊断-诊断标准
-
从导管的尖端和至少1次外周血样培养出相同的微生物。
-
从至少2份血样培养出相同的微生物(1份来自导管,另1份来自外周静脉),并且符合定量血培养或阳性差异时间(differential time to positivity, DTP)的标准。
DTP是指,从导管血样本检出的细菌生长比从外周静脉血样检出的细菌生长早至少2个小时。
定量标准:导管血样本茵落数>外周静脉血培养的茵落数的5倍及以上时
-
外周血和导管出口部位脓液培养均阳性,并为同一株微生物。
治疗
1.导管的处理
治疗静脉内导管相关全身性感染的第一步就需要临床医生决定如何处理导管,如补救、更换或移除。
-
对于周围静脉导管,当怀疑导管相关感染时,应立即拔除,并进行导管与外周血标本的培养
-
对于中心静脉导管,应当考虑临床相关因素后再做出是否拔除或更换导管的决定,这些因素主要包括导管的种类、感染的程度和性质、导管对于病人的意义、再次置管可能性及并发症以及更换导管和装置可能产生的额外费用等。
2.抗生素治疗
一般而言,在获得微生物培养和药敏试验结果之前,必须开始经验性抗生素治疗。后续治疗应根据微生物学检查结果按需进行调整
1)经验性治疗
根据疾病严重程度和病原微生物的流行病学,选用可能覆盖病原微生物的抗生素药物
-
葡萄球菌是导管相关感染最常见的病原菌,且存在高耐药性,糖肽类抗生素药物应作为导管相关感染经验性治疗的首选药物。
-
对于中性粒细胞减少或脓毒症患者而言,在疑似CRBSI的情况下,应对革兰阴性杆菌(包括假单胞菌属)进行经验性抗生素治疗是适当的。对于已知定植有耐药性微生物的患者,应予以相应挑选经验性抗生素治疗。
-
对于使用TPN、长期使用广谱抗生素、血液系统恶性肿瘤、骨髓移植或实体器官移植、股动/静脉插管、假丝酵母菌(Candida)定植于多个部位的患者可针对念珠菌进行经验性治疗,治疗首选棘白菌素类药物。
2)调整治疗(目标治疗)
凝固酶阴性葡萄球菌(如表皮葡萄球菌、腐生葡萄球菌)
-
致病力相对偏低,在移除导管后未给予抗生素治疗的情况下,这种感染也可能会消退。但多数专家建议抗生素治疗5-7d。
-
在移除导管后发热和/或菌血症仍持续存在,需要治疗
-
对于安置有血管内装置的患者,应移除导管,并需要进行更长期的治疗。如果排除了感染性心内膜炎,则需为期3周的治疗。
-
如果长期置管且全身情况相对稳定,也可进行导管补救,那么需要进行10-14日的抗生素治疗(全身性抗生素治疗+ALT)
金黄色葡萄球菌
-
一般而言,对于金黄色葡萄球菌引起的CRBSI,需要移除导管和全身性抗生素治疗,抗生素治疗至少2周。
-
移除导管后,如果72小时时再进行的血培养未发现微生物生长,则可以置入新的导管。
-
25%-30%的病例会出现金黄色葡萄球菌性菌血症的血源性并发症(例如,感染性心内膜炎IE)。开始恰当的抗生素治疗和移除导管后72小时,血培养结果为阳性是预测血源性并发症的有用指标。
-
建议在菌血症发病后5-7日进行TEE检查以排除IE。
-
如果患者发生了血源性并发症,应接受4-6周的抗生素治疗。
肠球菌、革兰阴性杆菌、假丝酵母菌
-
一般而言,治疗包括移除导管(如果可行)和全身性抗生素治疗
抗生素疗程
-
CRBSI的抗生素治疗持续时间取决于临床情况。一般而言,对于无并发症的CRBSI患者,如果移除导管或经导丝更换导管并开始适当抗生素治疗后血培养的结果呈阴性,则治疗的持续时间通常为10-14日(从获取阴性血培养结果第1日开始计算)。
-
对于移除导管后菌血症仍持续超过72小时的患者,需警惕发生了菌血症相关并发症 (如化脓性血栓性静脉炎、心内膜炎、骨髓炎、转移性感染),治疗一般需持续至少4-6周,具体应根据感染的性质相应调整。
小结
-
随着重症医学对导管技术的需求越来越高,导管相关性感染需要临床越来越重视。
-
导管相关血流感染是导管导致的血流感染,尽管各种血管内导管均可发生,但CVC最常见。
-
导管相关性血流感染的诊断方法包括临床评估和病原学证据,并且这种病原体与其他部位的感染无关。
-
导管相关性血流感染的治疗,包括对导管的处理(例如,补救、更换或移除),以及抗生素治疗(例如,先经验性给药,随后根据微生物培养和药敏试验结果加以调整)。
-
洗手、皮肤消毒、无菌原则、规范操作及护理是预防导管相关性感染的重要措施。


