AMERICAN JOURNAL OF TRANSPLANTATION:造血干细胞移植后儿科肝移植接受者实现了操作耐受性
时间:2023-09-13 23:07:05 热度:37.1℃ 作者:网络
器官移植耐受性代表了移植免疫学家的圣杯。在过去的几十年里,一些研究人员一直在探索通过移植造血干细胞(HSC)来诱导固体同种异体移植的耐受性,要么作为实现容性嵌合的策略,要么作为免疫再教育的平台。
2023年4月13日发表在AMERICAN JOURNAL OF TRANSPLANTATION的研究中,我们报告了一名患者在治疗肝炎相关再生障碍性贫血的不同捐赠者接受肝移植(LT)并随后获得操作耐受(ALT)的患者。

一名10岁的男孩在已故捐赠者LT约1个月后被诊断出患有严重的肝炎相关再生障碍性贫血。LT和移植后免疫抑制(IS)的详细信息在补充材料中报告。诊断后,患者接受马抗胸腺细胞球蛋白和强的松治疗,同时继续每天服用他克莫司。由于缺乏回应,决定继续进行alli-HSCT。在没有任何人类白细胞抗原(HLA)匹配的兄弟姐妹的情况下,确定了9/10高分辨率HLA匹配,ABO血型兼容的男性捐赠者。
关于HSCs供体和移植肝脏之间的兼容性,记录了HLA-DPB1位点的单个等位基因匹配和HLA-C和HLA-DQB1位点的单个抗原匹配。所有其他相关的HLA位点(HLA-A、-B、-DR和-DQA)完全不匹配。大约在LT后6个月开始的调理方案,包括氟达拉滨和环磷酰胺。兔子抗T细胞球蛋白和单剂量利妥昔单抗分别用于预防双向肾功能活性和移植后淋巴增生性疾病。
移植物抗宿主病(GvHD)预防包括静脉注射他克莫司和短期甲氨蝶呤。中性粒细胞和血小板恢复分别发生在+23和+33天。在巨细胞病毒重新激活期间,观察到肝酶暂时升高。出院后,患者继续接受口服他克莫司,以预防GvHD和肝脏移植排斥反应。然而,由于次优耐受性和患者对口服的遵从性差,血清他克莫司水平(5-10纳克/毫升)几乎没有维持。
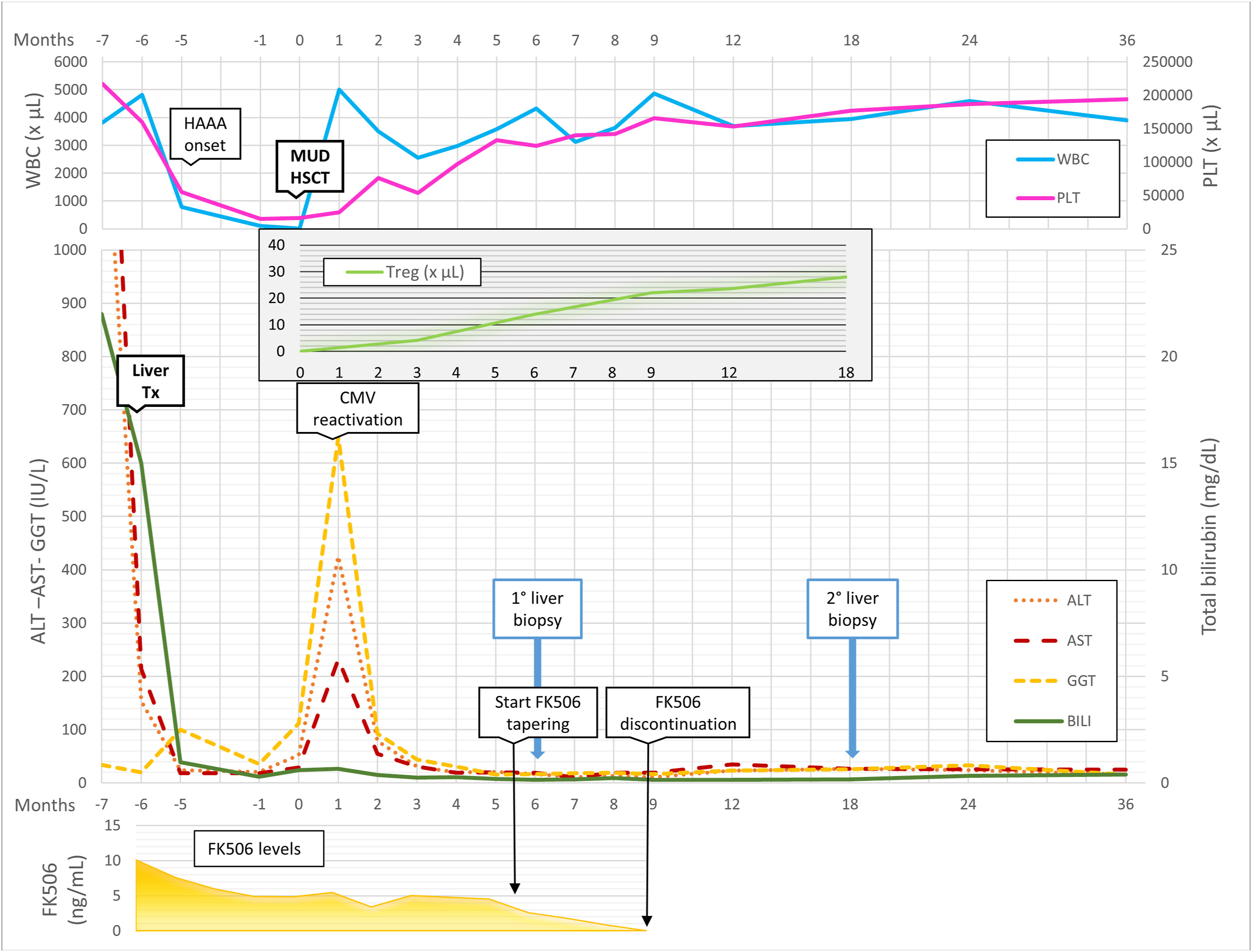
图1:患者从ALF开始到最后一次随访的临床过程
患者患上了I级急性GvHD,完全涉及皮肤,成功接受了外用类固醇治疗。值得注意的是,患者在肝功能测试中从未表现出任何重大改变,HSCT后6个月进行的肝脏活检显示完全没有表明移植物排斥的组织病理学结果。鉴于这些观察,在与家人讨论后,我们决定慢慢逐渐减少IS,直到完全停药,这是在HSCT后9个月实现的。免疫重建监测显示,在tacrolimus逐渐减少期间,调节性T细胞(Tregs)的绝对数逐渐增加。
对肝供体抗原的供体特异性抗体的监测检测总是呈阴性。HSCT前后T细胞受体(TCR)β链的后期DNA测序表明,通过调理方案大量克隆缺失,以及从de novo T细胞淋巴细胞中出现全新的克隆。在最后一次随访之前,外周血细胞上一直记录着完整的供体嵌合体。HSCT后18个月进行的后续肝活检证实了正常的移植组织学。患者目前在 allo-HSCT 30 个月后还活着,没有疾病,没有 IS,没有肝功能障碍或慢性 GvHD 的迹象。

图2:(A)患者临床过程的示意图;(B)跟踪的TCRβ生产重排随时间分布的变化;(C)Morisita重叠指数显示不同时间点在样本之间共享TCRβ DNA重排的程度;(D)不同时间点样本内顶部重排的分布;(E)根据与之前发布的CMV特异性TCR序列的对齐情况评估CMV相关TCRβ重排
本文的报告描述了第一个LT病例,随后是来自不同捐赠者的allo-HSCT,其中有可能在HSCT后成功终止任何IS并获得OT。在串联固体器官移植和allo-HSCT的背景下,HSCT后IS的管理和实现耐受性被认为严格取决于同种异体移植和HSC捐赠者之间的关系。如果固体器官和HSCs捐赠者不同,移植后IS的管理是一个挑战,因为一方面,它必须阻止发展严重的GvHD,另一方面,也避免了固体器官的排斥。
在我们的案例中,固体器官在allo-HSCT后可能特别暴露在免疫介导的攻击中,因为与其他受体组织相比,HLA与再填充的供体源性T细胞的不匹配程度更高。在之前的一份报告中,在之前接受过不同捐赠者LT的男孩的allo-HSCT后,环孢素A逐渐变细,随后进行了活检记录的排斥反应。
综上所述,我们的报告表明,通过完全重新配置适应性免疫系统, allo-HSCT能够诱导对从免疫学上不同的供体收集的先前LT的耐受性,从而终止IS。鉴于我们发现的初步性质,在HSCT后期间,任何退出IS的尝试都应谨慎对待,并始终密切监测肝功能测试和组织学。
原文出处
Algeri M, Velardi E, Spada M, Galaverna F, Carta R, Vinti L, Palumbo G, Gaspari S, Pietrobattista A, Boccieri E, Becilli M, Francalanci P, Bertaina V, Merli P, Locatelli F. Achievement of operational tolerance in a pediatric liver transplant recipient following successful hematopoietic stem cell transplantation from a different donor. Am J Transplant. 2023 Sep;23(9):1446-1450. doi: 10.1016/j.ajt.2023.04.003. Epub 2023 Apr 13.


