JTO:同济大学周彩存团队发现晚期/转移性未经免疫治疗非小细胞肺癌的潜在治疗新策略
时间:2023-11-01 11:37:55 热度:37.1℃ 作者:网络
大约85%的肺癌病例是非小细胞肺癌(NSCLC),并且它仍然是2022年全球癌症相关死亡的主要原因。据估计,61%的NSCLC患者在诊断时已处于晚期(III/IV期),这与预后不良相关,在化疗时代,不可切除的III期疾病的5年总生存率(OS)约为30%,IV期疾病约为5%。
2023年10月23日,同济大学周彩存团队在Journal of Thoracic Oncology在线发表题为“A phase Ib study of ivonescimab, a PD-1/VEGF bispecific antibody, as first- or second-line therapy for advanced or metastatic immunotherapy naïve non-small-cell lung cancer”的研究论文,该研究评估了Ivonescimab作为晚期/转移性未经免疫治疗的非小细胞肺癌(NSCLC)患者一线或二线单药治疗的安全性和有效性。74例(68.5%)患者程序性死亡配体-1 (PD-L1)肿瘤比例评分(TPS)≥1%,其中TPS≥50%的患者35例(32.4%)。中位随访时间为10.4个月(8.4 - 10.9个月)。所有患者ORR和疾病控制率(DCR)分别为39.8%和86.1%。TPS <1%、≥1%、≥50%患者TPS的ORR分别为14.7%、51.4%和57.1%。
在接受一线Ivonescimab治疗的67例PD-L1阳性患者中,10 mg/kg Q3W、20 mg /kg Q2W、20 mg /kg Q3W和30 mg/kg Q3W剂量组的ORR分别为33.3%、52.6%、60.0%和75.0%。24例(22.2%)患者观察到≥3级治疗相关不良事件(TRAEs)。1例(0.9%)患者发生TRAEs导致停药。3例(2.8%)有鳞状组织的患者发生TRAEs导致死亡。鳞状和非鳞状组织中≥3级TRAEs和≥3级出血事件的发生率分别为25.5%对18.9%和0.0%对1.9%。综上,Ivonescimab单药治疗耐受性良好,在晚期或转移性NSCLC患者中显示出良好的疗效。
另外,2023年10月21日,同济大学周彩存等团队合作在国际知名医学期刊NEW ENGLAND JOURNAL OF MEDICINE (IF=159)在线发表题为“First-Line Selpercatinib or Chemotherapy and Pembrolizumab in RET Fusion–Positive NSCLC”的研究论文,在一项随机3期试验中,该研究评估了一线selpercatinib与对照治疗的疗效和安全性,对照治疗由铂类化疗组成,研究者自行决定是否使用帕博利珠单抗。主要终点是无进展生存期。该研究发现,在晚期RET融合阳性NSCLC患者中,selpercatinib治疗比铂基化疗加或帕博利珠单抗治疗的无进展生存期明显更长。
2023年10月21日,同济大学周彩存等团队合作在国际知名医学期刊NEW ENGLAND JOURNAL OF MEDICINE(IF=159)在线发表题为“Amivantamab plus Chemotherapy in NSCLC with EGFR Exon 20 Insertions”的研究论文,在这项3期国际随机试验中,研究人员以1:1的比例分配了EGFR外显子20插入的晚期NSCLC患者(这些患者之前没有接受过全身治疗)接受静脉注射Amivantamab加化疗(Amivantamab-化疗)或单独化疗。主要终点为无进展生存期。该研究发现作为EGFR外显子20插入的晚期NSCLC患者的一线治疗,Amivantamab化疗的疗效优于单纯化疗(点击阅读)。

目前,使用免疫疗法已成为治疗无驱动基因改变的NSCLC患者不可或缺的一部分。PD-1/PD-L1的药物已被批准作为一线治疗药物,用于PD-L1肿瘤比例评分(TPS)≥50%或≥1%的晚期NSCLC患者。KEYNOTE-042是一项比较派姆单抗单药与化疗作为晚期NSCLC一线治疗的3期研究,在PD-L1 TPS≥1%的患者中,派姆单抗显示出优于化疗的OS获益,但在TPS 1-49%的患者中,探索性分析没有获益。近年来,对于PD-L1 TPS为1-49%且无驱动癌基因的晚期NSCLC患者,免疫治疗联合铂基化疗已成为标准治疗(SOC)。遗憾的是,许多患者不能忍受化疗的毒性,这限制了从标准治疗中受益的患者数量。因此,临床迫切需要新的无化疗方案,以增强抗癌功效和可接受的安全性。
在临床前研究中,抗VEGF和抗PD-1/PD-L1抗体显示出协同抗肿瘤活性。抗VEGF不仅可以抑制血管生成,还可以增加免疫效应细胞的运输和浸润到肿瘤微环境中,以及调节T调节细胞和髓源性抑制细胞,从而实现免疫应答环境,从而提高抗PD-1/PD-L1抑制剂的疗效。抗PD-1/PD-L1抗体联合抗血管生成药物治疗晚期实体瘤已显示出抗肿瘤活性和可耐受的安全性。在IMpower150 iii期研究中,贝伐单抗联合阿特唑单抗和化疗在一线环境中显示晚期非鳞状NSCLC患者的生存获益,中位无进展生存期(PFS)为8.3个月,中位总生存期为19.2个月。阿特唑单抗联合贝伐单抗对PD-L1高表达的非鳞状NSCLC患者有效,客观缓解率(ORR)为64.1%。此外,ramucirumab是一种抗VEGF受体(VEGFR) 单克隆抗体,在先前治疗的晚期NSCLC患者中,与pembrolizumab联合使用显示出良好的抗肿瘤活性。综上所述,抗VEGF /VEGFR抗体和抗PD-1/PD-L1抗体对无驱动癌基因改变的晚期NSCLC患者具有重要的临床意义。
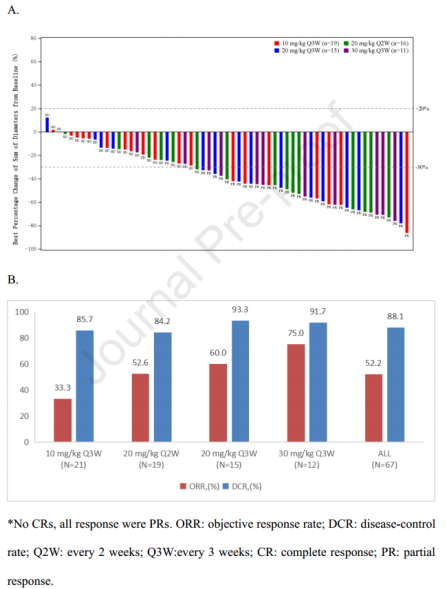
一线晚期/转移性非小细胞肺癌PD-L1阳性肿瘤患者的抗肿瘤活性(图源自Journal of Thoracic Oncology )
研究表明,局部晚期或转移性NSCLC患者的安全性,无论组织学或PD-L1状态如何。Ivonescimab还显示出剂量依赖性抗肿瘤活性,特别是在一线接受Ivonescimab剂量≥ 20mg/kg的PD-L1阳性患者中。这是首个报道使用PD-1和VEGF双特异性抗体治疗非小细胞肺癌而无需化疗的研究。
该研究发现,Ivonescimab单药治疗显示出可控的安全性。≥3级TRAEs仅出现在24例(22.2%)患者中。在四个剂量组中观察到类似的安全性概况,表明AEs在研究的剂量范围内不依赖于剂量。除了已知的与其他抗pd -1/PD-L1/VEGF抗体相关的AEs外,未发现新的安全信号。考虑到Q2W队列确实显示出数值上较高的不良事件发生率,考虑到与其他剂量相比,该剂量队列中的患者显示出相对更好的抗肿瘤活性和相对可耐受的安全性,因此选择20mg /kg Q3W剂量用于未来的3期研究。
Ivonescimab的分子结构和作用机制可以解释其耐受安全性。由于PD-1和VEGF在肿瘤微环境中共表达,Ivonescimab的双靶点设计将PD-1和VEGF结合在一起,使大分子药物在肿瘤微环境中富集和保留,从而减少其在外周血中的分布,降低脱靶效应引起的毒性。Ivonescimab的安全性可能更易于管理,作为双特异性抗体,而不是联合两种单一药物对抗PD-1和VEGF。总之,Ivonescimab单药治疗显示出可控的安全性和有希望的疗效,特别是对于患有PD-L1阳性疾病的晚期NSCLC患者的一线治疗。
原文链接:
https://www.jto.org/article/S1556-0864(23)02312-2/fulltext


