东华大学史向阳、沈明武ACS Nano:树枝状大分子共递送蛋白质和核苷酸用于磁共振成像引导的肿瘤化学动力学/饥饿/免疫治疗
时间:2023-12-01 15:33:54 热度:37.1℃ 作者:网络
尽管发展多年,但开发一种纳米级药物递送系统,而该系统可以同时发挥有效的肿瘤治疗效果并产生所需的抗肿瘤免疫反应,仍然具有挑战性。
近期,东华大学史向阳教授和沈明武研究员等人报道了使用包埋二氧化锰(MnO2)的树枝状大分子纳米载体(MGPP)来共递送葡萄糖氧化酶(GOx)和环状GMP-AMP(cGAMP),后者是干扰素基因刺激因子(STING)的激动剂,可用于改善肿瘤的化学动力学/饥饿/免疫治疗。MnO2核心尺寸为2.8nm的MGPP NP显示出有效的谷胱甘肽耗竭能力,并且在肿瘤微环境下具有良好的Mn2+释放特性,可实现Fenton样反应和T1加权磁共振(MR)成像。在双侧小鼠结肠直肠肿瘤模型中,枝状聚合物递送纳米系统具有强大的抗肿瘤性能和较强的远隔效应,大大提高了小鼠的整体存活率。更重要的是,枝状大分子介导的共递送不仅允许Mn2+与GOx和cGAMP配位,分别用于化学动力学/饥饿触发的免疫原性细胞死亡(ICD),增强STING激活以促进系统抗肿瘤免疫反应,而且还可实现T1加权肿瘤MR成像,有望成为抗肿瘤治疗的候选纳米平台。相关工作以“Manganese Dioxide-Entrapping Dendrimers Co-Deliver Protein and Nucleotide for Magnetic Resonance Imaging-Guided Chemodynamic/ Starvation/ Immune Therapy of Tumors”为题发表在ACS Nano。

【文章要点】
一、MGPP NP
为了制备MGPP NP,作者首先合成了甲氧基聚乙二醇(mPEG)和苯基硼酸(PBA)修饰的第5代(G5)聚氨基胺枝状大分子,然后用以包埋MnO2纳米颗粒以产生杂化物MnO2@G5-mPEG–PBA(MGPP)NP,并最终与GOx和cGAMP复合形成递药系统(图1)。研究表明,MGPP-介导的GOx递送促进了癌症细胞的化学动力学/饥饿治疗,并且cGAMP的进一步共递送可以有效地触发免疫原性细胞死亡,以强烈促进树突细胞的成熟。
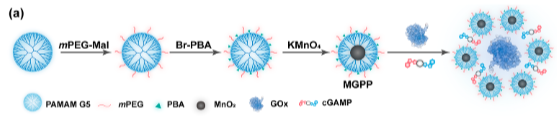
图1 材料制备
二、成像引导的化学动力学/饥饿/免疫治疗
在双侧小鼠肿瘤模型,随着Mn2+在TME中的释放和积累,原发性肿瘤中纳米系统的局部治疗能够协调化学动力学/饥饿触发的ROS生成,以促进癌症细胞ICD和损伤相关分子模式(DAMP)的释放,用于全身免疫激活。同时,释放的Mn2+与cGAMP联合强烈刺激附近淋巴组织中DC的cGAS STING,这导致一系列免疫反应,以增强系统免疫,用于远处肿瘤治疗和长期抗肿瘤保护。此外,肿瘤中Mn2+的积累也可以介导有效的T1加权MR成像(图2)。
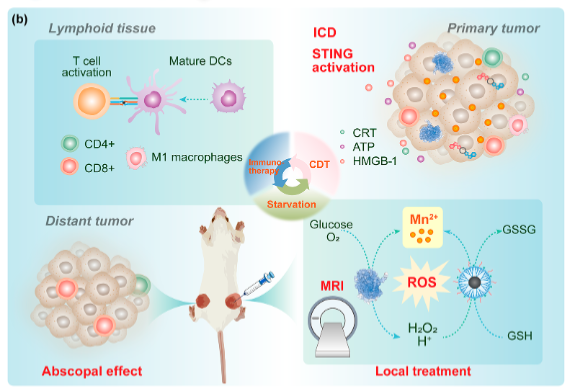
图2 抗肿瘤治疗示意图
原文链接:
https://pubs.acs.org/doi/10.1021/acsnano.3c08174


