II期临床试验显示,iNKT细胞治疗使肝癌患者治愈率提升5倍
时间:2024-01-12 20:59:45 热度:37.1℃ 作者:网络
亮点
1、和对照组(TAE组)相比,实验组(iNKT+TAE组)的不良事件发生率明显降低,说明iNKT细胞疗法的安全性优异。TAE-iNKT组患者生活质量发生恶化的中位时间是9.2个月,而TAE组的中位时间只有3.0个月,可见TAE联合iNKT在维持生活水平方面具有明显的优势。
2、实验组(iNKT+TAE组)有5位患者完全缓解(CR),而对照组(TAE组)仅有1位患者完全缓解(CR)。
3、实验组(iNKT+TAE组)的中位无进展生存期(mPFS)、中位总生存期(mOS),客观缓解率(ORR)和疾病控制率(DCR)分别为:5.7个月、25.9个月、52%和85%,明显优于对照组(2.7个月、17.3个月、11%和33%)
在肝癌治疗中,经动脉栓塞(TAE)或经动脉化疗栓塞(TACE)是不可切除肝癌常用的治疗手段。但有时,重复进行TACE治疗会使肿瘤出现耐药,并且反复进行TACE和TAE会损伤肝功能,从而导致患者治疗困难。

health.sina.cn
iNKT细胞是一种具有抗肿瘤免疫活性的淋巴细胞亚群。iNKT细胞通过直接细胞溶解和调节肿瘤微环境内的免疫抑制细胞发挥抗肿瘤作用。在TACE/TAE治疗后,肿瘤会形成局部炎症,iNKT细胞会被迅速募集到这些炎症部位,这有助于抗肿瘤治疗。
因此,研究人员进行了一项Ⅱ期临床研究,试图将两者结合起来,探究iNKT细胞输注和局部栓塞治疗联合对肝癌的疗效和安全性。

doi: 10.2147/JHC.S416933.
这项随机、多中心、开放标签的Ⅱ期临床试验共持续2年,受试者均为经TACE治疗失败,或诊断为难治性肝细胞癌的患者,分期为BCLC B/C。共54名患者被纳入本研究,并被随机均分为TAE组和TAE-iNKT组。
这54例患者均为中国人,中位年龄是64岁,其中男性占87%,女性占13%。TAE组患者仅接受单独TAE治疗;TAE-iNKT组患者每两周接受一次iNKT细胞输注,共6次,同时联用TAE治疗。
患者输注的iNKT细胞量约6~9×107个细胞/m2,纯度和活力均在95%以上。在iNKT细胞输注后,患者还接受了皮下注射白细胞介素-2,剂量为25000 IU/kg,每隔1天注射1次,持续2周。
在该试验结束时,患者中位随访时间为12.7个月,TAE-iNKT组和TAE组分别有82%和85%的患者出现疾病进展或死亡。这提示二者联用可能具有更优的治疗效果。
为了进一步分析治疗对患者生存的影响,研究人员延长了随访时间。他们发现TAE-iNKT组的中位总生存期(OS)是25.9个月,长于TAE组的17.3个月。
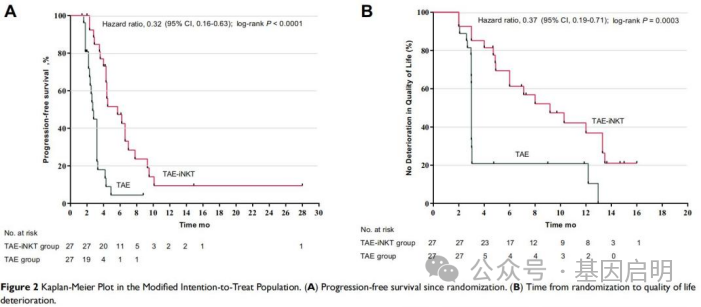
doi: 10.2147/JHC.S416933.
在无进展生存期(PFS)方面,TAE-iNKT组的中位PFS是5.7个月,明显优于TAE组的2.7个月,风险比为0.32,差异有显著的统计学意义。
值得一提的是,在复发性或难治性肝癌患者的疗效评价体系中,生活质量是与OS或PFS同样重要的临床结局,因为这些患者的生活质量已经因疾病本身和既往治疗而降低。对于这些患者,理想的治疗方法是延长生存期并保持或改善生活质量。
因此,研究人员对两组患者的生活质量也进行了比较,他们发现iNKT细胞治疗显著提高了患者的生活质量。总体来看,TAE-iNKT组患者生活质量发生恶化的中位时间是9.2个月,而TAE组的中位时间只有3.0个月,可见TAE联合iNKT在维持生活水平方面具有明显的优势。

m.thepaper.cn
身体功能方面,TAE-iNKT组的中位恶化时间是9.6个月,而TAE组仅为3.2个月,风险比是0.45。
另外,研究人员还评估了患者的社会角色功能。所谓角色功能,就是指个体在社会中扮演的角色或承担的职业,以及维持该角色和职业的能力。例如,教师如果因疾病无法正常履行教学任务,就判定为教师的角色功能发生了恶化。
研究人员发现,TAE-iNKT组的角色功能中位恶化时间也明显长于TAE组,分别为9.6个月和3.1个月,风险比为0.42。
客观缓解率(ORR)和疾病控制率(DCR)的分析同样说明TAE联合iNKT细胞治疗具有明显的优势。具体来说,TAE-iNKT组的ORR达到了52%,但TAE组仅为11%;DCR在这两组中分别为85%和33%。
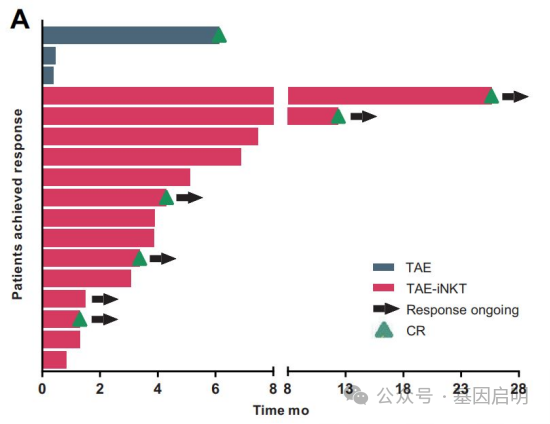
doi: 10.2147/JHC.S416933.
值得一提的是,TAE-iNKT组中有19%的患者达到了完全缓解,33%的患者达到了部分缓解。但在TAE组中,完全缓解只占4%,部分缓解占7%。
另外,TAE-iNKT组中33%的患者被鉴定为疾病稳定,但TAE组仅有22%。与之相反的是,TAE-iNKT组的疾病进展报告比例显著低于TAE组,分别为15%和67%。
淋巴细胞数量的增加往往是抗肿瘤免疫激活的标志,而以前的研究也发现iNKT细胞治疗能够较好地激活免疫系统。因此,研究人员进一步检测了两组患者的血液细胞组成。他们发现,TAE-iNKT组的确拥有更高的淋巴细胞数量,差异在第8周和第12周时最为显著。升高的淋巴细胞计数可能正是TAE联合iNKT细胞输注疗效增强的原因之一。
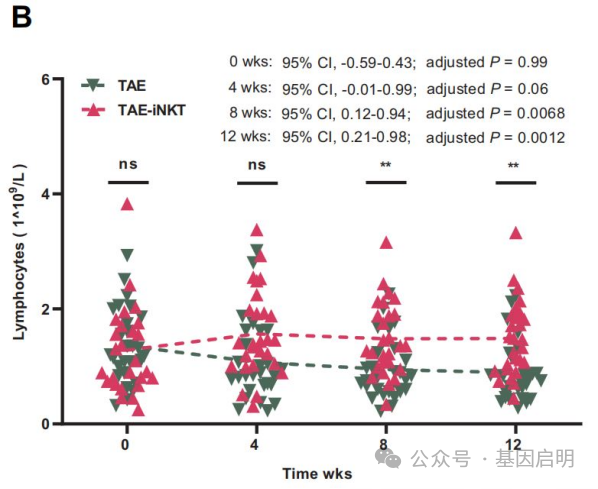
doi: 10.2147/JHC.S416933.
在安全性方面,所有受试者均出现了不同程度的不良反应。但是,疲劳、发热、谷丙转氨酶升高、血胆红素升高等不良反应率在TAE-iNKT组中较TAE组明显减少。TAE组胆红素和转氨酶水平升高的发生率是70.4%,TAE-iNKT组则为29.6%。
TAE-iNKT组和TAE组的3级不良事件发生率分别为4%和19%,这说明TAE和iNKT细胞的联合治疗具有较好的安全性和可控的毒副作用。在TAE-iNKT组中,研究人员发现转氨酶升高在未进行治疗或治疗中断的情况下可自行恢复正常,这进一步说明不良反应程度可控。值得一提的是,这项试验未观察到4 ~5级不良反应事件。
结合以上结论,该研究表明与单独TAE相比,iNKT细胞输注加TAE可改善患者的生存期,有利于控制疾病进展,提高患者的生活质量,且毒性作用相对较低。
作为首项探索TAE和iNKT细胞输注联合治疗肝癌的临床试验,本研究为肝癌患者提供了一种新的治疗选择。这种联合治疗的优势在于,既可以充分利用iNKT细胞的抗肿瘤免疫功能,又同时避免化疗药物的毒性损伤,具有很大的临床应用潜力。
来源:
微信公众号:基因启明
参考文献
Guo J, et al. Efficacy of Invariant Natural Killer T Cell Infusion Plus Transarterial Embolization vs Transarterial Embolization Alone for Hepatocellular Carcinoma Patients: A Phase 2 Randomized Clinical Trial. J Hepatocell Carcinoma. 2023, 10:1379-1388. doi: 10.2147/JHC.S416933.


