挑战重重!一例依从性差的转移性直肠癌病例分享
时间:2024-07-08 15:00:34 热度:37.1℃ 作者:网络
01病例介绍
患者:胡某,男,55岁
就诊时间:2018-8-18来诊。
主诉:排便困难20余天,大便带血5天
查体:指检:进指约7cm,可扪及一肿物呈菜花样生长,约占据整个管腔一周,质地中等,前壁稍固定,上缘未触及,退指套染血。
既往史:
既往有高血压病史4年,最高收缩压达190mmHg,规律服用氯沙坦钾氢氯噻嗪片。
入院评估
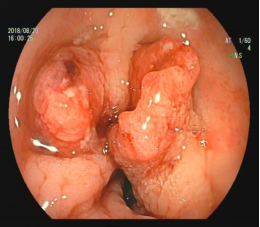
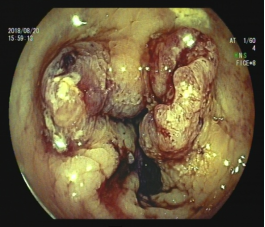
2018.8.20肠镜示:直肠距肛缘3-8cm见环周新生物,表面不平,部分溃烂,上覆坏死组织及污秽物,质脆。
超声肠镜:直肠Ca(T3N0)
病理活检:直肠腺癌
MRI:
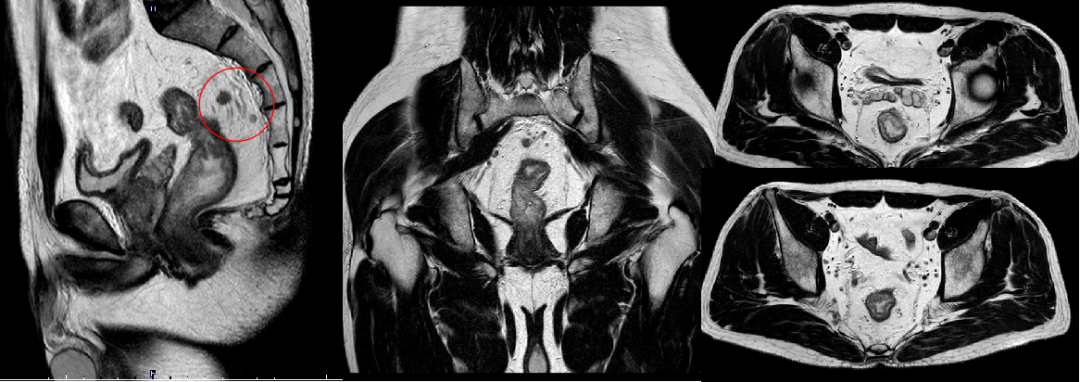
1、直肠中上段占位,性质待定:新生物?直肠癌?T3bN1M0?请结合临床进一步检查。
2、直肠筋膜系膜区多个小淋巴结显示,有强化。
初治诊断及分期:
1.直肠腺癌(cT3N1M0,III期)2.肠梗阻
第一次院内MDT
(2018-8)
初始治疗目标(2018-8):
1.解除梗阻,提高生活质量(支架、造瘘、介入等)
2.抗肿瘤治疗(新辅助化疗、放化疗等)
3.延长患者OS
第一阶段治疗方案
2018-8-27:横结肠双腔造口
8-30、9-20 XELOX方案诱导化疗
2018-10-29开始同步放化疗(DT45GY/25F治疗,放疗日口服卡培他滨)
2018-12-19、2019-1-15 XELOX方案巩固化疗
放化疗后评估
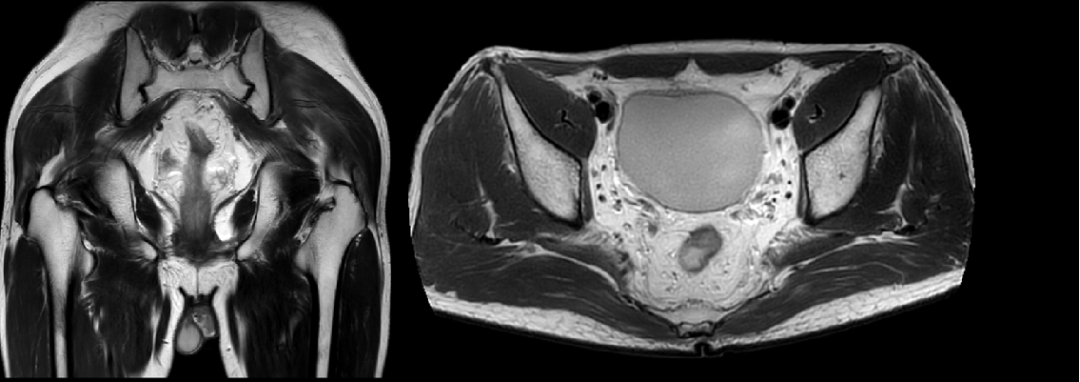
2019-2-14 CT:
1、直肠中上段占位,考虑肿瘤性病变,直肠癌?请结合临床及MR查。
2、直肠筋膜系膜区小淋巴结显示。
MRI:
1、直肠中上段病变,直肠癌可能,MR分期:T3a,直肠系膜筋膜(—)。
2、直肠筋膜系膜区小淋巴结显示。
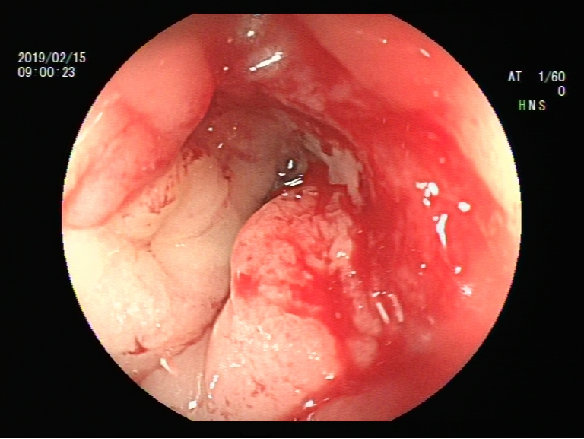
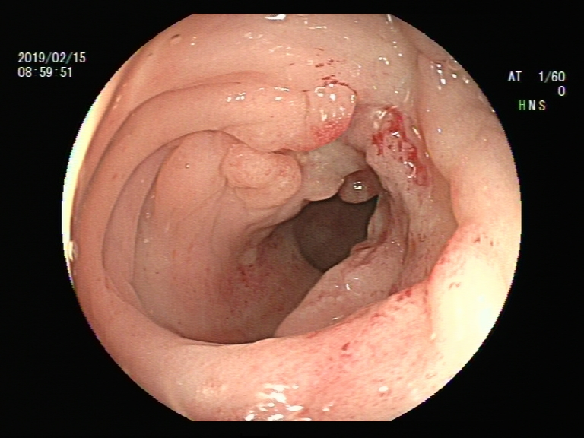
2019-2-15
肠镜:直肠糜烂。
手术:
2019-02-19腹腔镜拖出式直肠癌根治术。
术中见:直肠肿瘤位于腹膜反折处,浆膜面毛糙,肠系膜下动脉根部未见增大淋巴结。
术后病理:(直肠癌新辅助化疗术后)
1、(直肠及肿瘤)收缩区肌层内见部分管状腺癌伴纤维反应,放疗反应符合中度退缩(2级,TRG系统),肿瘤累及全层达外膜,脉管内未见确切癌栓,神经侵犯(-)。
2、远、近两端切缘及环周切缘净。
3、肠周淋巴结未见癌转移(0/2)。MLH1(+),PMS2(+),MSH2(++),MSH6(++)。
病理分期:ypT4aN0M0 Ⅱa期
手术后治疗:
2019-03-19、4-22、5-30、6-28术后辅助xelox方案化疗
2019-10-28造口还纳术
2021年4月复查
2021-4-21 CT:左肺下叶外基底段结节,转移不能排除,较前增大。
诊断:左肺下叶继发恶性肿瘤
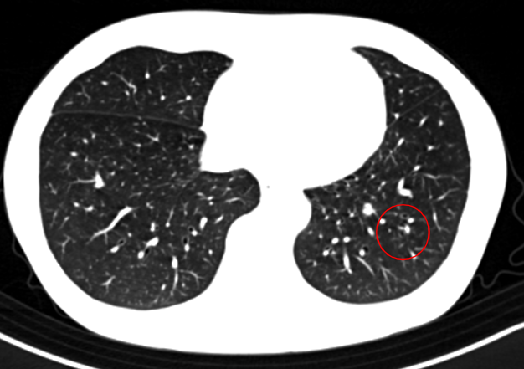
2021-4-22 CT引导下经皮左肺下叶病损微波消融术
基因检测:KRAS、NRAS、PIK3CA、BRAF都为野生型
2021-5-18奥沙利铂+雷替曲塞+西妥昔单抗(胃肠道反应严重,拒绝化疗)
2021年9月复查
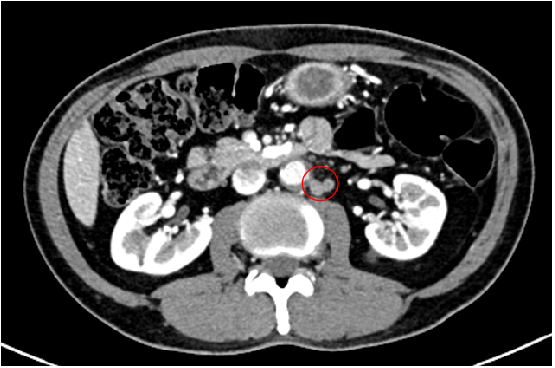
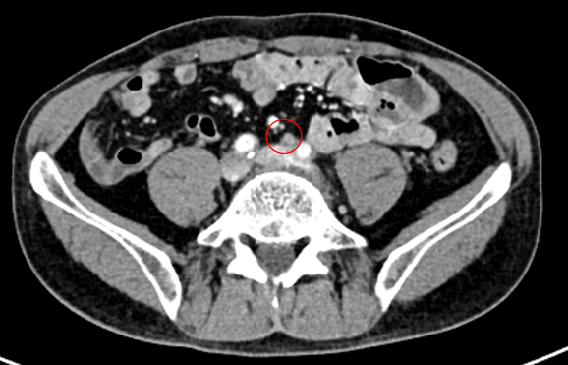
2021-9-14
CT:腹膜后淋巴结显示、增大,较前部分新增、部分增大。右肺上叶前段胸膜下结节(6,101)较前稍显增大。
2022年6月复查
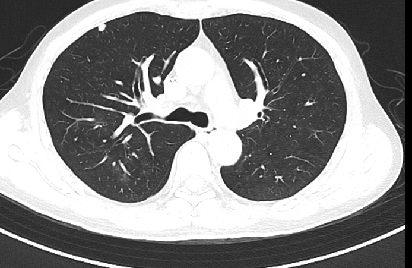
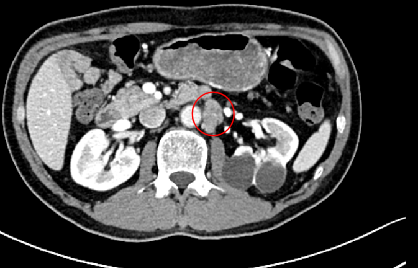
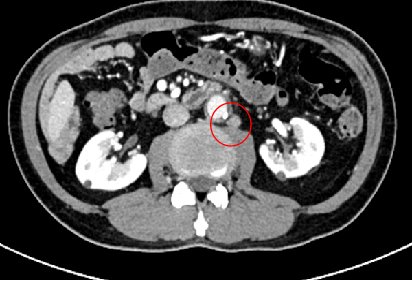
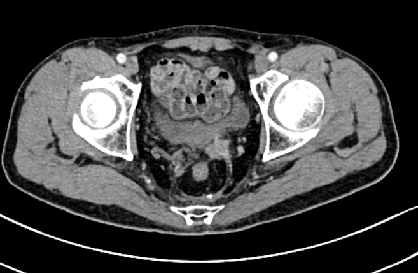
直肠后方、骶前条片状增多软组织影;左侧膀胱精囊角区增多软组织结节影,为新增,转移?腹膜后淋巴结肿大;双肺小结节,转移?
2022-6-30 PET/CT:1、直肠癌术后,术区软组织稍增多,未见异常显像剂浓聚影,考虑术后改变。2、左侧腋窝、腹膜后、左侧髂血管旁多发淋巴结增大,考虑转移。3、盆底直肠筋膜前方软组织密度影伴显像剂浓聚,考虑转移可能,左侧精囊腺受累不除外。4、双肺小结节,密切随诊右肺上叶前段实性结节,除外转移可能。
2022-7-5穿刺活检:(超声引导下左腋窝淋巴结针吸物液基制片)查见癌细胞。(左腋窝淋巴结穿刺组织)转移性腺癌,结合病史、组织形态及免疫组化结果,符合直肠腺癌转移。免疫组化结果:CK20(+),CDX2(+),Her-2(-),CK7(-),TTF-1(-),MLH1(+),MSH2(+),MSH6(+),PMS2(+),Ki-67(+,约80%)。
结论:石蜡包埋样本DNA中KRAS、NRAS、PIK3CA、BRAF都为野生型。
本次微卫星不稳定性(MSI)基因检测结果为:微卫星稳定(MSS)。
治疗
2022-7-9、7-27、8-23西妥昔单抗+曲氟尿苷嘧啶(西妥昔单抗700mg+曲氟尿苷嘧啶55mg bid)
治疗后复查(2022-9)
左侧膀胱精囊角区增多软组织结节影,转移?较前缩小;腹膜后淋巴结肿大,较前缩小;双肺小结节,转移?较前相仿。
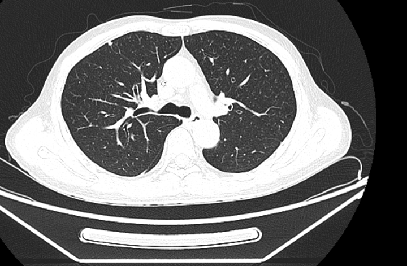
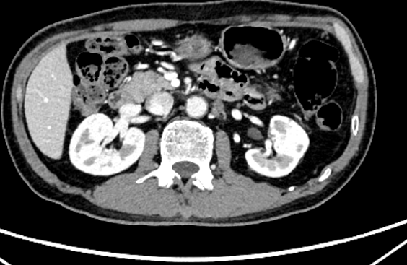
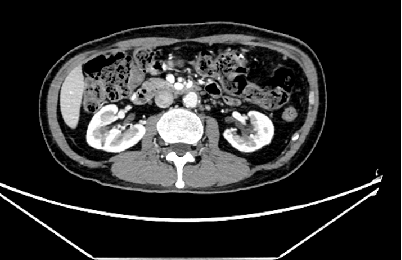
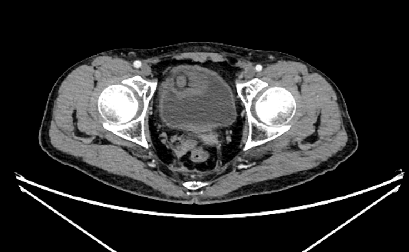
治疗
2022-9-9、9-28西妥昔单抗+曲氟尿苷嘧啶
副反应:
Ⅲ度骨髓抑制、乏力
不能耐受、自行停药等
治疗后复查(2022-11)
直肠后方、骶前条片状增多软组织影,较前变化不大;左侧膀胱精囊角区增多软组织结节影,转移?较前相仿;侵犯输尿管、伴上方左侧输尿管稍扩张积水,较前新增。腹膜后淋巴结肿大,较前稍缩小。
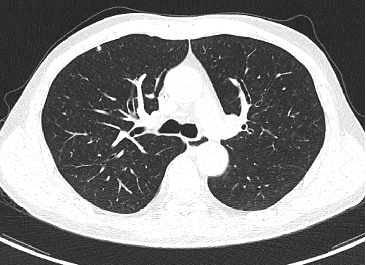
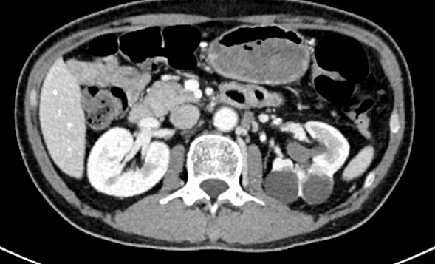
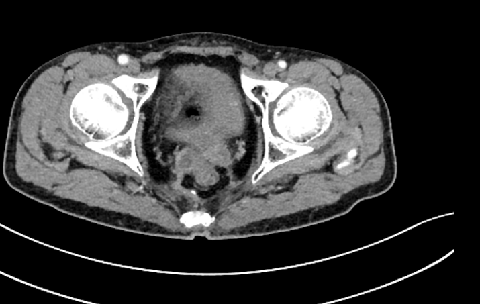
彩超:左侧腋窝暂未见确切肿大淋巴结声像。
2022-10-28 PET/CT示:1、直肠癌术后,术区软组织稍增多,未见异常显像剂浓聚影,考虑术后改变。2、左侧腋窝、腹膜后、左侧髂血管旁多发淋巴结增大,考虑转移。3、盆底直肠筋膜前方软组织密度影伴显像剂浓聚,考虑转移可能,左侧精囊腺受累不除外。4、双肺小结节,密切随诊右肺上叶前段实性结节,除外转移可能。
诊断:直肠癌术后转移(腹膜后、髂血管旁淋巴结、盆底结节)、腋窝淋巴结转移
肿瘤标记物:
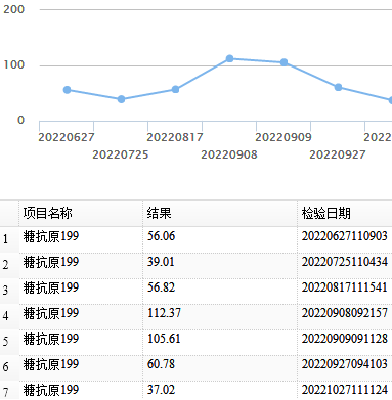
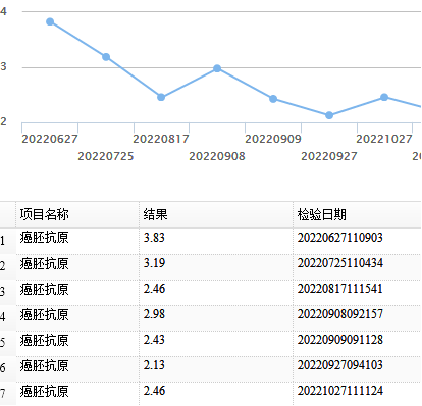
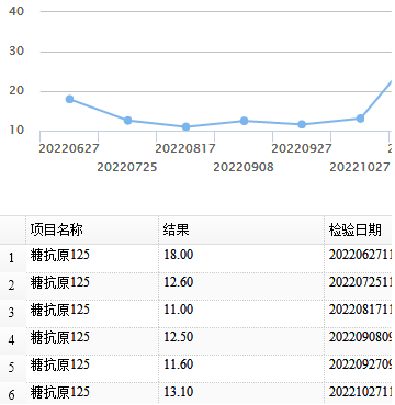
第二次院内MDT
(2018-8)
治疗目标:改善生存、延长OS
治疗方案:继续当前治疗至耐药或者尝试CRS+HIPEC
方案实施:减瘤手术(依从性差)
CRS
2022-11-1腹腔镜盆腔淋巴结清扫术+经尿道输尿管支架置入+肠粘连松解+腹腔穿刺术
手术探查:盆腔有少量淡黄色积液;肝胆胰脾胃、大网膜、肠系膜、盆腔未见肿瘤性结节,左侧腹回肠造口处及右髂窝处小肠、大网膜与腹膜粘连。原直肠吻合口与后方致密粘连,无法满意探及。
术后行腹腔热灌注治疗
术后恢复:左侧输尿管漏
术后病理(直肠癌新辅助化疗术后)
(1)(左侧精囊腺)左精囊腺肌层及周围纤维脂肪组织见腺癌浸润,符合肠癌转移;(2)(左侧盆侧壁结节)纤维组织内局灶见腺癌浸润,符合肠癌转移;(3)左侧髂血管旁结节示少许变性纤维脂肪组织,未见确切癌累及;(4)骶前结节:胶原变性组织局灶见个别异型腺体伴挤压,考虑肠癌转移;(5)盆底淋巴结示部分纤维脂肪组织,未见确切癌累及。
基因检测:KRAS、NRAS、BRAF野生型,MSS
术后治疗及复查
患者拒绝进一步化疗,采取W&W策略
2024-4-27复查CT:同2023-02-01胸部及2023-01-17腹部及盆腔旧片对比:
直肠术后;吻合口壁及直肠壁增厚及增多软组织,较前进展,考虑肿瘤复发转移可能,并累及左侧精囊腺、膀胱壁及左输尿管盆段,其上肠管支架置入术后同前,周围局限积液较前减少,请结合临床随诊。
整体治疗历史回顾
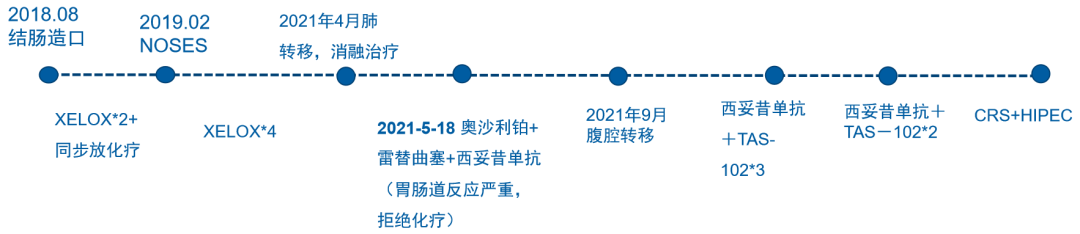
02 病例讨论
问题:RAS野生型患者西妥昔单抗联合TAS102的维持方案如何?CRS+HIPEC干预的作用及时机是否恰当?
福建医科大学附属第一医院-影像科-熊美连:针对直肠癌患者,首次发现一个小于5毫米的肺结节的话,影像上诊断它是一个转移瘤还是非转移瘤还是很困难的。在这种情况下,我们影像可能只能通过后面的随访看一下这个结节的大小变化,那么从给出的几次的随访的图像来看,这个肺部的结节有增多也有变大的,那对于这个转移瘤的诊断应该还是比较明确的。另外,针对这个病例的这个腹膜后盆腔软组织结节和淋巴结来说,影像上增强的强化不太均匀的话,影像的诊断应该也是没有大问题的。
福建医科大学附属第一医院-肿瘤放疗科-柯春林:该直肠癌病例是cT3N1M0Ⅲ期,肿瘤位于中段直肠,术前的诱导以后同步放化疗再加两次的巩固化疗,整个过程非常的规范,得到降期,达到了术前放化疗的目的。术后出现了左肺下的结节,考虑是转移做了消融。消融做完评估NED要很慎重,看到一个孤立的转移灶需要进行更详细的全身评估,一旦转移及时介入全身治疗,即使患者不耐受化疗,最基本的副作用小的全身系统治疗也要联合上,因为如果是新发转移灶,不太可能只有唯一一个,这个时候全身系统治疗是非常重要的。后来出现腹膜后盆腔腋窝的转移,全身系统治疗用了抗EGFR+TAS102,效果也不错。
再后来进行了减瘤手术,这个也是可以理解的,因为病人对手术可能会比较充满希望。但是可能用更微创一点的,或者伤害更小一点的减瘤术,包括局部放疗在内的一些减瘤手段也是可以考虑的。
福建医科大学附属第一医院-介入科-游翔:这个肺部结节确实比较小,如果仅凭CT诊断是否为转移瘤可能会存在一点问题,那在这个时候完善一下PET-CT全身检查,评估一下其他部位是否有其他转移瘤,可能会更恰当。后来做消融治疗,比较微创的一个治疗方法,基本上也把这个转移瘤控制得比较好,配合全身治疗,整体疗效不错。
福建医科大学附属第一医院-结直肠外科-庄金福:这个病例也让我学习到很多,首先这个病人从2018年发现肿瘤到现在2024年,活了5年多,经过严教授团队的努力病人有了很好的一个生存期,并且学习到了肠癌病人腋窝淋巴结转移这样比较少见的病例。
个人认为很多肿瘤到了T4a的时候做Noses对病人来说会比较辛苦一点。之后肺部、腋窝、腹膜后都有转移了,而且腹膜后的转移目前来说是不可转化,没办法达到NED状态的,这个时候做CRS跟HIPEC治疗这么大的手术,这在我们中心还是比较少的,除非有很明显相关的急危症,比如穿孔、梗阻、出血等需要我们去处理的问题。
关于西妥昔单抗+TAS 102的治疗方式我也是学习了,特别像这个病人整体来说还是比较惰性的,会有一个很好的一个生存期,西妥昔单抗+TAS 102的确让我们感受到在患者的维持中可以获益良多。
福建医科大学附属第一医院-肿瘤内科-刘晨:结直肠癌一二线治疗后可能跟外科缘分已尽,内科医生仍然愿意在三线四线甚至继续往下做,这是因为结直肠癌是实体瘤中疗效比较好的。虽然之前的内科治疗方案相对较少,除开奥沙利铂跟伊立替康,就没有什么药可以用。但是现在通过一些临床研究,又有TAS102、呋喹替尼之类的新药,结直肠癌患者的晚期生存质量还是有所保障。
今天的病例我觉得还是可圈可点,首先这是一个中年中高位直肠癌的Ⅲ期病人,KRAS、NRAS、BRAF都为野生型,那其病情上面并没有看到很明显的难治表现,新辅助治疗还是成功的,肿瘤退缩还能达到2级,这个还是不错的。而之后的靶向治疗,特别是在第一次出现转移之后,用了西妥昔单抗的治疗还是很成功,在西妥昔单抗和TAS102的结合下,PFS达到12个月,我们认为还是一个成功的晚期一线治疗,这里面团队做了创新性尝试,就是TAS102,在指南上一般都是奥沙利铂和伊立替康使用后三线甚至后线的一个治疗,那这个用在晚期二线的治疗效果能够这么好,我们认为这是一个创新结果,是值得我们参考的。
不过PD之后没有选择进行全身治疗,而是做了减瘤手术和腹腔热灌注,这个事情可能就体现了外科思维跟内科思维的差异,我们内科医生肯定就会反反复复地一直给这个病人做思想教育了,告诉他这个时候全身治疗有多重要,实在都不能接受,我们可能会选择呋喹替尼口服。那我们觉得这个时候病人短期内没有危及生命的外科症状的时候,不以NED为目的的减瘤手术,对病人的远期生存到底会不会有改善?这是一个值得讨论的地方。那这个病人确实就在这个减瘤手术之后不到五个月的时间内又复发了,之后如何治疗?如果他没有办法接受系统性治疗,确实这个病人后续的生存状态是比较堪忧的。
03 MDT小结
患者是一位 55 岁男性,于 2018 年底首次确诊直肠腺癌后,发生左肺下叶、左侧腋窝、腹膜后、盆腔淋巴结等多处转移,期间患者化疗不耐受,自行停药,拒绝接受进一步化疗。目前患者生活质量能够维持,但是腹腔的肿瘤还在缓慢地进展,采取等待观察的治疗策略中。
肖莉 述评——厦门大学附属中山医院
这个病例有两个节点可能是争议最大的,第一个节点就是第一轮围手术期治疗,因为这个病人初诊就是局部晚期的中段直肠腺癌,经过了围手术期的新辅助放化疗诱导后,它的降期和病理的缓解不是十分让人满意,术后还是T4分期。所以回过头来看,围手术期治疗,尤其是诱导治疗是不是能用一些更优化的方案,比如PRODIGE 23这样的治疗模式。第二个争议非常大的就是第二次CRS手术是否有必要做,因为在这个节点我们认为它可能已经是全身播散的,不只有腹腔内的病变,这个时候CRS可能对病人的远期获益不会有特别大帮助,所以这个时候以全身系统治疗为主可能更佳。
现在TAS102医保的适应症是既往只要接受过生物大抗和三种化疗药以后进展的病例就可以用TAS102,即医保的适应症远远突破指南上局限于三线的推荐,可能到二线的病人就可以使用。比如说第一线用了FOLFIRINOX+贝伐珠单抗的病人,二线就可以用TAS102做医保报销了。所以未来TAS102的应用场景和前景应该不只局限于SUNLIGHT,可能更多的和其他一些免疫抗血管的小分子TKI等结合,这可能是未来的组合研究方向。而西妥昔单抗诱导联合化疗之后,不一定西妥昔单抗一直走到底,可以用一个更优化经济性价比更高的方案维持。


