好文推荐 | 基于多模态MRI探讨参芪益智颗粒对高原地区前驱期阿尔茨海默病患者的疗效观测
时间:2025-02-13 12:13:06 热度:37.1℃ 作者:网络
摘要
目的 基于多模态磁共振成像技术探讨参芪益智颗粒对低氧环境下前驱期阿尔茨海默病(pAD)脑结构和功能的影响。方法 选择久居青海地区符合pAD纳入标准,年龄50~85岁、文化程度≥6年、汉族女性患者77例作为受试者。随机分为药物组(参芪益智颗粒)39例,对照组(安慰剂)38例进行临床观察24周。采集受试者临床信息、认知及神经心理测评和扩散张量成像(DTI)、静息态功能磁共振成像(rs-fMRI)。结果 认知及神经心理结果显示,药物组患者MoCA、AVTL、SDMT、CFT-copy得分明显高于治疗前,ADAS-cog和GDS得分显著低于治疗前(P<0.05);对照组ADAS-cog得分明显高于治疗前(P<0.001);治疗后药物组MoCA、AVTL得分高于对照组(P<0.05),ADAS-cog得分低于对照组(P<0.01)。DTI结果显示,治疗后药物组多个脑区的轴向扩散系数升高(P<0.05)。rs-fMRI结果显示,治疗后药物组右侧颞极:颞中回、三角部额下回、内侧和旁扣带回ALFF值升高,左侧小脑半球Crus1小叶、枕上回和缘上回ALFF值降低,药物组右侧背外侧额上回ALFF值较对照组升高(P<0.05)。治疗后药物组左侧三角部额下回和枕下回ReHo值升高,右侧小脑半球Crus1小叶下降(P<0.05),药物组左侧顶下缘角回ReHo较对照组升高(P<0.05)。结论 参芪益智颗粒通过调节认知相关脑区的白质微观结构和自发神经元活动,能够有效改善高原地区pAD总体认知和多认知域功能。
阿尔茨海默病(Alzheimer disease,AD)是一种进行性中枢神经系统变性疾病,是痴呆最常见的原因,以损害认知功能和记忆能力为主要临床表现,一旦发病不可逆转,疾病发展至中晚期难以进行有效治疗,会加重家庭和社会负担。研究表明,预计到2050年,全球AD患病人数将增加到1.31亿,因此如何在痴呆前阶段进行干预和治疗显得尤为重要。近年来,对AD的研究热点逐渐转移到了痴呆前阶段,包括主观认知功能下降(subjective cognitive decline,SCD)和轻度认知功能障碍(mild cognitive impairment,MCI),流行病学调查指出,我国60岁以上MCI患者约3 877万。高原具有低压低氧的特点,当长期暴露于高原低氧环境时,低氧环境可通过多种方式诱发或加重AD脑部的病理改变,导致机体出现认知功能损害。在既往基于扩散张量成像(diffusion tensor imaging,DTI)的研究中,发现AD患者从SCD进展至MCI,并最终演变为AD的过程中,DTI参数的变化反映出白质微结构的逐渐恶化,通常表现为各向异性分数(fractional anisotropy,FA)的降低和平均扩散系数(mean diffusivity,MD)的增加。此外,静息态磁共振功能成像(resting-state functional magnetic resonance imaging,rs-fMRI)的研究进展表明,在AD的不同阶段,低频振幅(amplitude of low frequency fluctuation,ALFF)和局部一致性(regional homogeneity,ReHo)的变化反映了大脑功能活动的异常,这些异常与认知功能减退、Aβ斑块沉积以及脑血流改变密切相关。参芪益智颗粒作为中医经验方,包含人参、黄芪、丹参、黄芩、泽泻等草药,具有促进气血、健脾益肾、安神益智、解毒通络的功效。前期研究已表明,参芪益智颗粒对多种AD的病理进程具有不同程度的改善作用,能够有效改善患者认知。本研究拟通过神经心理学检查结合多模态MRI观察参芪益智颗粒治疗对pAD患者的影响,并初步探讨其疗效的脑效应机制,以期为参芪益智颗粒在pAD研究中提供客观的影像学依据。
1 资料与方法
1.1 一般资料
采用随机、双盲、安慰剂对照试验方法,对2020年6月—2021年12月就诊于青海省人民医院认知障碍门诊50~85岁、文化程度≥6年人群进行筛查,共纳入pAD汉族女性患者80例,随机分为药物组和对照组各40例,最终完成研究的药物组39例、对照组38例。
1.2 纳入标准
(1)符合SCD诊断标准:主观上感觉记忆力下降,但客观的检查没有明显认知功能障碍;发病时间在近5年;或存在相关危险因素(如存在APOE4等位基因和(或)定义临床前AD的生物标志物,临床痴呆评定量表(clinical dementia rating,CDR)0分。(2)符合国际工作组在2003年修订的MCI诊断标准:患者和(或)知情者主诉有记忆力减退;存在一个或多个认知域损害的客观认知任务障碍;日常复杂的工具性生活能力可有轻微损害;尚未达到痴呆的诊断标准(CDR 0.5分)。(3)年龄50~85岁,右利手。(4)教育程度≥6年。(5)在青海地区居住20年以上(平均海拔:2 260 m)。(6)自愿参加试验并签署知情同意书。
1.3 排除标准
(1)脑外伤、脑梗死、脑出血、颅内占位等其他颅脑器质性病变。(2)既往有抑郁症、双相障碍或精神分裂症等严重精神疾病。(3)严重心、肺、肝、肾功能不全或其他重大疾病。(4)不能配合完成神经心理量表,如失语、听力及视力障碍。(5)存在MRI禁忌证。(6)近3个月使用其他改善认知的药物。
1.4 脱落标准
(1)自愿退出试验或因发生严重不良事件或不良反应相关因素退出试验。(2)患者在服药期间未能按规定用药或未能及时接受临床检查。(3)随访资料不完整,无法准确评估药物疗效的患者。(4)依从性不佳的患者,包括无法完成随访或自行更换治疗方案的患者。
1.5 方法
1.5.1 一般资料收集
收集所有研究对象的相关信息资料,包括年龄、受教育年限等人口学资料。
1.5.2 相关量表评估
由同一位受过专业培训的神经内科医师对两组治疗前后均进行神经心理量表评估。其中采用蒙特利尔认知评估(Montreal Cognitive Assessment,MoCA)量表评估整体认知功能,在情景记忆方面采用听觉词语记忆测验(Auditory Verbal Learning test,AVTL),注意力方面采用数字符号转换测验(Symbol-Digit Modalities Test,SDMT),视空间方面采用Rey-Osterrieth复杂图形测验-模仿(Copy Task of Complex Figure Test,CFT-copy),精神症状方面采用老年抑郁量表(Geriatric Depression Scale,GDS)进行评估,对AD病情以及治疗效果的评估采用阿尔茨海默病评定量表(Alzheimer’s Disease Assessment Scale-cognitive subscale,ADAS-cog)进行评定。
1.5.3 MRI数据采集
所有受试者治疗前后均使用同一台3.0T MRI扫描仪(型号:Siemens MAGNETOM Skyra)和20通道头线圈进行磁共振检查。在采集过程中,嘱受试者放松、闭眼、保持清醒、体位固定、避免任何思维活动,并戴好耳机,将泡沫塞入线圈与头部的间隙中,以减少头动伪影。成像方案包括3D磁化准备快速梯度回波T1加权序列(3D-T1MPRAGE)用于解剖学成像,静息态功能磁共振成像(rs-fMRI)采用T2*回波平面成像梯度回波序列,并进行扩散张量成像(DTI)序列扫描。此外,受试者均采集常规MR序列(轴向T2WI、T2-FLAIR和DWI)以检测脑部异常。
1.5.4 影像数据处理
DTI预处理步骤包括视觉质量控制,基于Marchenko-Pastur主成分分析的去噪,Gibbs伪影去除和对磁化率引起的畸变,涡流引起的畸变以及头部运动的动态校正,生成了基于扩散加权成像(DWI)数据的大脑掩膜,并进一步计算了DTI指标,使用的工具来自MRtrix3(www.mrtrix.org/,版本3.0.4)和脑功能磁共振成像软件库(FSL,版本6.0.7)。使用FSL进行TBSS分析,将FA图配准到标准空间(MNI152空间),并生成标准化的FA图像。将所有参与者的标准化FA图结合,生成一个代表共同白质结构的平均FA图,并对其进行骨架化处理,生成白质骨架。将每个参与者的FA图的最高值投射到公共白质骨架上,从而生成用于统计分析的白质骨架图。fMRI数据预处理由基于Matlab2024b的RESTplus(V1.30)的流水线模块完成。主要步骤包括去除前10个时间点的数据、时间层校正、头动校正、结构像分割、协变量回归、配准到蒙特利尔神经科学研究所(Montreal Neurological Institute,MNI)标准空间,进行图像平滑处理。
1.5.5 药物治疗
药物组患者接受参芪益智颗粒治疗方案。材料:参芪益智颗粒由广东一方制药有限公司受托生产批号:J2004002。主要成分为:人参、黄芪、丹参、黄芩、泽泻。用法用量:每次1包,每日2次,开水冲服。安慰剂组药物主要成分为淀粉,与药物组外包装、气味一致。用法用量与药物组一致。两组患者疗程均为6个月,研究期间禁止所有患者使用其他改善认知的药物。治疗期间记录两组有无出现不良反应(头晕、恶心、乏力等)的发生。
1.6 统计学分析
采用SPSS 26.0统计软件对一般资料、多维度认知域和神经心理量表评分进行统计分析,治疗前后组内量表评分的比较行配对t检验,两组间比较行双样本t检验,以P<0.05为差异有统计学意义。DTI数据使用Randomise工具进行非参数统计分析,同组前后对比采用配对t检验,两组间对比采用双样本t检验,对不同组之间的FA、MD等DTI指标进行比较,以确定在白质骨架上具有统计显著性的区域。统计结果行无阈值集群增强(threshold-free cluster enhancement,TFCE)校正,以减少多重比较引起的假阳性率,排列次数为500,P=0.05。rs-fMRI数据采用统计分析模块对同一组治疗前后各指标进行配对t检验,两组间采用双样本t检验,多重比较校正采用高斯随机场(gaussian random field,GRF)校正(体素水平P=0.05,聚类水平P=0.05)。
2 结 果
2.1 一般临床资料比较
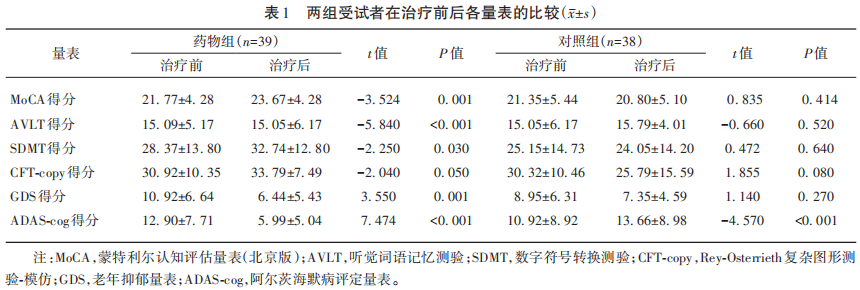
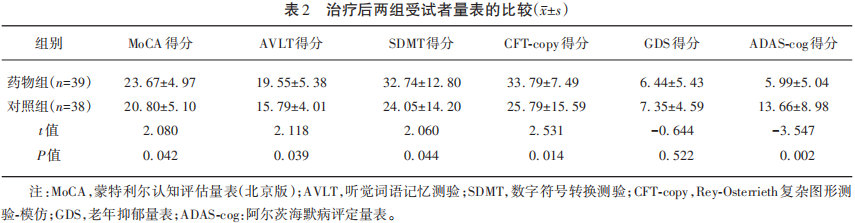
本次研究纳入的汉族女性患者共77例,平均年龄为63.42岁,平均受教育年限为9.85年。治疗前,两组患者年龄、文化程度、神经心理评估(MoCA、GDS)、多维度认知域量表(AVLT、SDMT、CFT-copy)和ADAS-cog得分无显著统计学差异(P>0.05),具有可比性。在总体认知功能方面,药物组MoCA得分明显高于治疗前(P<0.05),治疗后的药物组得分高于对照组(P<0.05)。情景记忆方面,治疗后药物组AVLT得分高于治疗前(P<0.05),治疗后的药物组高于对照组(P<0.05)。在注意力方面,治疗后的药物组SDMT得分高于治疗前(P<0.05),且治疗后的药物组SDMT得分高于对照组(P<0.05)。视空间方面,药物组治疗后CFT-copy得分高于治疗前(P<0.05),且治疗后两组间CFT-copy得分也有差异(P<0.05)。老年抑郁方面,药物组GDS评分明显降低,抑郁情况得到改善(P<0.001)。在AD病情改变方面,药物组治疗后ADAS-cog得分明显低于治疗前,表明情况有好转,而对照组ADAS-cog得分明显高于治疗前(P<0.001),且药物组治疗后得分明显低于对照组(P<0.01)。结果见表1、表2。参芪益智颗粒安全性较好,治疗期间未发生明显的不良反应。
2.2 影像数据比较
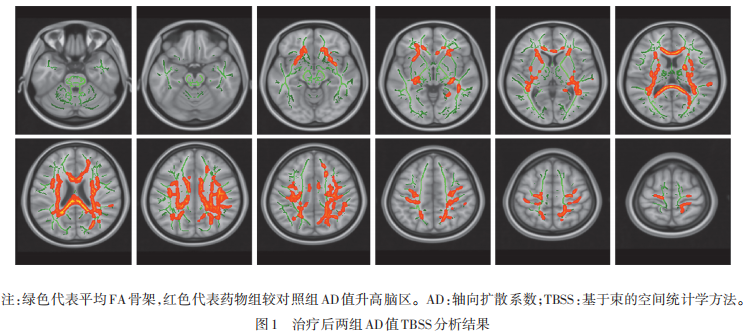
DTI结果显示,经过24周的治疗后,与对照组相比,药物组在胼胝体压、体及膝部、双侧上纵束、后、上及前辐射冠、双侧内囊豆状核后部和丘脑后辐射的轴向扩散系数(axial diffusivity,AD)升高(P<0.05,TFCE校正),而未见AD值显著降低的脑区。(见图1)。
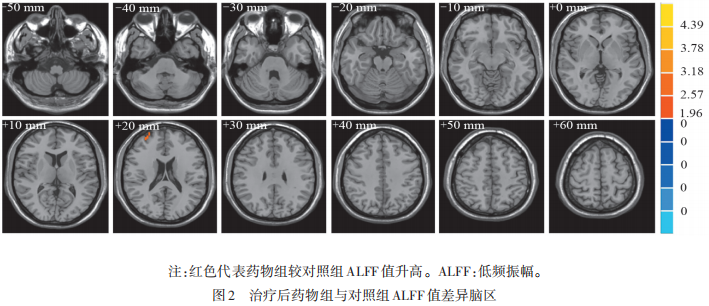
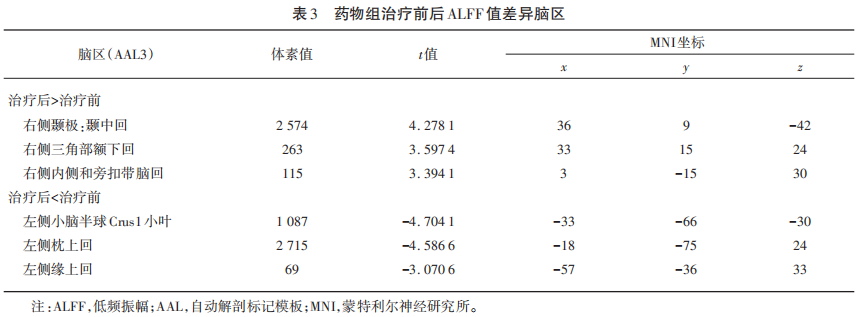
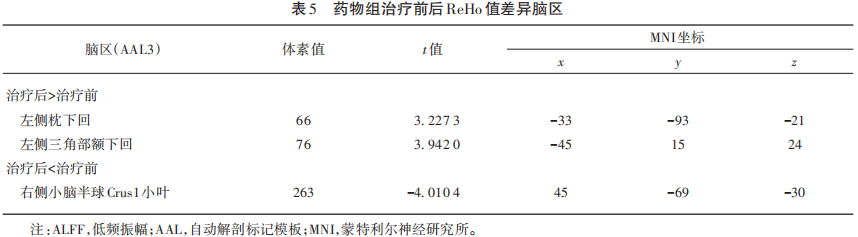
rs-fMRI结果显示:治疗24周后,药物组右侧颞极:颞中回、三角部额下回、内侧和旁扣带回ALFF值升高,左侧小脑半球Crus1小叶、枕上回和缘上回ALFF值降低;与对照组对比,药物组右侧背外侧额上回ALFF值升高(见图2)(见表3、表4)。ReHo结果显示,治疗后药物组左侧三角部额下回和枕下回升高,右侧小脑半球Crus1小叶下降;而对照组干预前后脑区ReHo无显著差异;与对照组对比,药物组的左侧顶下缘角回ReHo升高(见图3)(见表5、表6)。



3 讨 论
在本次研究中,我们发现参芪益智颗粒能够有效改善pAD患者的临床症状,包括总体认知和多领域行为认知如情景记忆、注意力、视空间能力以及抑郁症状。AD在中医典籍中属于“呆病”范畴,参芪益智颗粒是王永炎院士在古老方剂理论的支持下,根据长期临床经验提炼的治疗AD的临床经验方,已有研究表明,参芪益智颗粒可以通过多种机制干预AD的病理环节,并取得良好的临床疗效,从而延缓AD的进展。一项研究发现,参芪益智颗粒对5xFAD小鼠海马的药理机制可能与调节能量代谢、应激反应、细胞骨架等多种病理过程有关,并可调节突触传递、信号转导、氨基酸代谢、DNA修复等。Li等研究发现参芪益智颗粒可以通过抑制Aβ诱导的JAK2/STAT3途径减弱活化的星形胶质细胞来改善认知功能障碍。Wang等发现参芪益智颗粒通过调节脂质代谢、金属离子代谢、IL-17信号通路、GABA受体信号传导和神经活性配体-受体相互作用来缓解AD的认知障碍,其改善认知功能的分子机制与人参皂苷Rg1和Aβ1-42、丹参酮ⅡA和BACE1以及黄芩苷和AchE之间的高结合亲和力有关。然而,参芪益智颗粒如何改善pAD认知功能障碍的脑结构和脑功能尚不明确,需要进一步研究。本研究通过多模态磁共振技术探究脑结构和脑功能变化来阐释参芪益智颗粒改善AD认知功能障碍的可能作用机制,为参芪益智颗粒防治认知功能障碍提供了科学依据。
DTI是一种描述水分子扩散特征的技术,能有效观察和追踪脑白质纤维束,直接从微观水平反映神经元功能的改变。其中FA和MD可以反映脑白质微观结构的完整性,轴向扩散系数(axial diffusivity,AD)和径向扩散系数(radial diffusivity,RD)分别反映了轴突和髓鞘的完整性。最新的文献报道,在初始阶段,淀粉样蛋白负荷的增加与较低的扩散性指标(MD、AD、RD)相关,而在负荷进一步增加后,扩散性指标反而增高,这可能表明在不同的淀粉样蛋白负荷阶段,脑组织的微观结构和功能状态有所差异。另一项关于组织学的研究发现,初始的AD值降低与急性轴突损伤(如轴突肿胀和断裂)有关,而随后AD值增加与小胶质细胞清除膜碎片和轴突密度降低相关,提示神经修复或清除机制可能发挥了作用。经过参芪益智颗粒治疗24周后,pAD患者在多个脑区(如胼胝体、上纵束、辐射冠、内囊豆状核和丘脑后辐射)的AD值升高,推测研究对象的淀粉样蛋白负荷可能处于较低阶段,且治疗前的急性轴突损伤导致AD值降低。参芪益智颗粒具有修复轴突损伤和改善白质微观结构的潜力,促进认知功能的改善,从而表现为药物组AD值升高。然而,在本次研究中,我们发现对照组对pAD患者部分脑区同样存在AD值升高效应,我们详细分析其原因,可能从以下几个方面进行解释:其一可能是纳入患者病情较轻,导致药物特异性不明显;其次我们未能对pAD患者进行长期疗效追踪;再其次可能是招募的志愿者对中药持积极态度,这种期待效应可能会过度优化反应,改善对照组患者的症状。尽管两组均表现出AD值的升高,但药物组改变的脑区要明显多于对照组,这可能表明药物组的治疗效果更为广泛,从而对认知产生更全面的改善,仅药物组在认知量表方面有所好转进一步支持了这一点。此外,本研究还发现DTI指标中仅AD值有阳性结果,这可能表明AD值在观察早期轴突损伤-修复过程方面较为敏感。
低频波动幅度(ALFF)和局部一致性(ReHo)是静息态功能磁共振成像(rs-fMRI)评估大脑静息状态下自发神经活动的两个重要指标,提供了关于大脑功能状态和区域活动强度的重要信息。在pAD患者的研究中,ALFF的结论并不一致,大多数研究发现ALFF值同时存在升高和降低,一部分研究仅发现ALFF值降低,且不同研究所表现出受影响的大脑区域多种多样。
在参芪益智颗粒治疗后,前脑部多个与认知和记忆功能相关的脑区ALFF值显著升高,包括右侧三角部额下回、颞极:颞中回、内侧和旁扣带回。相较于对照组,药物组治疗后在背外侧额上回的ALFF值升高。众所周知,额叶与认知、记忆功能有关,而额下回是参与认知控制和语义处理的重要枢纽,在注意力和工作记忆维持中起重要作用,颞中回是参与语言、记忆处理的重要脑区,有研究发现,右侧颞中回与记忆有关,且颞中回局部自发脑活动的变化与情景记忆关系密切。内侧和旁扣带回则是参与了情感和感觉处理。背外侧额上回属于背外侧前额叶,参与高级认知任务及介导情绪调节。以往的研究显示,与健康对照组相比,pAD患者的上述脑区存在ALFF值降低的情况,因此本研究表明,经过中药治疗后以上脑区ALFF值得以升高,表明与认知相关脑区的自发神经元活动增强,可能与认知功能改善相关。
先前的研究已经揭示,SCD患者的顶下小叶、小脑及枕回的ALFF值呈现上升趋势,这可能与脑功能代偿性改变相关。我们进一步发现,经过中药参芪益智颗粒治疗,患者后脑部的特定区域,包括左侧枕上回、缘上回及小脑半球Crus1小叶ALFF值有所降低。枕上回在视觉信息处理中扮演着重要角色,其变化可能对pAD患者早期视觉空间记忆任务的表现产生影响。缘上回作为顶下小叶的组成部分,与记忆力和执行力等认知功能紧密相关。近期的研究成果也表明,小脑不仅参与运动控制,还涉及记忆、学习、语言和情感等认知过程。我们推测,参芪益智颗粒通过降低这些脑区的ALFF值,表明该药存在纠正相应脑区过度代偿的机制。
ReHo的分析结果揭示了药物组在治疗24周后的变化:左侧枕下回和三角部额下回ReHo值升高,而右侧小脑半球Crus1小叶ReHo值降低。这些变化表明ReHo值的改变同样与脑功能代偿有关。具体来说,这些脑区在多认知域功能中扮演着重要角色:如三角部额下回作为额顶网络(FPN)的组成部分,涉及执行功能和工作记忆;枕下回属于视觉网络(VSN),主要负责视觉信息的处理;角回是韦尼克区的一部分,负责语言与空间定位,同时参与语义加工;小脑除了维持身体姿势和平衡,一定程度上也参与了情绪控制和认知加工。
参芪益智颗粒对脑区的激活升高表明该药物能增强特定脑区的神经活动,进而改善功能;而脑区激活的降低可能与药物对过度代偿脑区的调节有关。综合以上多认知域相关的重要脑区,反映出参芪益智颗粒具有激活或降低相关脑区神经活动的能力,从而表现出对pAD患者总体认知能力、注意力以及视空间等多个认知领域的双向调节和整体调节效应,通过平衡异常脑区的活动,改善高原地区患者的认知功能异常。
本研究的不足之处:样本量相对较小,存在一定选择偏倚,且缺乏后期随访,限制了对pAD患者长期疗效的评估。今后将开展多中心、大样本研究,增强研究结果的普适性和可靠性,并进行纵向研究进一步评价参芪益智颗粒对患者认知功能的长期影响,同时增设正常对照组,以观察基线期pAD和正常组之间的影像差异,并评估药物治疗后相关脑区异常的影像变化是否向正常认知组方向改善。
参考文献
[1]Jia L,Du Y,Chu L,et al. Prevalence,risk factors,and management of dementia and mild cognitive impairment in adults aged 60 years or older in China:a cross-pal study[J]. Lancet Public Health,2020,5(12):e661-e671.
[2]中华医学会神经病学分会痴呆与认知障碍学组,中国医师协会神经内科医师分会认知障碍疾病专业委员会. 前驱期阿尔茨海默病的简易筛查中国专家共识(2023年版)[J]. 中华神经医学杂志,2023,22(05):433-444.
[3]Ren R,Qi J,Lin S,et al. The China Alzheimer Report 2022[J]. Gen Psychiatr,2022,35(1):e100751.
[4]Ji W,Zhang Y,Luo J,et al. Memantine ameliorates cognitive impairment induced by exposure to chronic hypoxia environment at high altitude by inhibiting excitotoxicity[J]. Life Sci,2021,270:119012.
[5]Urrunaga-Pastor D,Chambergo-Michilot D,Runzer-Colmenares FM,et al.Prevalence of cognitive impairment and dementia in older adults living at high altitude:a systematic review and meta-analysis[J]. Dement Geriatr Cogn Disord,2021,50(2):124-134.
[6]Wang L,Xu X,Wang Z,et al. Network pharmacology and molecular docking-based strategy to investigate the multitarget mechanisms of shenqi yizhi granule on Alzheimer’s disease[J]. Evid Based Complement Alternat Med,2022,2022:8032036.
[7]Li P,Wu Q,Li X,et al. Shenqi Yizhi Granule attenuates Aβ(1)(-)(42) induced cognitive dysfunction via inhibiting JAK2/STAT3 activated astrocyte reactivity[J]. Exp Gerontol,2021,151:111400.
[8]Ren J,Wei D,An H,et al. Shenqi Yizhi granules protect hippocampus of AD transgenic mice by modulating on multiple pathological processes[J]. J Ethnopharmacol,2020,263:112869.
[9]Jessen F,Amariglio RE,van Boxtel M,et al. A conceptual framework for research on subjective cognitive decline in preclinical Alzheimer’s disease[J]. Alzheimers Dement,2014,10(6):844-852.
[10]Winblad B,Palmer K,Kivipelto M,et al. Mild cognitive impairment-beyond controversies,towards a consensus:report of the international working group on mild cognitive impairment[J]. J Intern Med,2004,256(3):240-246.
[11]Collij LE,Ingala S,Top H,et al. White matter microstructure disruption in early stage amyloid pathology[J]. Alzheimers Dement (Amst),2021,13(1):e12124.
[12]Winklewski PJ,Sabisz A,Naumczyk P,et al. Understanding the physiopathology behind axial and radial diffusivity changes-what do we know?[J]. Front Neurol,2018,9:92.
[13]Zang YF,He Y,Zhu CZ,et al. Altered baseline brain activity in children with ADHD revealed by resting-state functional MRI[J]. Brain Dev,2007,29(2):83-91.
[14]Pan P,Zhu L,Yu T,et al. Aberrant spontaneous low-frequency brain activity in amnestic mild cognitive impairment:A meta-analysis of resting-state fMRI studies[J]. Ageing Res Rev,2017,35:12-21.
[15]Rolls ET. The hippocampus,ventromedial prefrontal cortex,and episodic and semantic memory[J]. Prog Neurobiol,2022,217:102334.
[16]Tops M,Boksem MA. A potential role of the inferior frontal gyrus and anterior insula in cognitive control,brain rhythms,and event-related potentials [J]. Front Psychol,2011,2:330.
[17]Humphries C,Love T,Swinney D,et al. Response of anterior temporal cortex to syntactic and prosodic manipulations during sentence processing[J]. Hum Brain Mapp,2005,26(2):128-138.
[18]Zheng Z,Zhu X,Yin S,et al. Combined cognitive-psychological-physical intervention induces reorganization of intrinsic functional brain architecture in older adults[J]. Neural Plast,2015,2015:713104.
[19]Yang L,Yan Y,Wang Y,et al. Gradual disturbances of the amplitude of low-frequency fluctuations (ALFF) and fractional ALFF in alzheimer spectrum[J]. Front Neurosci,2018,12:975.
[20]王心茹,邱丽华. 青少年抑郁症性别差异的磁共振脑结构成像研究进展 [J]. 临床放射学杂志,2023,42(10):1689-1692.
[21]Ni L,Liu R,Yin Z,et al. Aberrant spontaneous brain activity in patients with mild cognitive impairment and concomitant lacunar infarction:A resting-state functional MRI study[J]. J Alzheimers Dis,2016,50(4):1243-1254.
[22]Sun Y,Dai Z,Li Y,et al. Subjective cognitive decline:mapping functional and structural brain changes-A combined resting-state functional and structural MR imaging study[J]. Radiology,2016,281(1):185-192.
[23]Stoodley CJ,Valera EM,Schmahmann JD. Functional topography of the cerebellum for motor and cognitive tasks:an fMRI study[J]. Neuroimage,2012,59(2):1560-1570.


