【NEJM】Cilta-cel治疗RRMM后2例CAR+ T细胞淋巴瘤的报道
时间:2025-02-16 12:11:20 热度:37.1℃ 作者:网络
CAR-T后T细胞肿瘤
CAR-T细胞疗法显著改善了多种血液恶性肿瘤的预后,近期关于继发性T细胞恶性肿瘤成为关注的焦点,但多数研究显示整体风险极低,CAR-T治疗后需要密切监测。
Ciltacabtagene autoeucel(cilta-cel)是一种FDA批准的BCMA CAR-T细胞疗法,通过慢病毒转导产生,3期随机CARTITUDE-4研究证实了cilta-cel与标准治疗相比可显著提高无进展生存期。
新英格兰医学杂志2月13日报道了两例接受cilta-cel治疗后出现的外周T细胞淋巴瘤(PTCL-NOS),带有CAR转基因整合和表达的恶性单克隆T细胞淋巴增生,作者将其称为CAR转基因T细胞淋巴增殖性肿瘤(CAR transgenic T-cell lymphoproliferative neoplasm,CTTLN)。

患者1
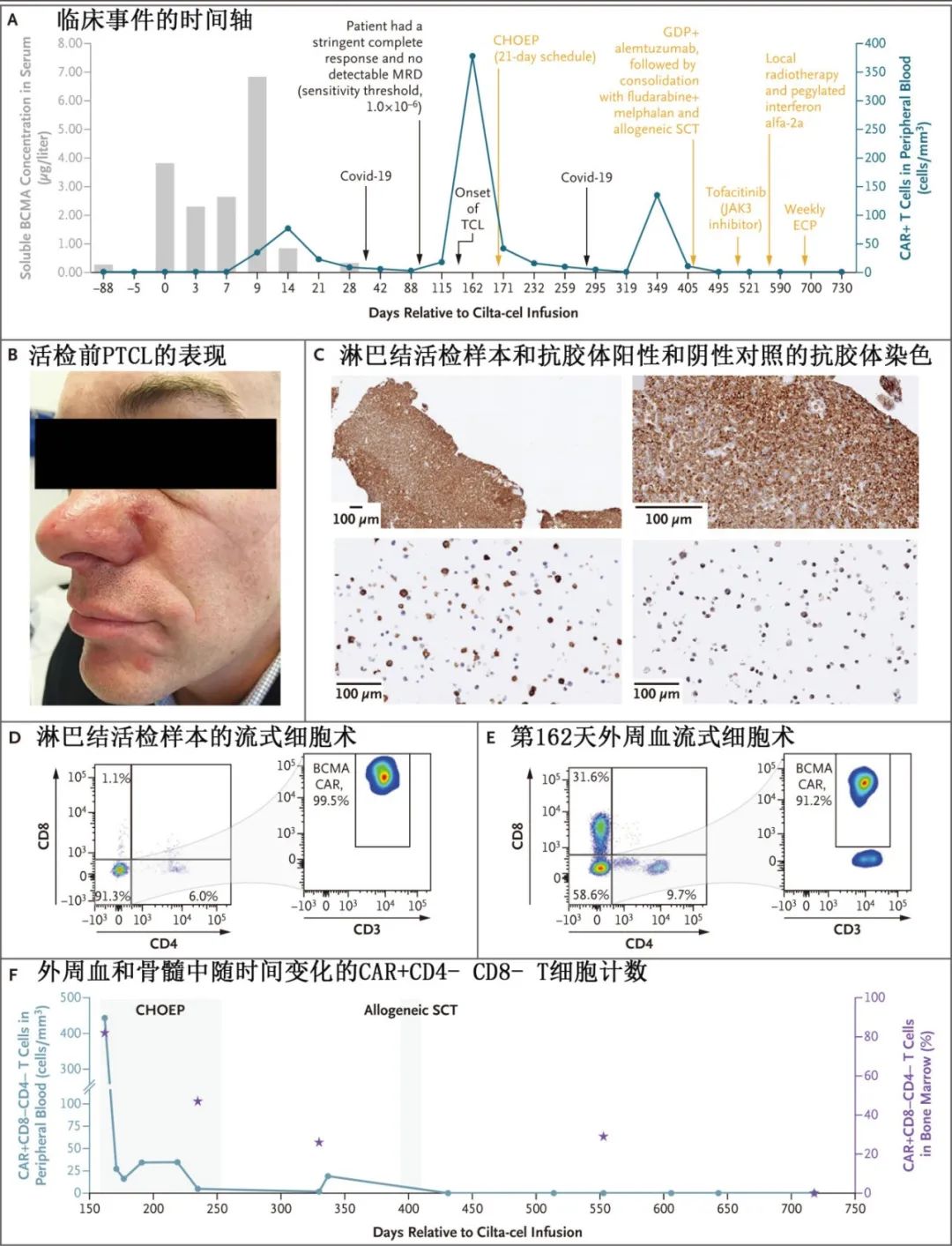
51岁男性,2019年12月被诊断为多发性骨髓瘤,具有高危细胞遗传学特征(del[17p]和gain[1q])。2021年11月加入CARTITUDE-4研究,接受cilta-cel治疗。治疗后,患者在血液中的CAR+ T细胞计数在第14天达到峰值(77个/立方毫米),随后在第92天降至3个/立方毫米。患者在治疗后2年内保持严格意义的完全缓解(sCR)和微小残留病(MRD)阴性状态。
但在治疗后5个月,患者出现快速生长的红斑性鼻面部斑块,活检显示为PTCL-NOS,且CAR转基因表达和整合阳性。基因分析显示,患者的T细胞受体β链(TCRβ)序列中存在TET2基因的错义变异(H1416R),且在治疗前样本中也检测到该变异。患者接受了多种治疗,包括化疗、异基因造血干细胞移植等,最终在2024年4月停止治疗,目前无临床或影像学疾病证据。
患者2
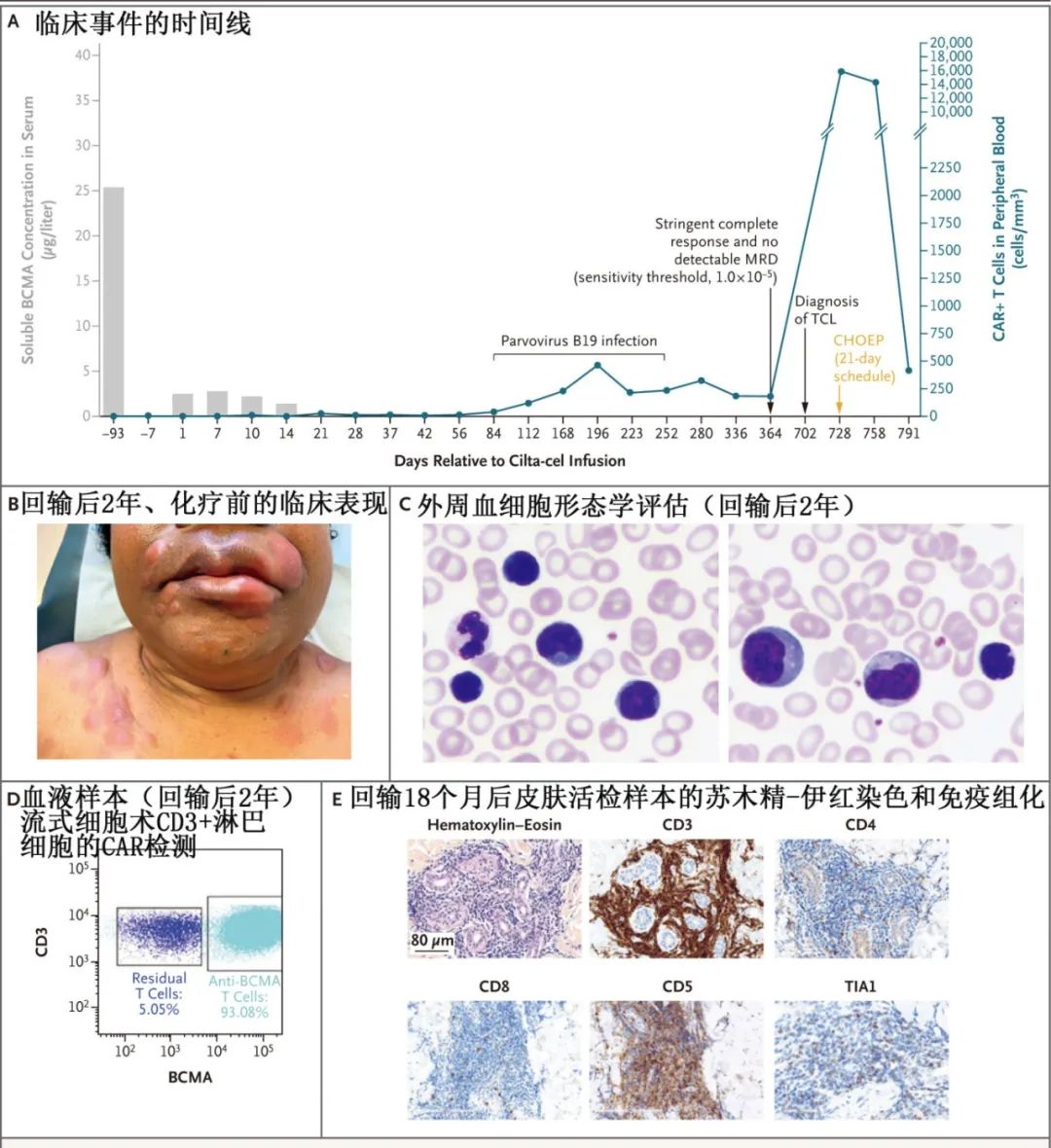
54岁女性,2019年11月诊断为IgG kappa型多发性骨髓瘤,具有高危细胞遗传学特征(t[4;14]和gain[1q])。2021年10月加入CARTITUDE-4研究,接受cilta-cel治疗。治疗后,患者在第21天血液中的CAR+ T细胞计数为29个/立方毫米,第42天为8个/立方毫米。患者在治疗后2年内保持sCR和MRD阴性状态。
但在治疗后16个月,患者出现面部、躯干和乳房的皮肤肿块,最终诊断为PTCL-NOS,且CAR转基因表达和整合阳性。基因分析显示,患者的T细胞中存在TET2基因的错义变异(Y1902H),且在治疗前的样本中也检测到该变异。患者接受了化疗和异基因造血干细胞移植,目前处于完全代谢缓解状态。
总结
两例患者在接受cilta-cel治疗后出现CAR转基因T细胞淋巴增殖性肿瘤(CAR transgenic T-cell lymphoproliferative neoplasm,CTTLN),这是一种罕见但具有临床侵袭性的疾病。两病例的共同特征包括皮肤受累、TET2基因的预测失功能变异,以及在治疗前就可检测到的低水平TET2突变克隆性造血。两例患者在CAR-T细胞治疗前均有病毒感染史,且接受过与第二原发恶性肿瘤风险增加相关的治疗。研究未能明确CAR转座插入突变是否对T细胞淋巴瘤的发展有直接贡献。
此外,2月5日另一篇报道中,一例患者接受cilta-cel治疗后,CAR被插入到抑癌基因TP53中,引起CAR阳性T细胞淋巴瘤【2】。
CAR-T细胞疗法治疗多发性骨髓瘤的效果显著,获益远大于风险,但也应保持对继发T细胞淋巴瘤的警惕性,并建议对所有接受CAR-T细胞治疗的患者进行第二肿瘤的终身监测。
参考文献
1.Harrison SJ, et al. CAR+ T-Cell Lymphoma after Cilta-cel Therapy for Relapsed or Refractory Myeloma.N Engl J Med . 2025 Feb 13;392(7):677-685. doi: 10.1056/NEJMoa2309728.
2.Perica, Karlo et al. “CD4+ T-Cell Lymphoma Harboring a Chimeric Antigen Receptor Integration in TP53.” The New England journal of medicine vol. 392,6 (2025): 577-583. doi:10.1056/NEJMoa2411507.


