Eur Heart J 陶辉/赵健元/张野教授团队发现线粒体铜耗竭促进心肌纤维化的表观遗传互作机制
时间:2025-03-11 12:08:32 热度:37.1℃ 作者:网络
心肌纤维化(Cardiac fibrosis, CF)作为多种心血管疾病的终末病理转归,其特征性表现为心脏成纤维细胞的异常活化、迁移及过量细胞外基质(尤其是I/III型胶原)的异常沉积。临床常见的心房颤动、心力衰竭、心肌梗死等疾病进程中,心肌细胞器(包括线粒体、质膜、收缩装置及肌浆网)的级联性损伤,将导致心肌收缩-舒张功能障碍的恶性循环,最终进展为终末期心脏病。值得注意的是,尽管全球CF疾病负担持续攀升,仍鲜有能持久缓解疾病的治疗方案,这凸显了深入解析CF分子机制并开发新型治疗靶点的迫切需求。
在治疗困境下,危险因素的精准解析尤为重要。流行病学证据显示,遗传易感性与环境暴露(尤其是重金属暴露)的交互作用显著增加CF及相关心血管事件风险。其中,铜、铁、锌、铅、镉和锰等普遍存在的环境金属污染物,即使在亚毒性浓度下仍可能通过表观遗传调控等途径产生显著的生物学效应。
铜作为必需微量金属元素,通过参与细胞色素C氧化酶(COX)、超氧化物歧化酶(SOD)等关键酶的结构形成与功能调控,在维持线粒体氧化磷酸化、氧化还原稳态及铁代谢平衡中发挥核心作用。近年研究发现,细胞内铜稳态失衡与糖尿病性心肌病等疾病的病理进程密切相关。特别值得注意的是,过量铜蓄积可通过破坏呼吸链酶复合体(如复合体IV)的结构完整性,导致质子梯度异常和线粒体膜电位崩解,进而诱发能量代谢危机。引人注目的是,铜缺乏同样会引发显著的代谢重编程。肿瘤学研究表明,铜耗竭的恶性细胞会通过Warburg效应转向糖酵解主导的能量代谢模式。由于活化态成纤维细胞与肿瘤细胞在异常糖酵解活性和增殖特性方面具有显著相似性,这提示我们:铜代谢紊乱可能通过调控线粒体-糖酵解代谢平衡影响成纤维细胞的生物学行为,但其潜在的机制还需要进一步的研究。
2025年3月6日,安徽医科大学第二附属医院/上海交通大学医学院附属新华医院的陶辉教授、赵健元教授、张野教授在心血管领域顶级期刊European Heart Journal 《欧洲心脏杂志》在线发表了题为“SLC31A1 loss depletes mitochondrial copper and promotes cardiac fibrosis”的研究论文。该研究发现一种新的表观遗传机制,其通过影响铜转运蛋白SLC31A1的表达水平导致线粒体铜耗竭,进而促进氧化磷酸化向糖酵解的转变,引起心脏成纤维细胞的活化,最终介导心脏纤维化的发生和发展,该研究结果为制定心肌纤维化的预防措施提供了新的见解。

研究团队构建了异丙肾上腺素(ISO)和血管紧张素II (Ang II)诱导的小鼠心肌纤维化模型,发现纤维化心脏组织中铜离子浓度显著降低,且铜转运蛋白SLC31A1表达下调。线粒体铜耗竭通过抑制氧化磷酸化、增强糖酵解,促进成纤维细胞增殖及胶原沉积。

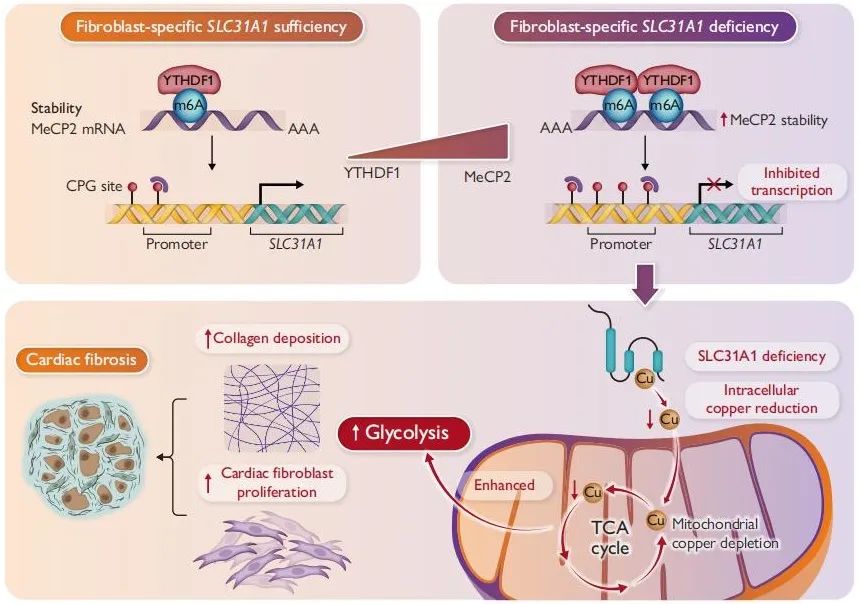
MeCP2通过识别SLC31A1启动子区甲基化CpG岛抑制其转录,而YTHDF1通过m6A修饰增强MeCP2 mRNA的稳定性,形成“YTHDF1-MeCP2-SLC31A1”调控轴。靶向敲低YTHDF1或MeCP2可逆转SLC31A1抑制,改善线粒体铜稳态并减轻纤维化。
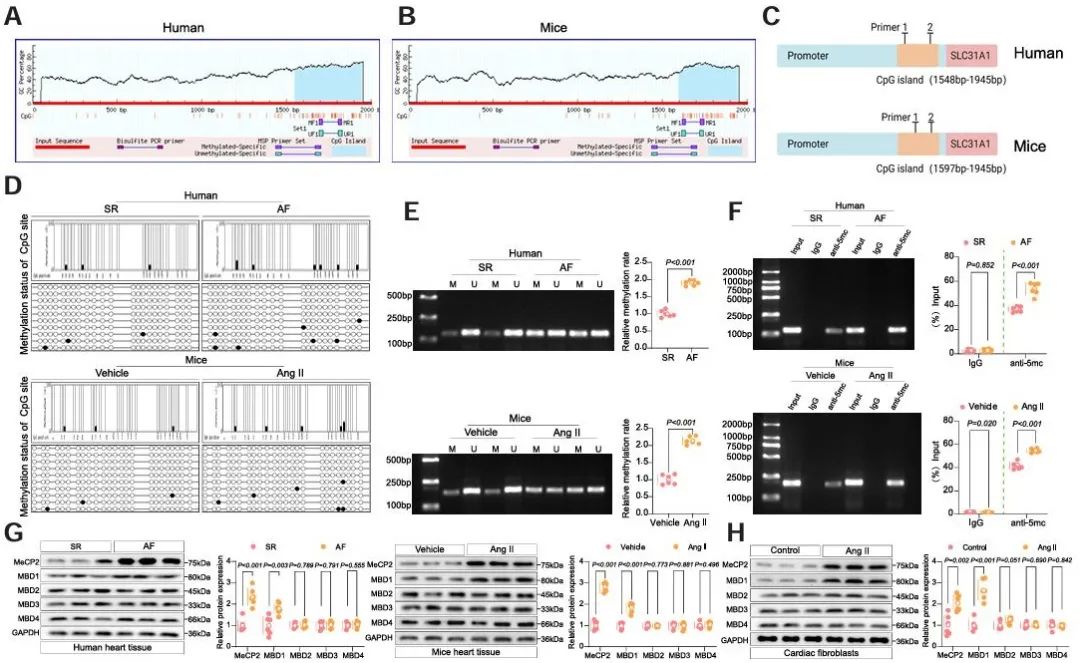
在房颤(AF)和糖尿病心肌病(DCM)患者的心脏组织中,SLC31A1表达显著降低,YTHDF1和MeCP2水平升高,且线粒体铜含量减少。铜螯合剂四硫钼酸盐(TM)加剧纤维化,而过表达SLC31A1或抑制YTHDF1/MeCP2可有效缓解病理表型。
综上,本研究揭示了表观遗传机制调控铜代谢异常导致心肌纤维化的分子路径,为靶向YTHDF1-MeCP2-SLC31A1信号轴的治疗策略提供了理论依据。未来可通过小分子药物或基因编辑技术干预该通路,为逆转心脏重构开辟新方向。
安徽医科大学第二附属医院/上海交通大学医学院附属新华医院研究生涂彬、宋凯及周泽宇为本文第一作者,安徽医科大学第二附属医院/上海交通大学医学院附属新华医院的陶辉教授、赵健元教授、张野教授为通讯作者。
参考文献:
1.Bin Tu, Kai Song, Ze-Yu Zhou, Li-Chan Lin, Zhi-Yan Liu, He Sun, Yang Zhou, Ji-Ming Sha, Yan Shi, Jing-Jing Yang, Ye Zhang, Jian-Yuan Zhao, and Hui Tao, SLC31A1 loss depletes mitochondrial copper and promotes cardiac fibrosis, European Heart Journal (2025) 00, 1–17, https://doi.org/10.1093/eurheartj/ehaf130
2.He Sun, Kai Song, Ze-Yu Zhou, Bin Tu, Yang Zhou, Li-Chan Lin, Zhi-Yan Liu, Zhen-Yu Liu, Ji-Ming Sha, Yan Shi, Jing-Jing Yang, Dong Lu, Jian-Yuan Zhao, Hui Tao,Cirrhosis Promotes Cardiac Fibrosis Development by Inhibiting Notch1 in Cardiac Fibroblasts,JACC: Basic to Translational Science,2025,https://doi.org/10.1016/j.jacbts.2024.11.015.
3. Ding JF, Tu B, Song K, Liu ZY, Lin LC, Liu ZY, Shi Y, Yang JJ, Zhao JY, Tao H. Epitranscriptomic regulation of cardiac fibrosis via YTHDF1-dependent PIEZO2 mRNA m6A modification. Cardiovasc Res. 2024:cvae239.
4. Lin LC, Liu ZY, Yang JJ, Zhao JY, Tao H. Lipid metabolism reprogramming in cardiac fibrosis. Trends Endocrinol Metab. 2024 Feb;35(2):164-175.
5. Liu ZY, Lin LC, Liu ZY, Song K, Tu B, Sun H, Zhou Y, Mao S, Zhang Y, Li R, Yang JJ, Zhao JY, Tao H. N6-Methyladenosine-mediated phase separation suppresses NOTCH1 expression and promotes mitochondrial fission in diabetic cardiac fibrosis. Cardiovasc Diabetol. 2024 Sep 28;23(1):347.
6. Wang J, Zhao R, Xu S, Zhou XY, Cai K, Chen YL, Zhou ZY, Sun X, Shi Y, Wang F, Gui YH, Tao H, Zhao JY. NOTCH1 mitochondria localization during heart development promotes mitochondrial metabolism and the endothelial-to-mesenchymal transition in mice. Nat Commun. 2024 Nov 16;15(1):9945.
原文链接:
https://doi.org/10.1093/eurheartj/ehaf130


