Cancer Res:暨南大学邹畅/王继刚合作研究发现SNHG17通过激活线粒体DNA转录重编程乳腺癌的能量代谢
时间:2025-04-04 12:08:52 热度:37.1℃ 作者:网络
在多数固体肿瘤中,细胞能量代谢主要受有氧糖酵解支配,这种方式以满足生物大分子的高需求为代价,降低了ATP的生产效率。阐明快速增殖的恶性细胞在这种糖酵解产生ATP效率低下的状态下如何获取充足能量的机制,有望推动针对代谢的治疗策略的发展。
2025年3月14日,暨南大学邹畅和王继刚共同通讯在Cancer Research在线发表题为“SNHG17 Reprograms Energy Metabolism of Breast Cancer by Activating Mitochondrial DNA Transcription”的研究论文。该研究观察到长非编码RNA小核RNA宿主基因17(SNHG17)的表达水平升高与乳腺癌的不良预后之间存在显著关联。SNHG17通过增强线粒体ATP的产生来促进乳腺癌细胞的增殖。
从机制上讲,SNHG17直接与NF-κB的P65亚基相互作用,并在苏氨酸505位点使P65发生磷酸化。SNHG17在其截断的loop2位点与P65结合,将P65募集到线粒体,并共同调节线粒体DNA的转录激活,以促进ATP的产生。因此,使用反义寡核苷酸靶向SNHG17可显著减少乳腺癌肿瘤在体外和体内的生长。总体而言,这些结果证实了SNHG17通过增加ATP产生在促进乳腺癌进展中的作用,并为固体肿瘤中能量代谢的重编程提供了见解。

为适应具有挑战性的肿瘤微环境,快速增殖的癌细胞发展出了一种机制,即使在有氧的情况下也能通过糖酵解高效地利用葡萄糖,这被称为有氧糖酵解或瓦氏效应。这种重新编程的能量代谢满足了生物合成过程中对大量生物大分子的需求,尽管这以降低ATP生产效率为代价。ATP对细胞活力的重要性已得到广泛认可。在肿瘤细胞的增殖和侵袭过程中,对ATP的需求不断上升。然而,癌细胞如何依赖有氧糖酵解来维持足够的ATP供应,其机制至今仍不清楚。
氧化磷酸化(OXPHOS)和有氧糖酵解都是细胞能量代谢中的两个关键组成部分。这两个过程之间的微妙平衡对细胞的存活至关重要。越来越多的证据表明,长非编码RNA(lncRNA)参与了癌细胞内的葡萄糖代谢。具体而言,GLCC1通过抑制c-Myc泛素化来促进葡萄糖糖酵解和细胞增殖,同时还促进结直肠癌中的乳酸产生。YAP通过靶向BCAR4促进BCa的糖酵解。糖酵解过程导致乳酸的释放,随后增强lncRNA HIFAL的表达。因此,HIFAL抑制PHD2与HIF-1α之间的相互作用,从而防止BCa细胞中HIF-1α的羟基化和降解。此外,观察到HIFAL通过反式激活HIF-1α增强BCa细胞中的糖酵解。
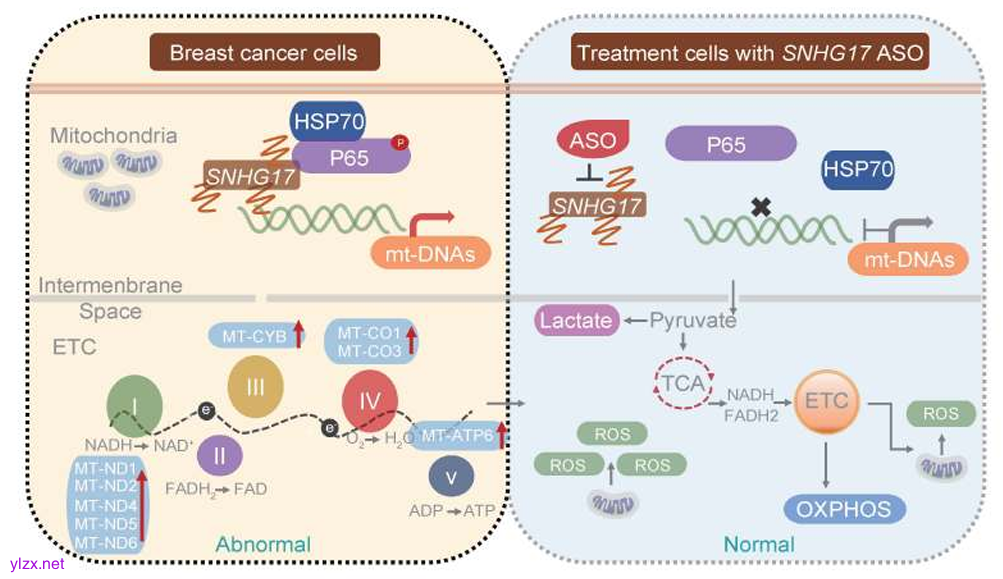
模式机理图(图片源自Cancer Research)
最近,新兴的研究揭示了小核RNA宿主基因(SNHGs)在协调癌细胞存活和进展中的关键作用。现有证据表明,小核仁RNA宿主基因(SNHGs)在癌症细胞存活的启动和操作中起着关键作用。Lin等人发现,SNHG5作为肿瘤抑制因子,在调节细胞能量稳态中发挥着至关重要的作用。他们还报告说,SNHG6通过激活胆固醇诱导的mTORC1途径,触发非酒精性脂肪肝向肝癌的进展。小核仁RNA宿主基因17(SNHG17)已成为致癌作用中的新型参与者,发挥显著的致癌作用。SNHG17在肺癌中通过促进细胞增殖和迁移、调节结直肠癌中CXCL12介导的血管生成以及通过靶向星形细胞瘤中的miR-875-5p/ERLN2来驱动细胞恶性转化,从而在细胞发育中发挥关键作用。此外,它可以通过调节食管鳞状细胞癌中的miR-338-3p/SOX4途径来增强细胞侵袭能力。在大多数癌症中,糖酵解的调节主要由致癌驱动因素决定,而不是线粒体呼吸复合物。然而,SNHG17如何调节BCa中癌细胞的能量代谢仍然不清楚。
线粒体DNA(mt-DNAs)是小的环状DNA,编码13种线粒体蛋白质,这些蛋白质通过复合物I、II、III、IV和V参与质子向膜间隙的转移。复合物V专门促进ADP和Pi生成ATP。此外,某些类型的癌症已经证明,通过调节高水平的OXPHOS,能量代谢的动态平衡被重新编程,这是由ATP产生控制的。mt-DNAs拷贝数的扩增与各种类型的癌症密切相关。例如,mt-DNAs的高表达有助于微卫星稳定型结肠癌细胞的转移。癌症治疗领域最近对探索线粒体代谢的潜力越来越感兴趣。此外,ATP可以通过mt-DNAs合成的线粒体呼吸复合物生成,并保持氧化还原平衡。当细胞内OXPHOS受到抑制时,细胞外应激和细胞内代谢途径都可以通过补偿性氧化ATP产生来调节对OXPHOS抑制的反应。然而,lncRNA调节对BCa中mt-DNAs表达的影响及其对能量代谢的影响在很大程度上尚未探索。
转录因子的参与对于mt-DNAs的转录过程是必不可少的。最近的研究证实,线粒体转录因子A(TFAM)是一种在细胞核中编码的蛋白质,对mt-DNAs具有序列特异性和非特异性结合亲和力。TFAM特异性结合到mt-DNAs的启动子区域,激活线粒体转录。此外,它在基因组凝聚中自主发挥作用。目前,关于线粒体内转录因子的调节研究有限。几项研究表明,热休克蛋白(HSPs)作为分子伴侣,有助于多肽的正确折叠,同时防止错误折叠的蛋白质聚集或沉淀。线粒体Hsp70(mt-HSP70,Mortalin,Grp75)作为HSP70家族中的应激伴侣蛋白,是基于其与其他成员的重要同源性而分类的。Mt-HSP70通过底物的结合和释放以循环方式促进蛋白质转运。在癌细胞中,mt-HSP70蛋白与抑癌蛋白p53在细胞核附近共定位,并且其与P65的相互作用有助于P65向线粒体的转运,从而调节OXPHOS。然而,这种行为调节线粒体DNA的具体机制尚不清楚。
在本研究中,作者发现SNHG17在BCa中上调。此外,SNHG17通过反式激活mt-DNAs的表达来增强ATP的产生、提高ATP/ADP比率并维持细胞存活。SNHG17在苏氨酸505(Thr 505)位点磷酸化P65,有助于增强BCa细胞的代谢重编程。使用反义寡核苷酸(ASO)靶向SNHG17可有效抑制BCa肿瘤的生长。因此,作者的研究结果表明,SNHG17在调节以糖酵解为主的癌细胞中的ATP水平方面发挥着至关重要的作用,这突显了靶向SNHG17作为治疗BCa的创新治疗策略的潜力。
原文链接:
https://doi.org/10.1158/0008-5472.CAN-24-1271


