Am J Clin Nutr:DHA摄入或对AD高遗传风险者有益
时间:2021-04-11 22:01:30 热度:37.1℃ 作者:网络
阿尔茨海默病(AD)造成巨大的社会经济负担。鉴于目前还没有批准的治疗阿尔茨海默病的疾病修正药物,预防策略至关重要。有大量的观察证据表明,经常食用富含脂肪的鱼类对认知有好处,这是DHA的主要饮食来源(22:6n-3)。这种脂肪酸对大脑功能至关重要,可以改善阿尔茨海默病的特征。膳食摄入DHA是否与认知功能下降和阿尔茨海默病有关,目前仍在争论中。APOE-ε4等位基因的数量是散发性阿尔茨海默病(AD)的主要不可改变的危险因素。有越来越多的证据表明,在AD症状出现之前,饮食中服用DHA(22:6n-3)的益处,特别是在APOE-ε4携带者中。临床前阶段的脑改变可以通过结构磁共振检测出来。鉴于越来越多的证据表明APOE-ε4负荷是AD临床前阶段大脑易损性的一个因素,Sala-Vila A等在认知正常、AD风险增加的中年人群中,横断面研究膳食中DHA摄入量是否与认知功能、脑小血管疾病和AD相关神经变性的磁共振标志物有关,并探讨APOE-ε4状态对其影响。并在Am J Clin Nutr杂志发表文章。

为了确定这一点,评估了自我报告的DHA饮食摄入量,并在APOE-ε4携带者(n=122,非携带者;n=157,1个等位基因;n=61,2个等位基因)丰富的人群中,寻找与神经心理测试(情景记忆和执行功能)、脑小血管疾病的磁共振标志物(WMHs和CMBs)以及早期AD相关神经变性(AD易损区的皮质厚度)的相关性。
在阿尔茨海默病(阿尔茨海默病和家系)研究的340名受试者中,通过FFQ评估APOE-ε4携带者(n=122,非携带者;n=157,1个等位基因;n=61,2个等位基因)的自我报告的DHA摄入量。通过进行情景记忆和执行功能测试来衡量认知表现。进行了高分辨率结构磁共振成像,以评估脑小血管疾病[白质高信号(WMHs)和脑微出血(CMBs)]和AD相关性脑萎缩(AD征象中的皮质厚度)。构建了调整了潜在混杂因素的回归模型,探索了DHA×APOE-ε4的交互作用。
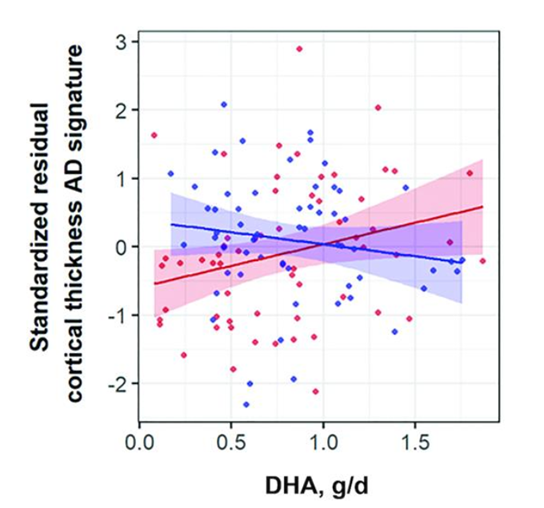
AD自我报告的DHA饮食摄入量与皮质厚度的标准化残留物之间关系的散点图。从包括性别、年龄、体重指数、高胆固醇血症、高血压、能量摄入量和α-亚麻酸摄入量在内的一般线性模型中输出,在APOE-ε4纯合子(n=59,红色)和非纯合子(n=59,蓝色,n=59)中。DHA×APOE-ε4相互作用的p=0.025。APOE-ε4纯合子的Pearson相关系数=-0.151(P=0.253),配对的非纯合子的Pearson相关系数=0.267(P=0.041)。
该研究没有观察到DHA与认知表现或WMH负荷之间的显著关联。观察到DHA与脑叶CMBs的患病率之间非显著的负相关(OR:0.446;95%CI:0.195,1.018;P=0.055)。在纯合子中,DHA与AD信号中较大的皮质厚度显著相关,而在非纯合子中则不显著(P-交互作用=0.045)。当分析风险因素匹配的纯合子和非纯合子时,这种关联加强了。
该研究的结果有三个方面值得强调。首先,尽管关于饮食(包括营养素、食物和饮食模式)和核磁共振评估的AD标志物的研究越来越多,但该研究以检查APOE-ε4如何在临床前阶段调节饮食DHA和结构性AD特征之间的关联。其次,该研究描述了仅在APOE-ε4纯合子中对DHA有利的关联。APOE-ε4纯合子的高患病率提供了前所未有的统计能力来测试不同的遗传外显性模型,这可能捕捉到不同水平的易患阿尔茨海默病的风险等位基因的易感性。第三,该研究结果强化了这样的假设,即这些遗传弱势群体可能从与饮食DHA相关的干预中获益最多。
总之,在散发性AD遗传风险增加的中年认知正常个体中,自我报告的膳食DHA被发现与几种有益的脑血管病理或AD相关神经变性相关的脑神经成像表型有关。需要进一步的研究来探索干预措施的有效性,包括在AD的临床前阶段补充这种脂肪酸,特别是在疾病的高危人群中。
原文出处
Sala-Vila A, Arenaza-Urquijo EM, Sánchez-Benavides G, et al. DHA intake relates to better cerebrovascular and neurodegeneration neuroimaging phenotypes in middle-aged adults at increased genetic risk of Alzheimer disease [published online ahead of print, 2021 Mar 18]. Am J Clin Nutr. 2021;nqab016. doi:10.1093/ajcn/nqab016


