阿斯利康称其抗体疗法AZD7442预防有症状新冠肺炎效果未达主要目标
时间:2021-06-15 23:02:06 热度:37.1℃ 作者:网络

阿斯利康 (AstraZeneca) 周二表示,一项名为STORM CHASER 后期临床试验未能提供证据证明其新冠抗体疗法可以保护与感染者接触过的人免受该疾病的影响,这是其寻找疫苗替代品的努力中的一个小挫折。该研究评估了这种由两种抗体混合而成的疗法是否可以防止在过去八天内接触过该病毒的成年人出现新冠症状。
AZD7442 在试验中耐受性良好。 初步分析显示安慰剂组和治疗组中出现类似的不良事件,STORM CHASER 的完整结果将提交在同行评审的医学期刊上发表,并在即将召开的医学会议上公布
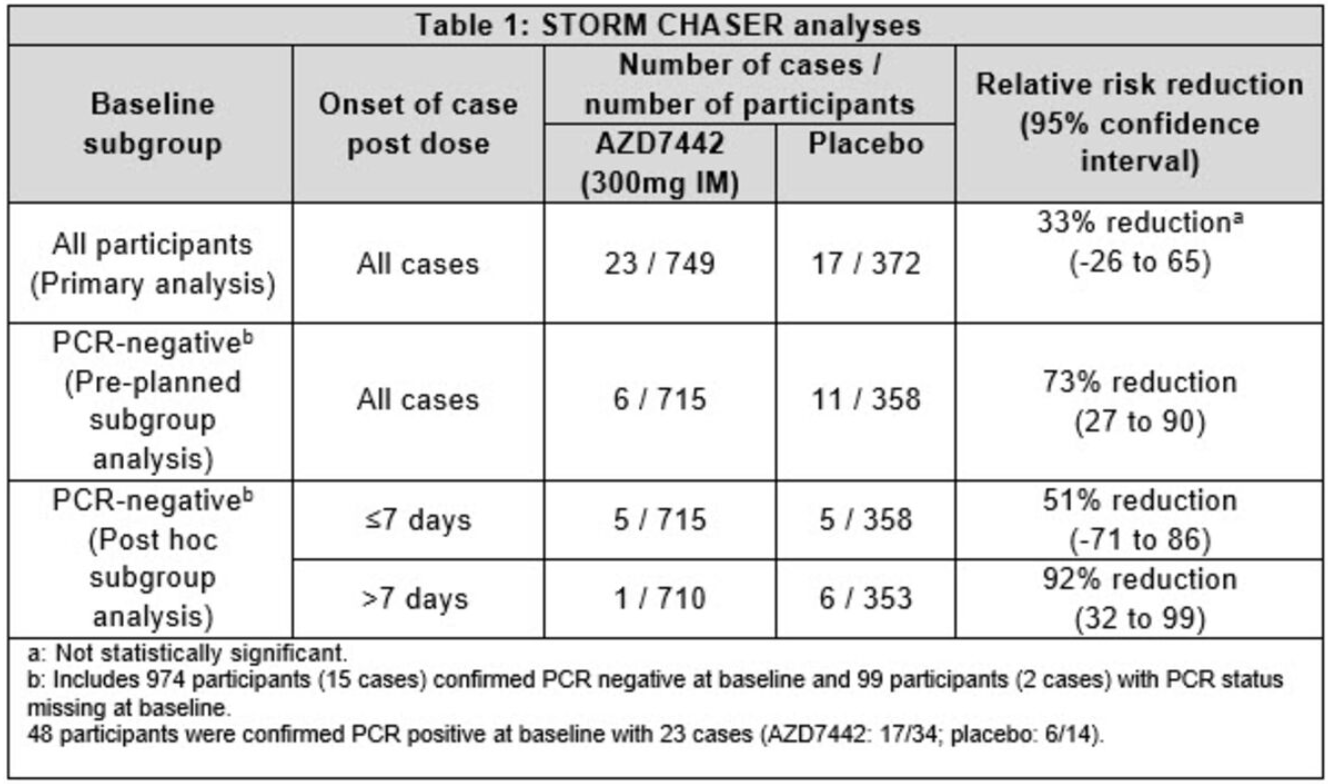
与安慰剂相比,AZD7442 疗法在降低人们出现症状的风险方面的有效率为 33%,但该结果在统计上并不显著。尚未经过同行评审的 III 期研究包括来自英国和美国的1121 名参与者。绝大多数(尽管不是全部)在试验开始时没有感染病毒。一开始没有被感染的一部分参与者的结果更令人鼓舞,但主要分析依赖于所有参与者的结果。
阿斯利康执行副总裁 Mene Pangalos 在一份声明中说:“虽然这项试验没有达到针对症状性疾病的主要终点,但我们对 PCR 阴性参与者在接受 AZD7442 治疗后所看到的保护感到鼓舞。”
该公司正依靠进一步的研究来重振该产品的命运。还有五项试验正在进行中,以测试抗体鸡尾酒作为治疗或预防。下一个可能来自一项更大的试验,在因癌症或器官移植而免疫系统减弱的人群中测试该产品,这些人群可能无法从疫苗中受益。
AZD7442 属于一类称为单克隆抗体的药物,它能模仿人体产生的天然抗体来抵抗感染。是两种 LAAB 的组合——tixagevimab (AZD8895) 和 cilgavimab (AZD1061)——来源于 SARS-CoV-2 病毒感染后恢复期患者捐赠的 B 细胞。由范德比尔特大学医学中心发现并于 2020 年 6 月授权给阿斯利康,人类单克隆抗体与 SARS-CoV-2 刺突蛋白 2 上的不同位点结合,并由阿斯利康优化,延长半衰期并减少 Fc 受体结合。与传统抗体相比,半衰期延长使其作用的持久性大约增加了三倍,并且在单次给药后可以提供 6 到 12 个月的 COVID-19 保护。减少的 Fc 受体结合旨在最大限度地降低抗体-疾病的依赖性增强——一种病毒特异性抗体促进而不是抑制感染和/或疾病的现象。
AZD7442 目前正在另外几项 COVID-19 预防和治疗试验中进行测试: PROVENT8 III 期试验,涉及 5,000 多名暴露前预防参与者; TACKLE COVID-199 III 期门诊治疗试验;和合作者在门诊和住院环境中进行的治疗试验。 AZD7442 正在 IM 和静脉内给药途径中进行评估。
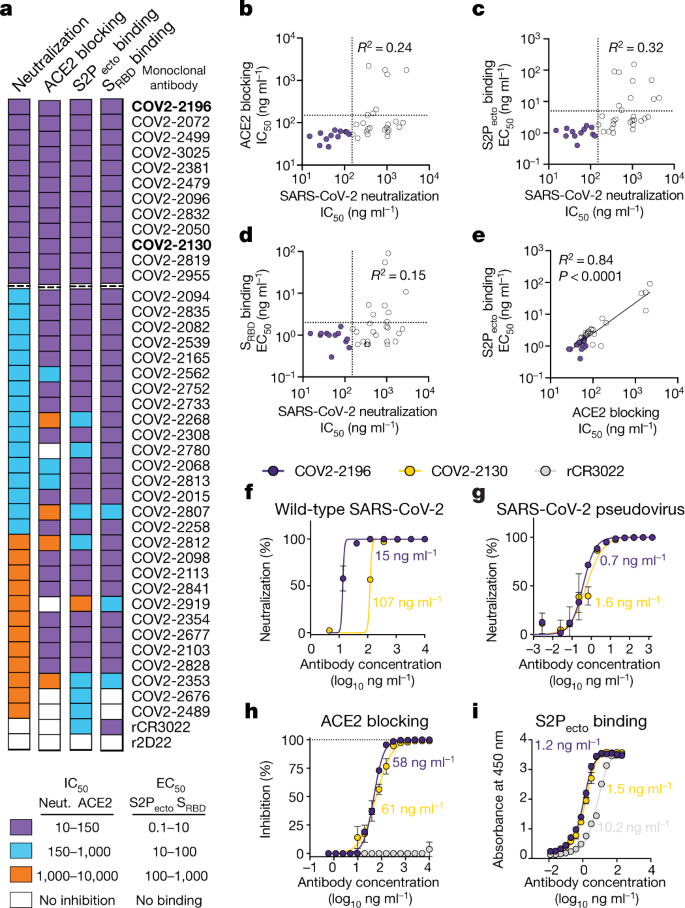
Potently neutralizing and protective human antibodies against SARS-CoV-2
牛津大学和哥伦比亚大学研究人员的初步“体外”发现也表明 AZD7442 中和了最近出现的 SARS-CoV-2 病毒变体。2020 年 7 月发表在《自然》杂志上的数据表明,在临床前实验中,LAAB 能够阻断 SARS-CoV-2 病毒与宿主细胞的结合,并在细胞和疾病动物模型中防止感染。
根据与范德比尔特的许可协议条款,阿斯利康将按未来净销售额支付个位数的特许权使用费。由竞争对手 Regeneron 和 Eli Lilly 开发的类似疗法已获得美国监管机构的批准,用于治疗未住院的新冠患者。
欧洲监管机构还批准了 Regeneron 的疗法,并正在审查由合作伙伴葛兰素史克和 Vir Biotechnology 以及礼来和 Celltrion 开发的疗法。Regeneron 还寻求美国对其作为预防性治疗的疗法的授权。
但阿斯利康的结果对制药业来说是一个小小的打击,因为它试图找到更有针对性的新冠接种替代品,特别是对于可能无法接种疫苗或对接种反应不足的人。它也在开发新的治疗方法并重新利用现有药物来对抗这种病毒。
AZD7442 正在美国政府的支持下开发。阿斯利康在 3 月份宣布与美国政府达成协议,提供多达 50 万剂 AZD7442。 该公司周二表示,目前正在与美国政府就该交易的后续步骤进行谈判。它正在与美国政府就一项 2.05 亿美元的交易“下一步”进行谈判,以供应多达 50 万剂 AZD7442。与瑞士制造商 Lonza签约生产 AZD7442。
该公司表示,完整的结果将提交在同行评审的医学期刊上发表。
参考资料:
Potently neutralizing and protective human antibodies against SARS-CoV-2,https://www.nature.com/articles/s41586-020-2548-6.pdf
https://www.astrazeneca.com/media-centre/press-releases/2021/update-on-azd7442-storm-chaser-trial.html


