Science:神奇“变瘦分子”被发现,可以直接从皮肤中流走油脂!
时间:2021-08-09 12:01:20 热度:37.1℃ 作者:网络
皮肤出油应该是皮脂溢出的问题,常常发生在皮脂腺丰富的区域,皮肤的皮脂腺分泌大量的皮脂,通过皮脂腺毛囊通路到达皮肤表面而滋润皮肤。事实上,如果真能把人的脂肪从皮肤中“流出”来,那也真是件好事!这样就真能实现懒人减肥了,不运动就减肥。
这样的“天方夜谭”最近还真被科学家发现了。
7月30日,权威期刊Science上发表了最新研究进展,科学家发现有一种叫作胸腺基质淋巴细胞生成素(TSLP)的细胞因子可以显著降低小鼠的体重和白色脂肪含量。短短28天,小鼠的体重从45克降低到了25克,足足轻了40%!
意外的副作用TSLP是一种由皮肤或肺部上皮细胞产生的细胞因子,可作用于多种免疫细胞。目前TSLP多应用在哮喘及其他过敏性疾病药物的研发中。
在2012年,一批科学家发现TSLP介导癌细胞和免疫系统之间的交叉对话。肿瘤细胞或癌症相关成纤维细胞产生了TSLP,而TSLP又促进了未成熟树突状细胞(iDC)的成熟,并通过单核细胞来源的树突状细胞(MoDC)促进了CCL17、CCL22及OX40配体的产生。这些细胞因子吸引原始T细胞和调节性T(Treg)细胞,而OX40配体诱导了炎性Th2细胞的极化。Th2细胞产生的炎性细胞因子(IL-13、IL-4、TNF-α)诱导了巨噬细胞向M2型肿瘤相关巨噬细胞(M2-TAM)的极化。M2-TAM 分泌的EGF和TGF-β以及Th2细胞产生的IL-13促进了肿瘤建立和转移。
进一步发现TSLP有可能成为过敏治疗的靶标。
这项研究开始,研究人员的本意并非将TSLP用于研发“燃脂神药”,而是想探究它在激活2型免疫细胞和促进调节T细胞增殖中的作用。有研究表明,这两种细胞可对能量代谢产生调节作用。研究人员猜想,如果把TSLP用在超重的小鼠身上,就可以刺激小鼠的免疫反应,进而抵消肥胖带来的负面影响。
科学家们原本只是想知道TSLP是否会降低胰岛素抗性(一种糖尿病的危险因素),进而降低患2型糖尿病的风险。
令他们震惊的是,在小鼠体内连续四周注射病毒载体AAV以提高TSLP水平后,不仅高脂饮食(HFD)小鼠患糖尿病的风险降低了,而且体重也大幅下降了40%!
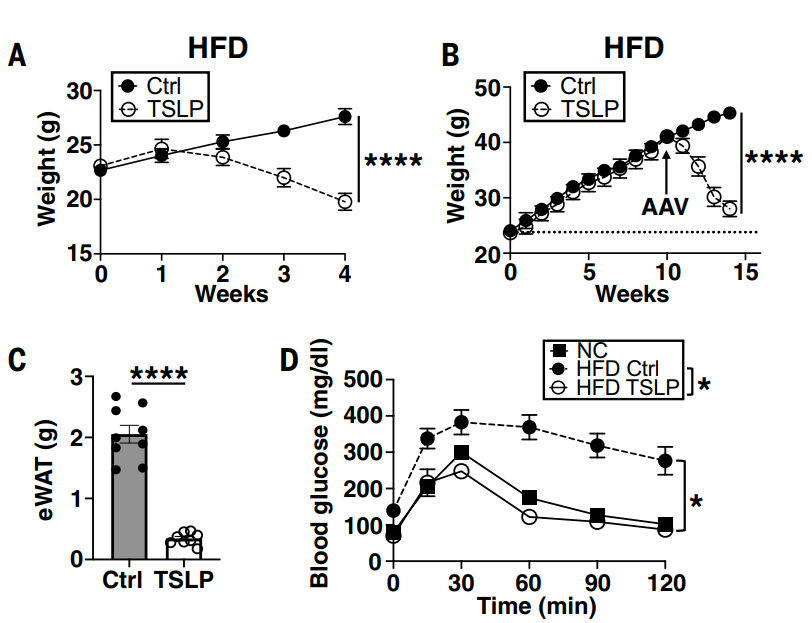 TLSP显著降低了小鼠的体重,白色脂肪和血糖含量也有所降低(来源:Science)
TLSP显著降低了小鼠的体重,白色脂肪和血糖含量也有所降低(来源:Science)
不仅如此,小鼠体内的白色脂肪含量也大大减少。白色脂肪是体内脂肪的主要储存形式,主要分布在内脏周围和皮下组织。白色脂肪的过度积累对人体有害,可能诱发2型糖尿病和脂肪肝等疾病。
小鼠是如何变瘦的?小鼠在28天里体重迅速下降,研究者首先怀疑TSLP有较大毒性,使小鼠的健康受损,食欲变差。但他们发现,TSLP实验组小鼠的进食量反而比对照组多了20%~30%。同时,体重下降也不是由于能量消耗更大或代谢更快引起的。
研究者回忆起实验时的一个小发现:TSLP实验组的小鼠毛发总是亮亮的,看起来油乎乎,一眼就能区分出来。难道体重大幅下降的玄机藏在小鼠的皮肤上?TSLP会使小鼠的皮肤“出油”吗?
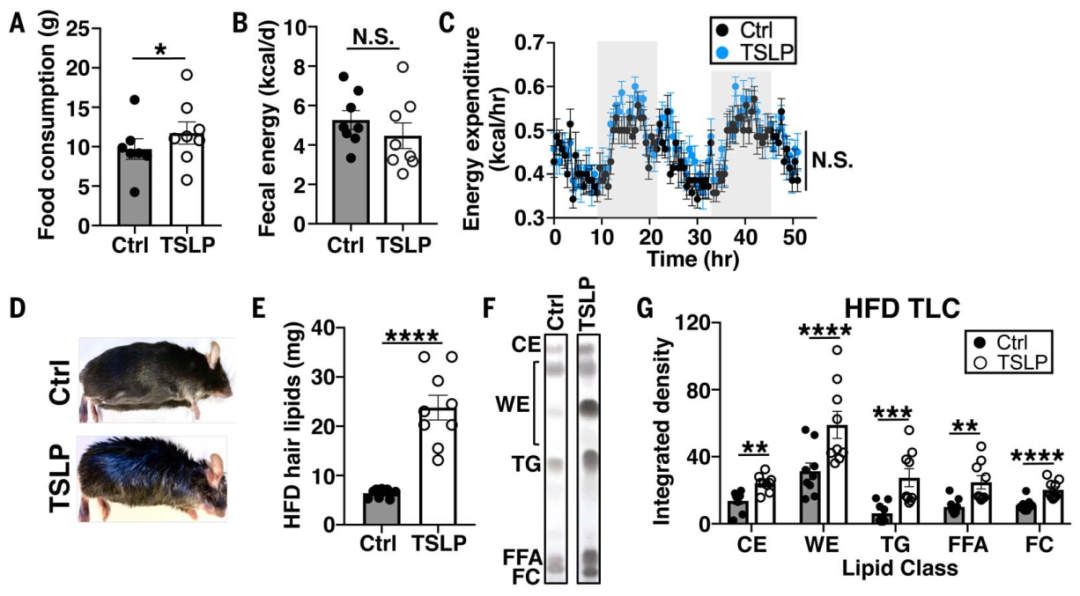 小鼠通过促进皮脂的分泌诱导脂肪流失(来源:Science)
小鼠通过促进皮脂的分泌诱导脂肪流失(来源:Science)
带着这个猜想,研究者剃光了两组小鼠的毛发,从它们的皮毛中提取油脂。他们发现,TSLP实验组亮亮的毛皮中含有皮脂特异性脂质。小鼠亮亮的毛发的确是皮脂腺“出油”了!
我们平时说的“出油”,其实是皮脂腺分泌出的油脂到了皮肤表面。别小看这层油脂,它是皮肤化学屏障的重要组成部分,可以发挥多重保护作用。现在看来,TSLP试验组小鼠正是通过皮脂腺把脂肪排出体外了。
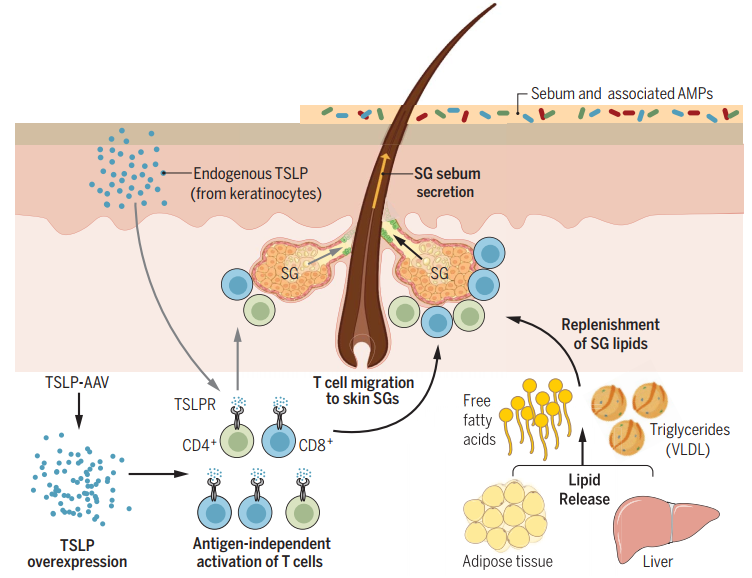
TSLP激活T细胞促进皮脂的分泌(来源:Science)
TSLP的过度表达造成T细胞的抗原非依赖性刺激。T细胞迁移到皮脂腺处促进皮脂的分泌。与此同时,脂肪组织和肝脏中的脂肪变为游离的脂肪酸,从皮脂腺处分泌到皮肤表面。这就解释了小鼠在TSLP治疗后的一系列变化。
然而,导致肥胖的因素多种多样,这种方法在人类身上是否同样可行仍具有不确定性。同时,安全性也是一个需要重点考虑的问题。皮脂的大量分泌可能会导致皮肤的炎症反应,造成痤疮的发生。并且人类和小鼠的免疫系统也有较大差异,可能需要更长时间的TSLP治疗才能获得预期效果。
关于TSLP的生物学特性
1.TSLP的结构:
TSLP主要由活化的肺和肠上皮细胞、角质形成细胞和成纤维细胞表达,树突状细胞(DC)、肥大细胞等免疫细胞也可生成。人TSLP是由三对链内二硫键连接形成的四螺旋束细胞因子,编码基因位于5q22.1染色体。人TSLP主要存在短型(sfTSLP)和长型(lfTSLP)两种同源异构体。sfTSLP与lfTSLP的末端区域有部分重叠。sfTSLP主要由60个氨基酸组成,常于健康状态表达并发挥稳态作用。lfTSLP编码159个氨基酸,分子量约14.9 kD,多于炎症时表达上调并发挥促炎作用 。健康者肠道和皮肤组织sfTSLP表达较lfTSLP显著增高。一旦经Toll样受体3(TLR3)、TLR2和TLR6配体及多种细胞因子[如肿瘤坏死因子α(TNF-α)、IL-4和IL-13]刺激,lfTSLP水平显著上调,而sfTSLP水平相仿。其实,未经刺激的上皮细胞lfTSLP组成性表达显著低于sfTSLP,而过敏原(变应原)刺激后lfTSLP水平显著升高。sfTSLP尚可抑制多种细胞因子(包括TNF-α、IL-1β、IL-6)的产生。sfTSLP可抑制TSLP信号传导并降低气道炎症和气道高反应性,lfTSLP则通过增加IFN-γ释放并激活TSLPR而介导炎症反应 。
2.TSLP受体:
TSLP与其特异性受体TSLPR及IL-7Rα结合,形成三元复合物,启动信号传导。比如,通过Janus激酶1(JAK1)、JAK2磷酸化,激活信号转导和转录因子(STAT)1、STAT3、STAT5,启动促炎信号,促进DC成熟和活化,诱导功能性Ⅱ型辅助性T细胞(Th2)、调节性T细胞(Treg)和滤泡辅助T细胞(Tfh)表达,调节皮肤、肺和肠道黏膜屏障的炎症过程。TSLPR缺陷小鼠Th2免疫较低,但Th1免疫正常甚或增强,提示TSLPR数量是影响过敏症发展的重要因素。
3.TSLP的生物学作用:
TSLP在抗原提呈细胞和造血细胞成熟中至关重要。TSLP分布于多种免疫细胞[包括DC、Ⅱ型固有淋巴细胞(ILC2)、T细胞、B细胞、自然杀伤T细胞(NKT)、Treg细胞、嗜酸粒细胞、中性粒细胞、肥大细胞和巨噬细胞]和非免疫细胞(血小板和感觉神经元)。TSLP通过形成TSLP-TSLPR-IL-7Rα复合体而作用于多种细胞系,特别是髓样DC。TSLP可激活人外周血CD11c + DC,上调主要组织相容性复合物(MHC)Ⅱ类、OX40配体(OX40L/CD134L,CD252)、CD54、CD80、CD83和CD86以及激活标记物DC-LAMP的表达,促进幼稚型CD4 + T细胞(Th0)分化为Th2细胞。
尤其,TSLP不能刺激髓系DC产生Th1极化细胞因子IL-12、促炎细胞因子TNF-α、IL-1β和IL-6,这是TSLP构建Th2免疫微环境的关键特征。TSLP-DC通过激活Th2效应记忆细胞并阻碍FOXP3 + Treg产生,增强Th2免疫应答。TSLP与CD4 + T细胞、CD8 + T细胞和Treg细胞交互作用,进一步促进Th2细胞增殖和活化 [ 6] 。TSLP尚可激活肥大细胞、固有淋巴细胞、上皮细胞、巨噬细胞等,协同IL-25、IL-33等上皮细胞趋化因子,共同促进Th2细胞因子(IL-4、IL-5和IL-13)生成。此外,TSLP可促进嗜酸粒细胞激活和趋化。TSLP以浓度依赖方式显著延缓嗜酸粒细胞凋亡,通过上调CD18和细胞间黏附因子1(ICAM1)表达、下调L-选择素,诱导IL-6和趋化因子CXCL8、CXCL1生成,导致嗜酸粒细胞炎症。
内容来自于医药魔方Pro,Science等源。
参考资料:
Ruth Choa et al. Thymic stromal lymphopoietin induces adipose loss through sebum hypersecretion. Science . 2021 Jul 30;373(6554):eabd2893. doi: 10.1126/science.abd2893


