Liver Cnacer:mTOR抑制剂Temsirolimus联合索拉非尼治疗晚期肝细胞癌的疗效和安全性:II期临床研究
时间:2021-09-19 20:26:13 热度:37.1℃ 作者:网络
mTOR信号通路在近一半的肝细胞癌(HCC)中上调,并与不良预后相关。在HCC的临床前模型中,mTOR通路抑制与索拉非尼的联合证明了治疗的有效性。I期临床研究提示mTOR抑制剂temsirolimus联合索拉非尼的具有可接受安全性,并显示一定疗效。因此,近期有研究者进行II期临床研究,评估mTOR抑制剂Temsirolimus联合索拉非尼治疗晚期肝细胞癌的疗效和安全性。相关结果发表在Liver Cancer杂志上。

该研究是单臂、开放性的II期研究,患者接受temsirolimus 10 mg/周联合sorafenib 200 mg Bid治疗。研究主要终点为治疗至进展的时间(TTP),次要终点为OS,ORR,安全性,AFP反应。研究共纳入29例患者,48%是丙型肝炎病毒(HCV)感染, 28%是HBV感染。大多数患者(86%)为BCLC C期,41%为门静脉血栓形成,69%为肝外扩散。31%的患者血清AFP水平至少为400 ng/mL。
28例患者(97%)可评估TTP。中位TTP为3.7个月(95% CI: 2.2, 5.3)个月,14% (95% CI: 0.5, 28)达到至少6个月的TTP。中位OS为8.8个月(95% CI: 6.8, 14.8)个月。
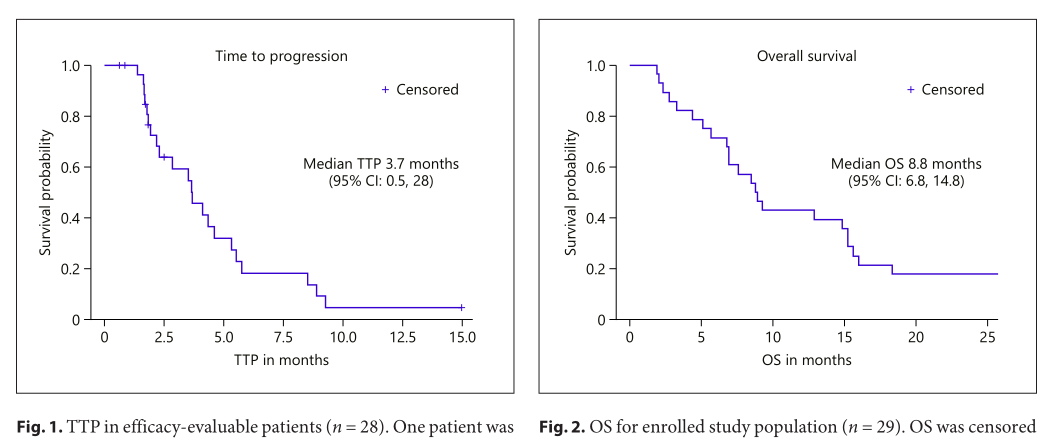
TTP和OS
没有患者达到完全缓解(CR)或部分缓解(PR)。21例(75%)患者达到病情稳定(SD),4例(14%)患者疾病进展(PD)。HBsAg +或HCV Ab +状态与TTP或OS预后之间没有显著关系。
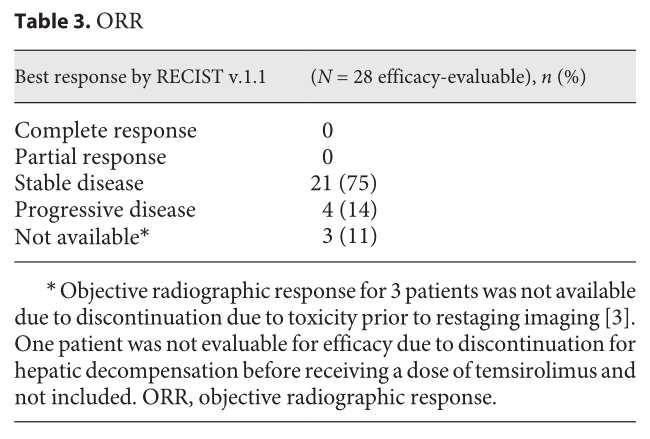
ORR
28例(21%)可进行安全性评价的患者中有6例发生了严重不良事件(SAE),至少有2例(7%)患者发生了与治疗相关的SAE(1例SAE为3级腹泻和3级脱水,需要住院治疗;1例SAE为 3级蜂窝织炎和2级肢体疼痛需住院治疗)。CTCAE 3级或更高级别最常见的与治疗相关的AEs是低磷血症、血小板减少和皮疹。
AFP反应,定义为AFP从基线水平下降至少50%。21例可评估患者中有10例(48%)发生AFP反应。与无AFP反应的患者(n = 11)相比,有AFP反应的患者TTP更长(中位5.8个月,95% CI: 4.1, 9.3),无AFP反应患者的中位TTP为2.3个月(95% CI: 1.6, 3.5) (p<0.0001)。有AFP反应和没有AFP反应患者的中位OS分别为11.1个月(95% CI: 1.9, 18.3) 和 7.6个月(95% CI: 2.3, 8.9) (p = 0.10)。
研究者还进行了二代测序(NGS)进行探索研究,研究发现最常见的基因改变是TP53(67%)、TERT启动子(38%)、CTNNB1(33%)、TSC1或TSC2(30%)、KMT2D(17%)和CCND1/ FGF19/4/3扩增子(13%)。Wnt通路突变(包括CTNNB1、APC和AXIN1)占42%,mTOR通路突变(包括TSC1、TSC2、磷酸酶和张力蛋白同源物、磷脂酰肌醇-3激酶和RICTOR)占46%。任何基因突变或发生率为10%的突变组与TTP或OS之间均无显著关系。在mTOR通路改变的患者中,TTP和OS均无明显缩短趋势。TERT启动子突变与HCV Ab+ (p = 0.0001)、非HBsAG + (p = 0.223)和非亚洲人种(p = 0.033)相关。
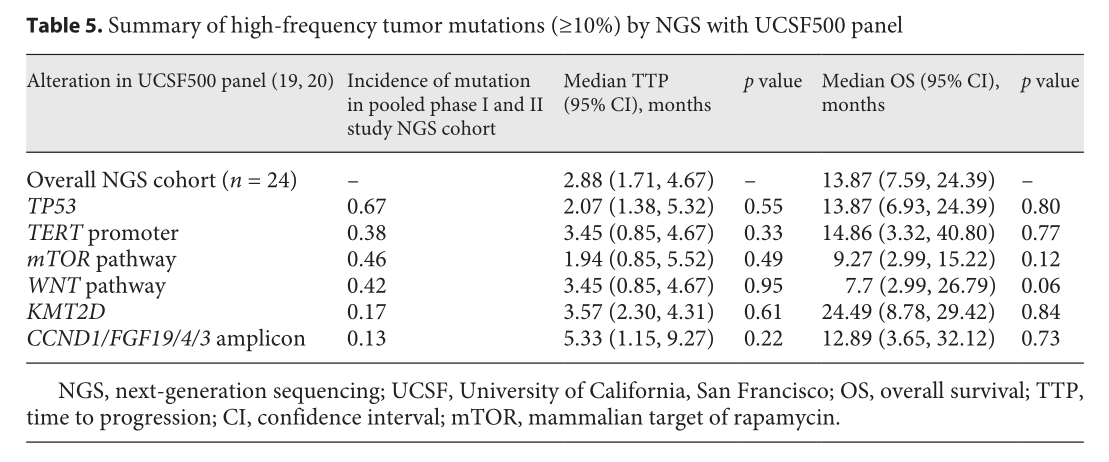
NGS探索
综上,mTOR抑制剂Temsirolimus联合索拉非尼治疗晚期肝细胞癌安全性可耐受,但没有达到研究终点。NGS分析mTOR通路突变跟肿瘤治疗反应无明显相关。
原始出处:
Robin K. Kelley, Nancy M. Joseph, Halla S. Nimeiri, et al. Phase II Trial of the Combination of Temsirolimus and Sorafenib in Advanced Hepatocellular Carcinoma with Tumor Mutation Profiling. Liver Cancer. DOI: 10.1159/000518297. Published online: September 6, 2021.


