Front Oncol: 阿帕替尼联合卡瑞利珠单抗在既往治疗过的晚期胆管癌患者中的疗效和安全性
时间:2021-10-18 22:01:14 热度:37.1℃ 作者:网络
胆道癌(BTC)是一组来自胆道上皮细胞的异质性肿瘤,通常分为肝内和肝外胆管癌(ICC, ECC)和胆囊癌(GBC)。尽管BTC传统上被认为是罕见的恶性肿瘤,它是第二大最常见的原发性肝脏肿瘤,约占所有肝胆恶性肿瘤的10%-15%。与其他胃肠道肿瘤一样,切缘阴性的根治性手术是唯一可能的治愈方式。但约60-70%的患者诊断为疾病晚期,不适合手术切除。此外,针对晚期BTC患者的治疗方案极为稀缺,疗效有限。只有少数化疗方案,包括吉西他滨+顺铂或其他铂衍生物被批准作为一线治疗,疗效有限,对二线和后线治疗没有共识的标准方案。对于晚期HCC患者,阿帕替尼联合卡瑞利珠单抗作为一线治疗的客观应答率为34.3%,作为二线治疗的客观应答率为22.5%。在骨肉瘤、胃癌、晚期三阴性乳腺癌和其他各种肿瘤中也观察到类似的结果。然而,到目前为止,没有研究报道该方案在BTC患者中的结果。因此,来自北京的学者开展了前瞻性临床研究,以评估阿帕替尼联合卡瑞利珠单抗在既往治疗过的晚期BTC患者中的有效性和安全性。相关结果发表在Frontiers in Oncology杂志上。

研究纳入22例患者,中位患者年龄为58岁(39-72岁),11例患者(52%)为男性。大多数患者(16例[76.2%])ECOG为1分,7例患者(33.3%)有HBV感染。15例(71%)为肝内胆管癌,4例(19%)为肝外胆管癌,2例(9%)为胆囊癌。胆管癌组织病理分级中,分级不确定4例(19%),低分化8例(38.1%),中分化7例(33.3%),高分化2例(9.5%)。21例患者中有20例(95.2%)出现转移,12例(57.2%)根治性切除术后复发。转移部位以肝内或淋巴结转移为主(17 80.9%),肺转移8例(38.1%)。20例(95.2%)患者接受了全身化疗,10例(47.6%)患者接受了至少两种治疗方案。此外,12例(57.1%)患者的CA19-9水平超过150 ng/ml。

疗效评估
根据RECIST 1.1标准,没有观察到CR,4例(19%)获得了PR,ORR为19%,和11例则为SD,疾病控制率(DCR)为71.4%。15例肝内胆管癌患者中有3例(25%)观察到客观反应,1例胆囊癌患者观察到PR。数据截止日期2020年8月1日,平均随访时间为13.4个月(IQR 11.9 - 14.8),治疗持续时间的中位数是4.9个月(IQR 3.8 -5.9), 21例患者中还有4例(19%)患者仍在接受治疗。在整个人群中,中位OS为13.1个月(95% CI, 8.1-18.2),中位无进展生存期(PFS)为4.4个月(95% CI, 2.4-6.3)。
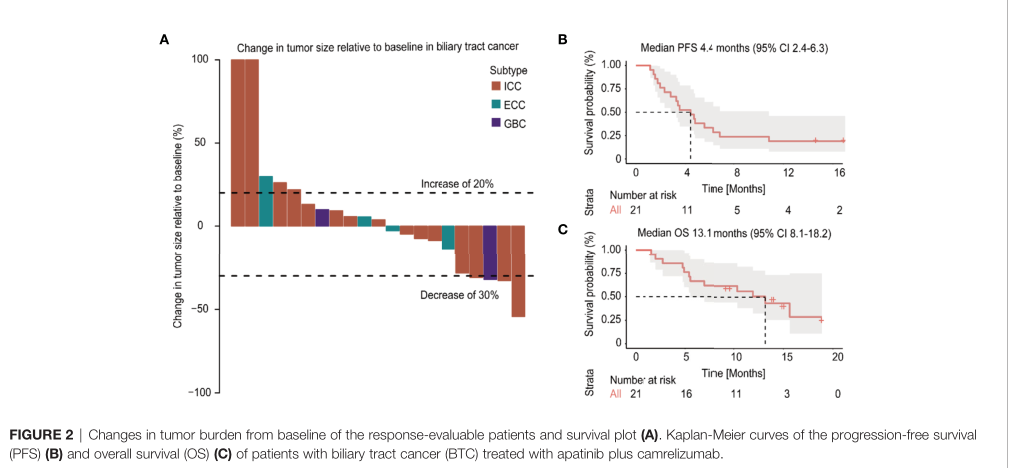
预后
所有患者都经历了至少一种不良事件,22例患者中有14例(63.6%)发生了3级或4级AEs。任何级别中最常见的与治疗相关的AEs为虚弱(n=15,68.2%)、食欲下降(n=10,45.5%)和高血压(n=7,31.8%)。最常见的3级或4级AEs为高血压(n=3,13.6%)、血胆红素升高(n=3,13.6%)和血小板计数下降(n=3,13.6%)。18例患者(81.8%)经历了治疗中断或调整,3例患者(13.6%)停止治疗。没有观察到与治疗相关的死亡。
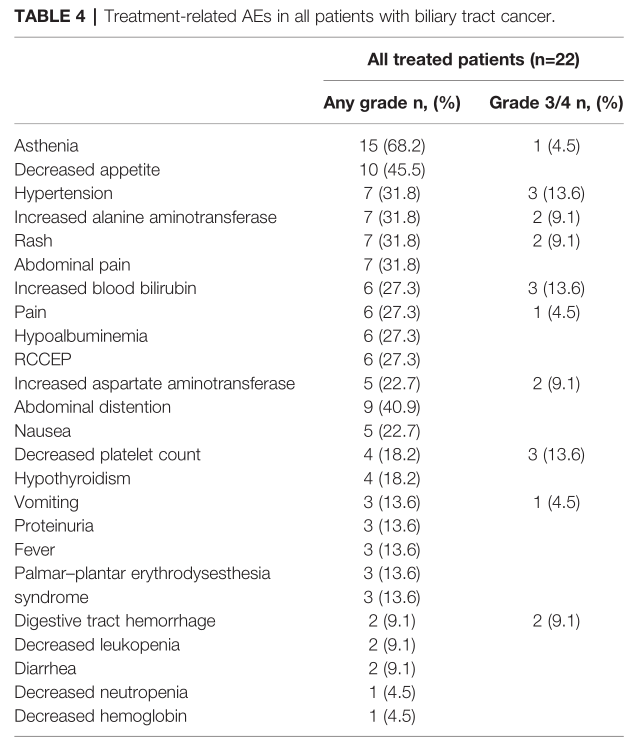
治疗相关不良事件
21例可用的肿瘤标本中,4例(19%)肿瘤细胞或免疫细胞中PD-L1染色阳性。在4例PD-L1阳性患者中,3例患者肿瘤缩小,但只有1例患者发生PR。PD-L1≥1%和PD-L1<1%患者的中位PFS和OS差异均无统计学意义(p=0.58,p=0.83)。虽然本研究样本有限,但考虑到胆道癌的异质性,我们分析了不同肿瘤亚型的疗效和安全性。结果显示,肝内胆管癌、肝外胆管癌和胆囊癌的ORR (X2 = 2.666, p=0.264)、3-4级AEs (X2 = 0.649, p=0.723)、PFS (p=0.958)、OS (p=0.725)差异无统计学意义。
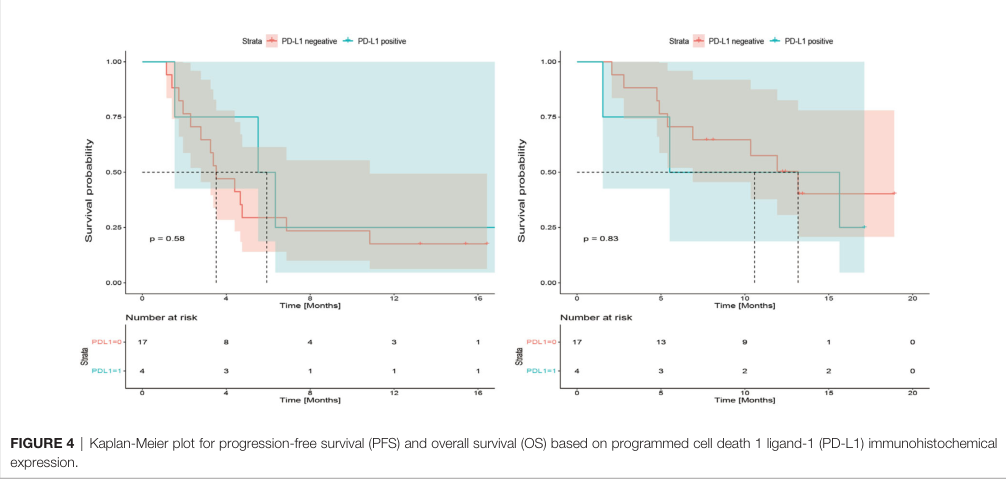
PD-L1状态对预后影响
综上,这是首个研究评估卡瑞利珠单抗联合阿帕替尼治疗胆道癌患者的有效性和安全性。结果表明,该方案治疗效果良好,毒性相对可控。
原始出处:
Wang D, Yang X, Long J, Lin J, Mao J, Xie F, Wang Y, Wang Y, Xun Z, Bai Y, Yang X, Guan M, Pan J, Seery S, Sang X and Zhao H (2021) The Efficacy and Safety of Apatinib Plus Camrelizumab in Patients With Previously Treated Advanced Biliary Tract Cancer: A Prospective Clinical Study. Front. Oncol. 11:646979. doi: 10.3389/fonc.2021.646979


