NLRP3抑制剂调节免疫微环境有助于改善肺动脉高压引起的急性右心衰竭
时间:2021-11-12 15:01:24 热度:37.1℃ 作者:网络

右心室衰竭(RVF)是肺动脉高压(PAH)患者发病率和死亡率的最重要预后因素。PAH患者出现肺部感染或产褥感染时,往往会迅速发展为心力衰竭。迄今为止,与左心衰竭的研究不同,对 RVF 的研究还不够充分。炎症可能在左心衰竭中起重要作用。当PAH患者出现肺部感染或产褥感染时,往往会迅速发展为心力衰竭。低剂量脂多糖诱导肺动脉高压大鼠快速右心室衰竭。NACHT、LRR 和 PYD 结构域蛋白 3 (NLRP3) 是一种细胞内危险传感器,它在激活时寡聚化并通过募集含有半胱天冬酶募集结构域 (ASC) 和 pro-casp1 的凋亡斑点样蛋白来启动炎性体的组装。
研究目的:研究NLRP3炎性体是否介导PAH大鼠心室免疫微环境的紊乱并促进右心室衰竭。
研究方法:
腹腔注射野百合碱用于诱导大鼠PAH。用脂多糖和MCC950治疗大鼠前后通过超声心动图测量右心室功能。用大鼠趋化因子和细胞因子抗体阵列、Western印迹、流式细胞术和定量实时PCR分析测量右心室组织中免疫微环境紊乱的程度。
研究结果:
NLRP3 炎症小体的形成导致 IL-1β 成熟和释放,这是细胞或组织损伤后炎症反应放大过程中一个关键的、精细调节的步骤。

许多研究强调了 NLRP3 激活与高血压和心血管疾病的关联。最近的一项研究表明,通过 NLRP3 炎症小体途径,低剂量脂多糖 (LPS;2 mg/kg) 足以诱导 NLRP3-A350V/CreT 突变小鼠的心脏功能障碍。NLRP3介导IL-1β的表达和释放,但NLRP3通过介导心肌细胞与巨噬细胞相互作用参与调节炎症状态下心肌免疫微环境的机制尚未报道,NLRP3炎性体通路是否有助于RVF并且其潜在机制在很大程度上是未知的,系统性阻断 NLRP3 可改善 LPS 诱导的右心组织免疫微环境波动。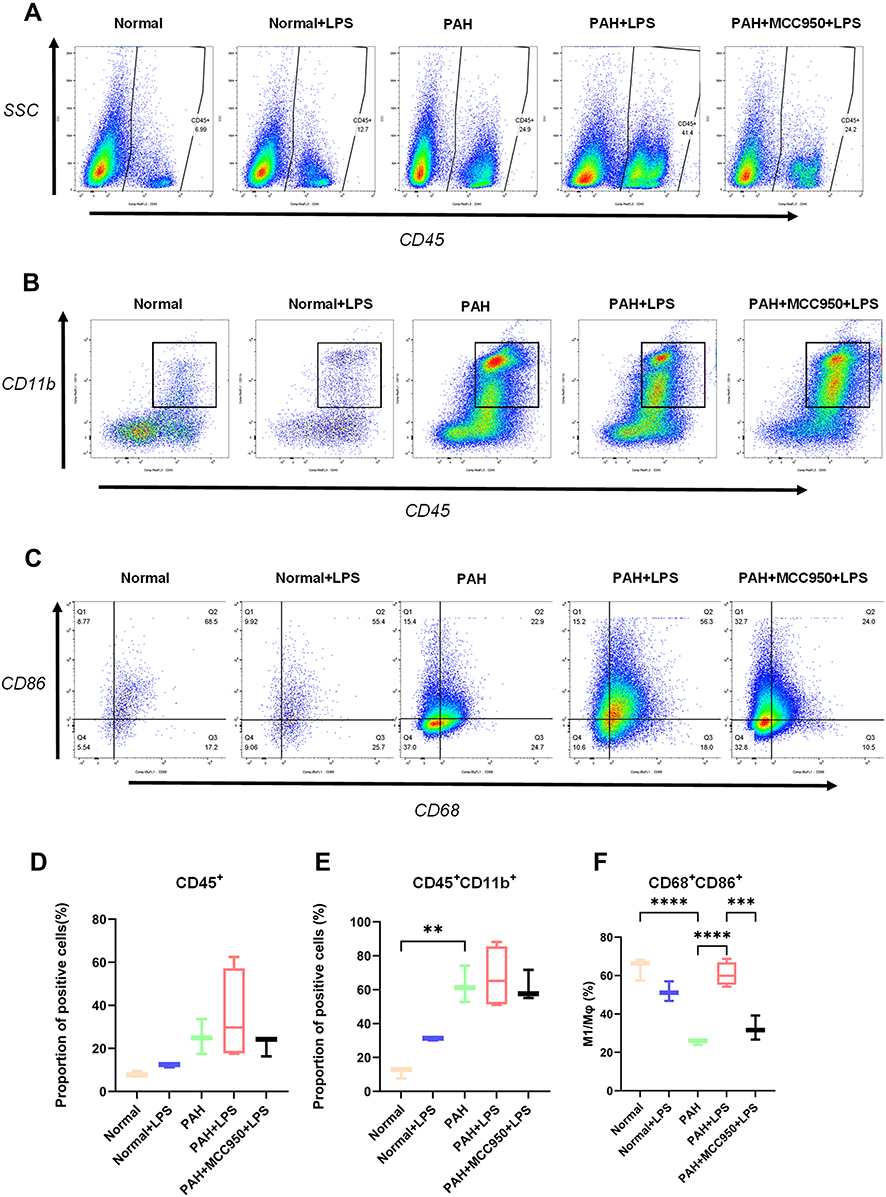 我们证实NLRP3炎性体通过促进心肌细胞焦亡和单核细胞趋化蛋白1(MCP-1)的表达参与调节巨噬细胞极化,促进急性右心衰竭的发生和发展。
我们证实NLRP3炎性体通过促进心肌细胞焦亡和单核细胞趋化蛋白1(MCP-1)的表达参与调节巨噬细胞极化,促进急性右心衰竭的发生和发展。

在这项研究中,我们证明 NLRP3 炎症小体在介导 PAH 大鼠的急性 RVF 中起重要作用。当 PAH 大鼠接受 LPS 时,免疫微环境发生显着变化,炎症细胞因子、趋化因子、生长因子表达增加,M1 巨噬细胞极化比例增加。抑制 NLRP3 可显着降低心肌细胞炎症水平并阻止 M1 巨噬细胞极化,最终改善心脏功能障碍并维持钙稳态相关蛋白的表达。本研究首次在 RVF 模型中研究 NLRP3 通路与心肌免疫微环境之间的关系。
参考文献:
Guo L, Qin G, Cao Y, Yang Y, Dai S, Wang L, Wang E. Regulation of the Immune Microenvironment by an NLRP3 Inhibitor Contributes to Attenuation of Acute Right Ventricular Failure in Rats with Pulmonary Arterial Hypertension. J Inflamm Res. 2021 Nov 2;14:5699-5711. doi: 10.2147/JIR.S336964. PMID: 34754216; PMCID: PMC8572093.


