安心求美,闻“毒”不色变内容。
时间:2021-11-22 18:01:49 热度:37.1℃ 作者:网络

“肉毒毒素”由于天生自带毒属性总会让人在选择肉毒素用于皱纹的治疗时心存担忧,别求美不成反而搭上了自己的健康,特别是由于肉毒毒素A必须在较长时间内重复应用才能防止眉间纹的复发,因此它的“毒性”是否会蓄积成安全问题?放心求美的前提可是必须证明其在长时间重复给药时具有可靠的安全性和有效性。
那么我们来看看证据如何,本研究招募了1,415 名患者接受24个月的肉毒毒素A连续治疗并在长达36个月的时间里监测其安全性,为肉毒毒素A的临床应用提供更加准确的安全性和有效性数据。
具体结果如下:
患者数据和治疗方案
患者的临床特征总结在表 1 中。平均年龄为 49.5±9.7 岁,大多数患者为女性 (n = 1,289, 91%) 和白人 (n = 1,151, 81%)。在1,415名接受治疗的患者中(2005年11月14日–2011年12月5日,44个美国中心),1,122名(79%)完成了 24 个月的治疗,922 名(65%)在 36 个月时进行了安全性评估(图 1)。9 名 (<1%) 患者因副反应退出,没有患者因眼睑下垂或疗效不佳而退出。
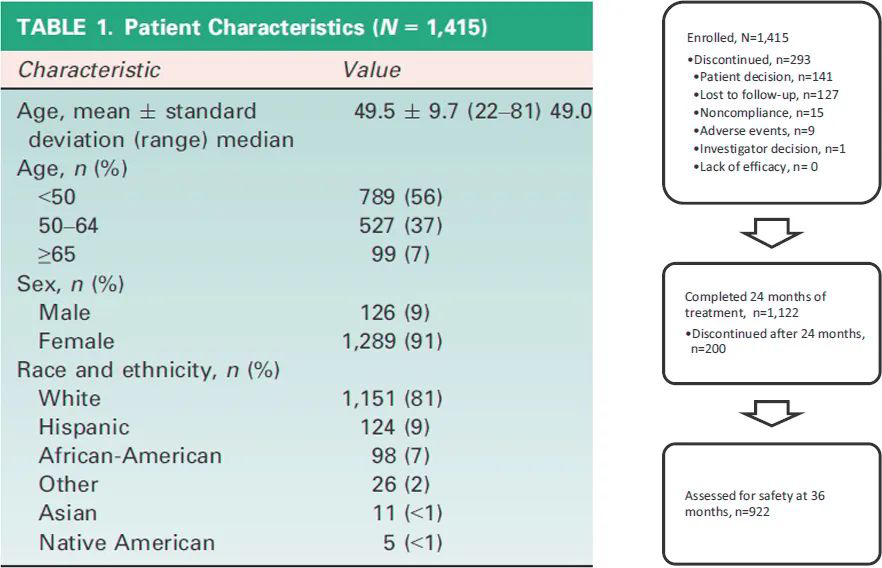
在为期24个月的治疗期间总共对患者施用了7,938剂肉毒毒素A,其中女性的平均接种次数为5.6±1.9(接种次数范围 1-9),男性为5.8±2.2(接种次数范围 1-9),267 名患者接受了 8个周期的治疗。此外,两男一女接受了九个治疗周期,四名女性接受了 80U的肉毒毒素A, 一名女性因为肌肉质量原因接受了一次70 U剂量和两次60 U剂量的治疗。
安全性:副作用中绝大多数(89%)为轻度和中度,重复给药并不会增加患者的副作用发生率
在所有受试者中有991 名(70%)患者发生了不良事件(表 2 和 3)。治疗相关的副作用(TEAE)在男性和女性以及所有剂量组中的发生率和类型均无显著差异,并且重复给药不会增加副反应的发生率(表 4)。大多数TEAE 为轻度 (n = 3,372, 69%) 或中度 (n = 998, 20%)。在以固定剂量应用肉毒毒素A和基于肌肉质量的剂量研究中,每位患者的严重 TEAE 发生率为 0.18 或更低。两个严重副作用(偏头痛和头痛)可能与治疗有关,其他的严重副作用与肉毒毒素A的治疗无明显相关性。其中一名患者的一项TEAE (<0.1%) 被归类为严重副作用,该患者因与治疗相关的轻度右眼睑下垂到医院急诊室就诊。
眼部相关TEAE的发生率为0.7%,共影响49名患者(49/1415,3.5%),所有与治疗相关的眼睑下垂事件都会自行恢复
该研究共发现 184 种眼部疾病的 TEAE,包括眼睑下垂、眼睑水肿、视力模糊、眼睛刺激,发生率为 0.7%(7,938 次注射中有 53 次事件),共发生49名患者(49/1415,3.5%) 中。在 49 名与治疗相关的上睑下垂患者中,46 名 (3.6%) 为女性,3 名 (2.4%) 为男性。所有与治疗相关的眼睑下垂事件都会自行恢复,并未影响肉毒毒素A的应用。
初次显示疗效的时间男性和女性相似,约为2-5天,总疗效持续时间患者评估为 94 天(范围30-801天),研究者评估为116天(范围30-813天),50岁以下患者疗效最好,65岁以上患者疗效最低
在每个治疗周期中,男性和女性初次出现疗效的时间相似,女性为 2-4 天,男性为 2-5 天(由患者报告并记录)。根据患者自我评估,总疗效持续时间中位数为 94 天(范围 30-801 天),根据研究者评估为 116天(范围 30-813天)。根据针对最大皱眉这一参数的研究人员实时评估和患者自我评估的对比发现,对于大多数访问,两个评分量表之间的相关性具有统计学意义(P< 0.05)。对比男性和女性的反应率发现,在所有治疗周期中,女性对50-U 固定剂量的复合反应率(范围 0.728-0.877)高于男性(范围 0.353-0.686)。在基于肌肉质量应用肉毒毒素A时,男性(0.583–1.000)和女性(0.647–1.000)的复合反应率相似。50 岁以下患者的反应率最高,65 岁及以上患者的反应率最低。因此在第 1 周期中,50 岁以下患者中显示疗效(研究者实时评估)的比例为 0.925 (699/756),65 岁以上患者中显示疗效的比例为 0.832 (79/95)。同样,在第 8 周期中,比例分别为 0.924 (122/132) 和 0.737 (14/19)。此外,种族和其他人口统计特征对反应率没有影响。
综上所述,该项长期研究的结果表明,肉毒毒素A在对患者长达24个月的反复给药和36个月的安全性监测中表现出了良好的治疗耐受性和有效性,可极大改善患者的中度和中度眉间纹。在连续的治疗周期中,TEAE 的总体发生率并未增加,并且大多数副作用为轻度至中度。此外,与治疗相关的眼睑下垂的发生率很低 (0.7%),并且这些副作用都会自我恢复。
往期推荐

https://www.medsci.cn/article/show_article.do?id=ebe4211932f2

https://www.medsci.cn/article/show_article.do?id=769321281112

https://www.medsci.cn/article/show_article.do?id=fcd32145e82a

https://www.medsci.cn/article/show_article.do?id=1ecc215025d5

https://www.medsci.cn/article/show_article.do?id=68c7215356e3
CN-DYS-2100061
材料仅供医疗卫生专业人士学习交流
不作为临床使用推荐及其他用途
相关临床应用应符合中国国家药品监督管理局批准的使用说明书
1. https://pubmed.ncbi.nlm.nih.gov/23190342/
2. https://pubmed.ncbi.nlm.nih.gov/19537366/
3. https://pubmed.ncbi.nlm.nih.gov/19584772/
4. https://pubmed.ncbi.nlm.nih.gov/19549186/
注册高德美院医师社区
获得更多医美前沿资讯,点击下方链接即可跳转
http://ypxcx.medsci.cn/calderma/index.html#/
参考文献:
1.Rzany B, Flynn TC, Schloebe A, Heinz M, Harrington L. Long-Term Results for IncobotulinumtoxinA in the Treatment of Glabellar Frown Lines. Dermatol Surg. 2013;39(1):95-103.
2.Rubin MG, Dover JS, Glogau RG, Goldberg DJ, Goldman MP, Schlessinger J. The Efficacy and Safety of a New US Botulinum Toxin Type A in the Retreatment of Glabellar Lines Following Open-Label Treatment. Journal of Drugs in Dermatology. 2009;8(5):439-44.
3.Kane MAC, Brandt F, Rohrich RJ, Narins RS, Monheit GD, Huber MB, et al. Evaluation of Variable-Dose Treatment with a New US Botulinum Toxin Type A (Dysport) for Correction of Moderate to Severe Glabellar Lines: Results from a Phase III, Randomized, Double-Blind, Placebo-Controlled Study. Plast Reconstr Surg. 2009;124(5):1619-29.
4.Brandt F, Swanson N, Baumann L, Huber B. Randomized, Placebo-Controlled Study of a New Botulinum Toxin Type A for Treatment of Glabellar Lines: Efficacy and Safety. Dermatol Surg. 2009;35(12):1893-901.


