Eur J Cancer:Nivolumab联合多西他赛治疗未经化疗的转移性去势抵抗前列腺癌(mCRPC)的疗效和安全性
时间:2021-12-02 10:02:01 热度:37.1℃ 作者:网络
免疫治疗目前已被用于多种肿瘤的治疗。多西他赛被推荐用于转移性前列腺癌的一线化疗药物。多西他塞具有免疫刺激作用,可能促进前列腺肿瘤免疫微环境。因此,美国的学者开展了II期临床研究CheckMate 9KD,旨在评估PD-1抑制剂nivolumab联合多西他赛治疗转移性去势抵抗前列腺癌(mCRPC)的疗效和安全性。相关结果发表在European Journal of Cancer杂志上。

CheckMate 9KD (NCT03338790)是一项非随机、多队列、全球II期临床研究。84例未化疗去势抵抗mCRPC患者接受nivolumab 360 mg和多西他赛75 mg/ m2每3周治疗1次,强的松5 mg,每日2次(≤10个周期),然后nivolumab 480 mg每4周1次(≤2年)。主要研究双终点为客观缓解率(ORR)和前列腺特异性抗原应答率(PSA 50 -RR;比基线减少≥50%)。
84名mCRPC患者(全治疗人群)接受了nivolumab联合多西他赛治疗。大多数患者(n=54, 64.3%)曾接受过NHT,主要是enzalutamide (n=24, 28.6%),阿比特龙(n=17, 20.2%)或两者(n=12, 14.3%)。在数据截止日期(2020年7月17日)时,76名患者(90.5%)停止了所有研究治疗,主要原因是疾病进展(n=50, 59.5%)或研究药物毒性(n=15, 17.9%)。治疗持续时间(范围): nivolumab 7.2个月(0.0-22.1),多西他赛5.2个月(0.0-7.6);中位随访时间为15.2个月。
在45例基线可测量病灶的患者中,确认的ORR (95% CI)为40.0% (25.7-55.7), 1例(2.2%)达到完全缓解,17例(37.8%)达到部分缓解。中位治疗至出现客观缓解的时间(范围)为2.0个月(1.6-7.3),中位缓解持续时间(95% CI)为7.0个月(6.4-12.4)。81例PSA可评价患者中,PSA 50 -RR (95% CI)为46.9% (35.7-58.3), PSA 30 -RR (95% CI)为58.0% (46.5-68.9)。
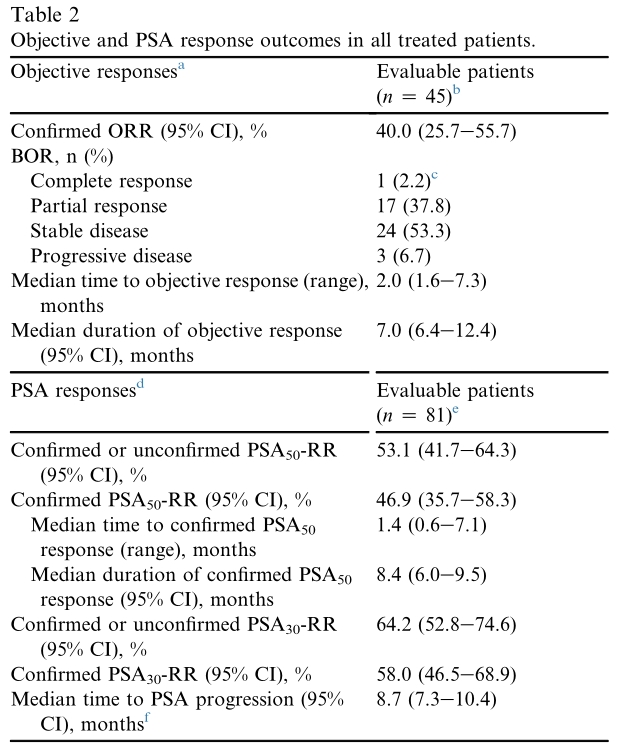
疗效评估
在所有84例接受治疗的患者中,中位rPFS (95% CI)为9.0个月(8.0-11.6),中位OS (95% CI)为18.2个月(14.6-20.7)。
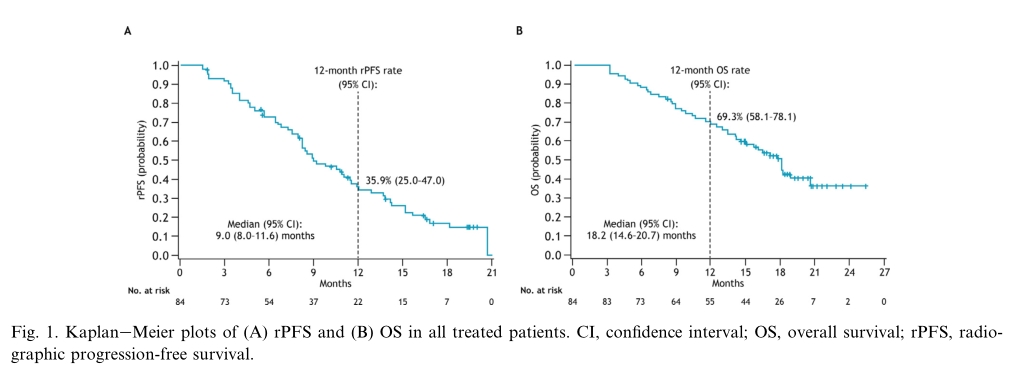
rPFS和OS
在有NHT对比无NHT治疗亚组分析中,ORR (95% CI)分别为38.7% (21.8-57.8)和42.9% (17.7-71.1)。PSA 50 -RR和PSA 30 -RR (95% CI)分别为39.6% (26.5-54.0) vs 60.7% (40.6-78.5)和52.8% (38.6-66.7) vs 67.9 (47.6-84.1)。中位rPFS (95% CI)为8.5个月(7.5-10.8) vs 12.0个月(6.2-18.2),中位OS (95% CI)为16.2个月(13.5-18.3) vs 未达到(9.9-不可估计)。
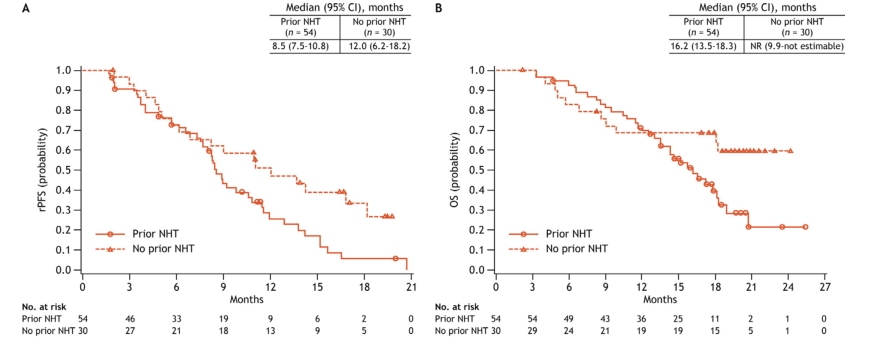
NHT治疗分组
在HRD阴性/不可评估 对比HRD阳性肿瘤亚组分析中,确认的ORR (95% CI)为42.3% (23.4-63.1) vs 36.8% (16.3-61.6)。在PSA可评估患者中,PSA 50 - RR和PSA 30 - RR(95% CI)分别为44.7% (30.2-59.9) vs 50.0% (32.4-67.6)和63.8% (48.5-77.3) vs 50.0% (32.4-67.6)。中位rPFS (95% CI)为8.3个月(5.7-11.5) vs 9.8个月(8.3-12.9);中位OS (95% CI)为18.2个月(13.5-不可估计) vs 18.3个月(13.0-不可估计)。
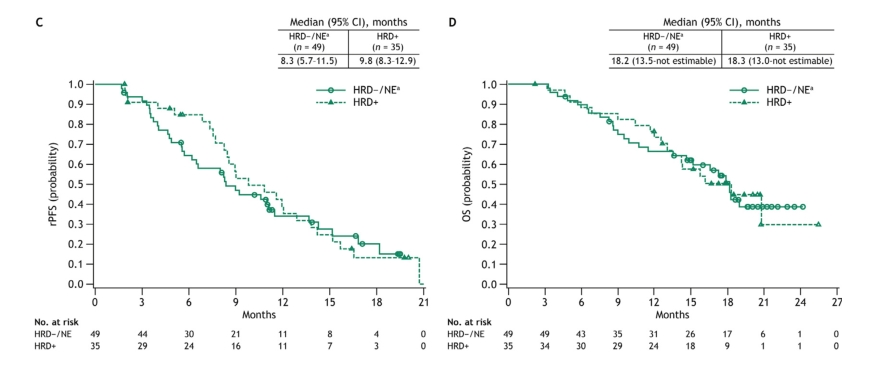
HRD状态分组
在TMB<10对比≥10突变/ Mb, ORR(95% CI)为50.0% (29.1-70.9) vs 38.5% (13.9-68.4)。PSA 50 - RR和PSA 30-RR (95% CI) 为52.2% (36.9-67.1) vs 31.6% (12.6-56.6)和58.7% (43.2-73.0) vs 52.6 (28.9-75.6)。中位rPFS (95% CI)为9.8个月(8.2-12.0) vs 9.0个月(6.2-12.9)。中位OS (95% CI)为17.3个月(13.0-不可估计) vs 15.7个月(6.-不可估计)。
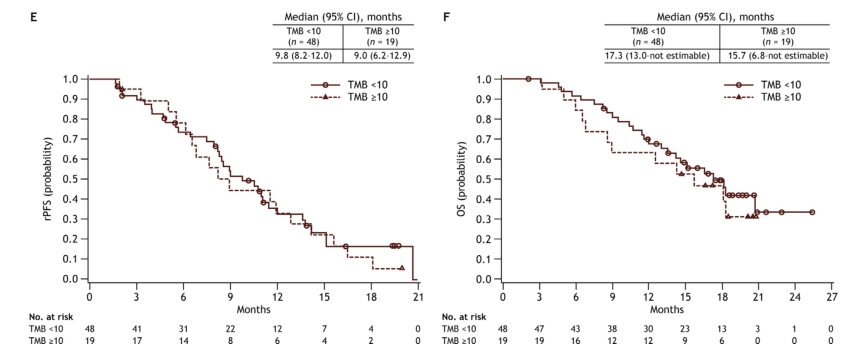
TMB分组

亚组分析汇总
95.2%患者发生与治疗相关的任何级别AEs,最常见的是疲劳(39.3%)、腹泻(35.7%)和脱发(34.5%)。47.6%的患者发生3-4级治疗相关AEs,最常见的是中性粒细胞减少(16.7%)。在所有接受治疗的患者中,27.4%和26.2%的患者报告了任何级和3-4级治疗相关的严重AEs,最常见的事件是肺炎(6.0%和4.8%)。任何级和3-4级治疗相关的AEs导致停用一种或两种研究药物在所有接受治疗的患者中,分别占29.8%和14.3%,导致停药的最常见事件是肺炎(分别占7.1%和4.8%)。最常见的任何级别免疫介导的AE是皮疹(10.7%)、肺炎(9.5%)和甲状腺功能减退(6.0%);最常见的3-4级免疫介导的AE为肺炎(4.8%)。
综上,研究表明,nivolumab联合多西他赛对未经化疗的mCRPC患者有一定临床疗效,且安全性可控。这些结果进一步支持了正在进行的III期临床研究CheckMate 7DX的实施。
原始出处:
Fizazi K, González Mella P, Castellano D, Minatta JN, Rezazadeh Kalebasty A, Shaffer D, Vázquez Limón JC, Sánchez López HM, Armstrong AJ, Horvath L, Bastos DA, Amin NP, Li J, Unsal-Kacmaz K, Retz M, Saad F, Petrylak DP, Pachynski RK. Nivolumab plus docetaxel in patients with chemotherapy-naïve metastatic castration-resistant prostate cancer: results from the phase II CheckMate 9KD trial. Eur J Cancer. 2021 Nov 18:S0959-8049(21)01144-8. doi: 10.1016/j.ejca.2021.09.043. Epub ahead of print. PMID: 34802864.


