JAMA:突破性感染新冠病毒后患者能获得超级免疫力
时间:2021-12-19 11:02:15 热度:37.1℃ 作者:网络
越来越多地报道了接种 SARS-CoV-2 疫苗后,出现突破性感染,这可能是由于疫苗诱导的抗体水平下降。此外,对疫苗诱导抗体的敏感性降低的新出现的变异是大多数新病例的原因。研究的重点是根据标准疫苗接种实践后的抗体水平来确定疫苗突破率。我们评估了突破感染后的抗体水平和变异交叉中和。
这项研究刚刚发表在最新一期的JAMA上。
2021 年 1 月 31 日至 2021 年 8 月 18 日期间,在俄勒冈健康与科学大学招募了突破性感染人群。患者根据PCR方法确诊突破性感染的人群。对照是完全接种疫苗的个体,没有突破感染。通过性别、年龄、疫苗接种之间的时间以及样本收集和最近一次抗原暴露之间的时间(有突破感染的人的 PCR 确认和对照的最终疫苗剂量)相匹配。全长病毒基因组测序用于确定 SARS-CoV-2 变异株。使用酶联免疫吸附试验来确定血清稀释滴度,其中 50% 有效浓度 (EC50) 的 IgG、IgA 和 IgM 抗体对 SARS-CoV-2 尖峰受体结合域具有特异性。通过针对原始 SARS-CoV-2 菌株 (WA1) 和相关变体(Alpha、Beta、Gamma 和 Delta)的分离株进行 50% 焦点减少中和试验 (FRNT50) 确定活的 SARS-CoV-2 中和血清稀释滴度。
中值突破和对照血清值在 GraphPad Prism 中计算,并与具有 Holm-Šídák 校正的 Wilcoxon 配对符号秩检验进行比较。通过比较序列确认的 Delta 变异突破案例、非 Delta 突破案例和对照的 Delta 和 WA1 中和效价,使用带有 Dunn 校正的 Kruskal-Wallis 检验来确定对 Delta 中和效力。
结果表明,共招募了26 名突破性感染受试者(平均年龄,38 岁;20 [77%] 名女性;24 [92%] 名接种了 BNT162b2,在 PCR 日期后中位数为 28 天和最终接种后 213.5 天进行采样;21 [81%] ] 与 26 名对照者(平均年龄 39 岁;21 名 [81%] 女性;26 名 [100%] 接种 BNT162b2,在最终接种后平均 28 天取样)。突破性感染参与者的总受体结合域特异性免疫球蛋白增加,EC50 中位数为 2152(95% CI,961-3596),而对照组为 668(95% CI,473-892)(增加 322%;P < 0.001)(图 1A)。 IgG 和 IgA 的中值血清稀释度均增加。突破感染后 IgA EC50 的中位数为 120(95% CI,44-246),而对照组为 24(95% CI,24-24)(增加 502%;P < .001)。 IgM 水平在各组之间没有显着差异。

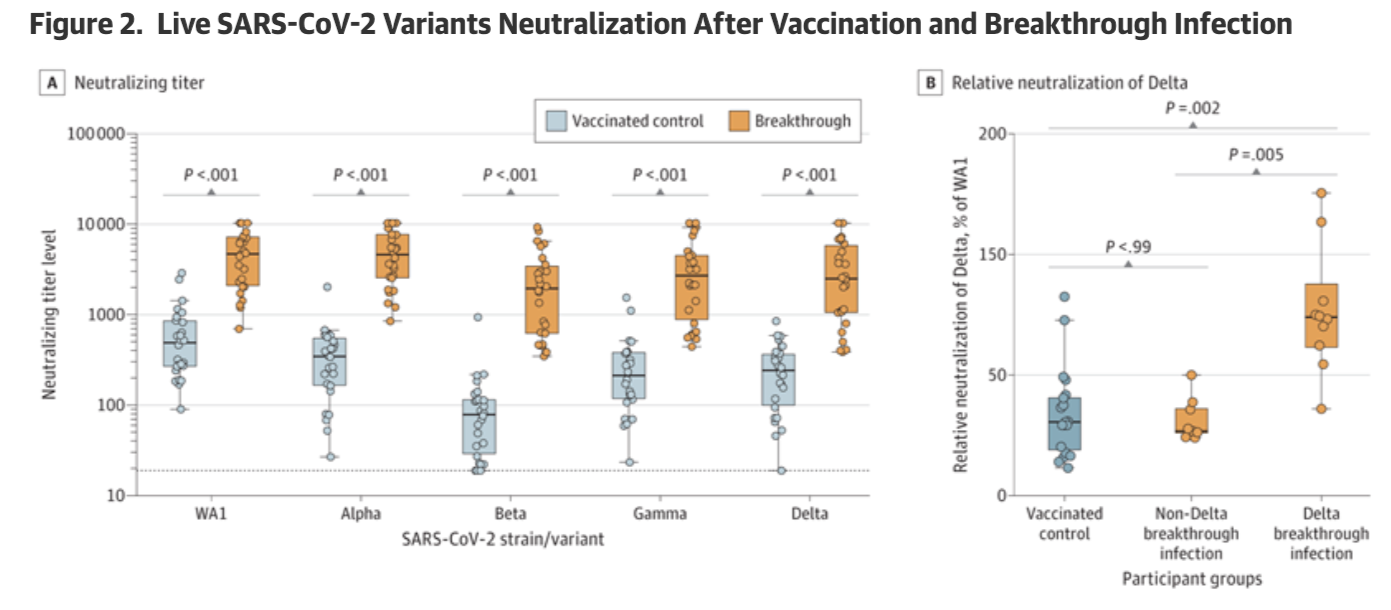
在序列确认的突破性病例中,10 例为 Delta 感染,9 例为非 Delta 感染。在突破性病例中,针对 WA1 的 FRNT50 中位数为 4646(95% CI,2283-7053),而对照组为 489(95% CI,272-822)(增加 950%;P < .001)。 Alpha、Beta 和 Gamma 变体的 FRNT50 结果如图 2A 所示。在突破性病例中,针对 Delta 变体的 FRNT50 中位数为 2482(95% CI,1072-4923),而对照为 243(95%CI,118-336)(增加 1021%;P < .001) . Delta 突破病例的血清对 Delta 变体的效力提高,每个参与者的 WA1 中和率为 99%(95% CI,73-151),而非 Delta 病例为 36%(95% CI,33-52)和41% (95% CI, 24-56) 为控制 (图 2B)。
这项研究的结果表明,尽管主要是轻度疾病,但在突破性感染后,体液免疫显着增强,尤其是 IgA 最为显著,可能是由于疫苗接种和自然感染之间的暴露途径不同。 此外,突破性血清表现出改进的变异交叉中和作用,尤其是 Delta 突破感染对 Delta表现出更高的效力,这表明通过开发具有与新兴 SARS-CoV 相匹配的抗原插入物的变体增强剂,可以扩大保护性免疫反应。
当然,这项研究的局限性包括样本数量少,以及突破组和对照组之间从初始接种到血清收集的时间差异,新出现的证据表明这可能有助于变异交叉中和抗体反应的发展。
另外,梅斯医学认为,突破性感染对奥密克戎是否同样有效,还需要进一步研究。
原始出处:
Bates TA, McBride SK, Winders B, Schoen D, Trautmann L, Curlin ME, Tafesse FG.Antibody Response and Variant Cross-Neutralization After SARS-CoV-2 Breakthrough Infection.JAMA. 2021 Dec 16. doi: 10.1001/jama.2021.22898


