Lancet Neurol:阿尔茨海默病的血液生物标志物:走向临床应用
时间:2022-01-10 18:15:52 热度:37.1℃ 作者:网络
:copyright:本文来源于:小崔和他的小伙伴们


导
读
 多年来,基于血液的AD的生物标志物似乎无法实现,但最近的结果显示,它们可以成为现实。如何将这些生物标志物进入临床实践,这一步将为血液生物标志物铺平道路,以支持AD和其他痴呆症的诊断和治疗的发展。近期,《Lancet Neurol》发表了一篇名为《Blood-based biomarkers for Alzheimer’s disease:towards clinical implementation》的文章,作者全面概述了最近的进展,重点关注最接近临床的三个生物标志物:Aβ、pTau和NfL。还讨论了新出现的星形细胞生物标志物胶质纤维酸性蛋白(GFAP)。最后,提出了一个基于血液的生物标志物路线图,解决了在临床护理和试验中实现所需的具体活动,突出了迄今为止的进展。
多年来,基于血液的AD的生物标志物似乎无法实现,但最近的结果显示,它们可以成为现实。如何将这些生物标志物进入临床实践,这一步将为血液生物标志物铺平道路,以支持AD和其他痴呆症的诊断和治疗的发展。近期,《Lancet Neurol》发表了一篇名为《Blood-based biomarkers for Alzheimer’s disease:towards clinical implementation》的文章,作者全面概述了最近的进展,重点关注最接近临床的三个生物标志物:Aβ、pTau和NfL。还讨论了新出现的星形细胞生物标志物胶质纤维酸性蛋白(GFAP)。最后,提出了一个基于血液的生物标志物路线图,解决了在临床护理和试验中实现所需的具体活动,突出了迄今为止的进展。

Part.01
散发性AD的血液生物标志物的介绍
1.淀粉样蛋白(Aβ1-42与Aβ1-40) Aβ是AD的主要病理标志,而在症状出现前几十年,CSF和PET生物标志物对Aβ的病理作用就已出现异常。现在有各种可靠的方法来精确和稳健地量化血浆Aβ1-42和Aβ1-40,每种方法在成本和使用方面有各自的优劣:质谱分析和自动超灵敏的免疫测定(如单分子阵列;组1)可以量化特定的全长型(Aβ1-42和Aβ1-40)或N端截断型(Aβx-42和Aβx-40)等多肽。这些对血浆Aβ定量的检测方法,在涵盖AD的整个过程的不同队列中,其临床价值已经得到验证。血浆Aβ1-42与Aβ1-40的比率(Aβ42/40)可以鉴定出CSF或PET状态的异常,质谱分析的准确率在82%到97%之间,免疫分析的准确率在62%到79%之间。血浆Aβ42/40对区分AD和非AD的诊断价值还没有被研究过。 组1:用于血源性生物标志物物测量的常用技术
2.磷酸化tau(pTau)
含有全长或截断形式的高磷酸化tau是AD的另一个主要病理标志。Tau有70多个翻译后修饰位点,包括40多个磷酸化位点和几个截断形式。不同的pTau形式在CSF和血浆中均可测量。 Aβ类似,现在有各种方法,如质谱和基于免疫的方法来检测淀粉样蛋白或tau的病理变化,准确率很高(80-98%)。血浆中不同位点磷酸化的tau的浓度(pTau181、pTau217或pTau231)有强烈的差异。AD患者与认知障碍的人相比、认知障碍的对照组和非AD患者相比,pTau181、pTau217或pTau231都强烈增加(超过两倍)。此外,血浆中pTau181浓度的增加与灰质萎缩这些关联只在有Aβ病理的个体中观察到,这说明了pTau181对AD以及神经病理变化的特异性,与Aβ42/40相比,其作为血浆生物标志物的性能更好。血浆中的p Tau217可以区分AD和非AD,准确率很高(96%),也能高度准确地识别tau-PET阳性病例。pTau217能更好地检测Aβ-PET阳性,与tau-PET的关联性更强。pTau231可以鉴别AD和非AD,与pTau181相似,然而,根据Aβ-PET和tau Braak阶段,pTau231在AD病理的早期阶段开始变化,这表明pTau231作为AD的早期病理标志物可能特别有价值,甚至在症状出现之前就已经存在。pTau形式已被证明可以检测到阿尔茨海默氏症的连续性病理变化,因此可以作为阿尔茨海默氏症的特定诊断标志物。此外,与血浆Aβ42/40不同,血浆pTau 浓度在疾病进展过程中逐渐增加,从而表明,pTau可能对监测疾病阶段有潜在的作用。迄今为止,研究的主要局限性是,它们主要是由几个小组利用回顾性队列完成的,前瞻性验证和纳入更多的异质性人群是一些研究的一些必要的下一步措施。
3.神经丝轻链(NfL)
NfL是一种轴突支架蛋白,是中枢神经系统中两个核心神经丝蛋白之一(另一个是 α-internexin),神经丝对于轴突的生长和稳定以及中枢神经系统的突触组织和功能都是必不可少的。这种生物标志物可以在脑脊液和血液中测量,是第一个被证实具有临床价值的神经特异性生物标志物。在神经炎症和神经退行性疾病中,CSF和血液中的NfL之间的相关性很好(r值为0-70-0-97).NfL浓度最高的是额颞叶、血管和HIV相关的痴呆,以及肌萎缩性脊髓侧索硬化症和非典型帕金森病。在散发性AD中,CSF NfL在AD相关液体生物标志物中显示出第二高的倍数变化(仅次于CSF tTau). 因此,NfL可被用作初步诊断测试,如果呈阳性,可进行更多的检查,以获得更具体的结果,更好地了解神经变性的根本原因。NfL还可以作为疾病严重程度的生物标志物,用于疾病调节治疗的临床试验,并在临床实践中优化和监测治疗效果,这与它在多发性硬化症中的应用相似。
4.神经胶质纤维酸性蛋白(GFAP)
GFAP是星形胶质细胞的一个主要细胞骨架成分,在AD中,反应性星形细胞增多症已被认为是AD的潜在驱动因素或影响疾病的病理变化。通过超灵敏的免疫分析法,在AD患者中,血浆或血清中的GFAP浓度会升高。此外,血浆或血清GFAP的增加也与临床上的疾病的严重程度有关,在患有轻度认知障碍的患者,血浆GFAP预测了AD的后续发展。在认知能力未受影响的人中,血清中GFAP的浓度越高,与认知能力下降的速度、更高的痴呆症风险有关。值得注意的是,血浆或血清GFAP的预测价值是独立于血浆的 Aβ42/40. 由于星形胶质细胞的激活不是AD病理生理学所特有的,GFAP可能是其他类型痴呆的潜在生物标志物。但是,还需要进一步的研究来确定这些潜在因素在不同类型的痴呆症和神经退行性疾病中的临床应用。
组1:用于血源性生物标志物物测量的常用技术
2.磷酸化tau(pTau)
含有全长或截断形式的高磷酸化tau是AD的另一个主要病理标志。Tau有70多个翻译后修饰位点,包括40多个磷酸化位点和几个截断形式。不同的pTau形式在CSF和血浆中均可测量。 Aβ类似,现在有各种方法,如质谱和基于免疫的方法来检测淀粉样蛋白或tau的病理变化,准确率很高(80-98%)。血浆中不同位点磷酸化的tau的浓度(pTau181、pTau217或pTau231)有强烈的差异。AD患者与认知障碍的人相比、认知障碍的对照组和非AD患者相比,pTau181、pTau217或pTau231都强烈增加(超过两倍)。此外,血浆中pTau181浓度的增加与灰质萎缩这些关联只在有Aβ病理的个体中观察到,这说明了pTau181对AD以及神经病理变化的特异性,与Aβ42/40相比,其作为血浆生物标志物的性能更好。血浆中的p Tau217可以区分AD和非AD,准确率很高(96%),也能高度准确地识别tau-PET阳性病例。pTau217能更好地检测Aβ-PET阳性,与tau-PET的关联性更强。pTau231可以鉴别AD和非AD,与pTau181相似,然而,根据Aβ-PET和tau Braak阶段,pTau231在AD病理的早期阶段开始变化,这表明pTau231作为AD的早期病理标志物可能特别有价值,甚至在症状出现之前就已经存在。pTau形式已被证明可以检测到阿尔茨海默氏症的连续性病理变化,因此可以作为阿尔茨海默氏症的特定诊断标志物。此外,与血浆Aβ42/40不同,血浆pTau 浓度在疾病进展过程中逐渐增加,从而表明,pTau可能对监测疾病阶段有潜在的作用。迄今为止,研究的主要局限性是,它们主要是由几个小组利用回顾性队列完成的,前瞻性验证和纳入更多的异质性人群是一些研究的一些必要的下一步措施。
3.神经丝轻链(NfL)
NfL是一种轴突支架蛋白,是中枢神经系统中两个核心神经丝蛋白之一(另一个是 α-internexin),神经丝对于轴突的生长和稳定以及中枢神经系统的突触组织和功能都是必不可少的。这种生物标志物可以在脑脊液和血液中测量,是第一个被证实具有临床价值的神经特异性生物标志物。在神经炎症和神经退行性疾病中,CSF和血液中的NfL之间的相关性很好(r值为0-70-0-97).NfL浓度最高的是额颞叶、血管和HIV相关的痴呆,以及肌萎缩性脊髓侧索硬化症和非典型帕金森病。在散发性AD中,CSF NfL在AD相关液体生物标志物中显示出第二高的倍数变化(仅次于CSF tTau). 因此,NfL可被用作初步诊断测试,如果呈阳性,可进行更多的检查,以获得更具体的结果,更好地了解神经变性的根本原因。NfL还可以作为疾病严重程度的生物标志物,用于疾病调节治疗的临床试验,并在临床实践中优化和监测治疗效果,这与它在多发性硬化症中的应用相似。
4.神经胶质纤维酸性蛋白(GFAP)
GFAP是星形胶质细胞的一个主要细胞骨架成分,在AD中,反应性星形细胞增多症已被认为是AD的潜在驱动因素或影响疾病的病理变化。通过超灵敏的免疫分析法,在AD患者中,血浆或血清中的GFAP浓度会升高。此外,血浆或血清GFAP的增加也与临床上的疾病的严重程度有关,在患有轻度认知障碍的患者,血浆GFAP预测了AD的后续发展。在认知能力未受影响的人中,血清中GFAP的浓度越高,与认知能力下降的速度、更高的痴呆症风险有关。值得注意的是,血浆或血清GFAP的预测价值是独立于血浆的 Aβ42/40. 由于星形胶质细胞的激活不是AD病理生理学所特有的,GFAP可能是其他类型痴呆的潜在生物标志物。但是,还需要进一步的研究来确定这些潜在因素在不同类型的痴呆症和神经退行性疾病中的临床应用。
Part.02
遗传性阿尔茨海默病的血液生物标志物
AD在少数情况下有一个单基因确定的病因,即PSEN1、PSEN2或APP基因的突变,或APP基因的增殖基因。遗传性AD的特点在于发病年龄小(平均40-60岁),这减少了老龄化对生物标志物浓度的干扰。自从引入高灵敏度的检测方法后,很多研究都分析了遗传性AD患者的血浆Aβ、pTau和NfL(但尚未分析GFAP)。 1.血浆Aβ1-42增加与散发性AD相反,在常染色体显性AD携带者中检测到较高的血浆Aβ1-42浓度和Aβ42/40,然而,在遗传性AD中,血浆Aβ1-42浓度的动态变化还没有被完全了解。总的来说,在遗传性AD中,血浆中的Aβ 浓度会增加,并在一生中波动,这取决于遗传变异和患者的疾病阶段,这些关系的机制还没有被完全解释。 2.血浆pTau和NfL增加 遗传性AD患者的pTau和NfL的生物标志物动态与散发性AD患者的研究结果一致。pTau181和pTau217的血浆浓度在常染色体显性AD症状发生前16-24年开始增加, 这与Aβ-PET和CSF Aβ测量的大脑中淀粉样物质积累的开始相一致。在显性遗传AD队列研究中,大约在症状发生前16年,血液中NfL的浓度也在早期增加。与散发性AD相似,在有症状者中观察到NfL浓度的持续增加。在唐氏综合症患者中,痴呆发病前20多年,血浆NfL也就已开始增加。这些关于遗传性AD的发现,支持了血浆pTau181、pTau217和NfL可能被用于诊断、预后和疾病监测目的,并在病程的早期就可以使用。
 图1:阿尔茨海默病的病理机制及其相关的生物流体生物标志物
3.与异质性相关的因素
随着血液Aβ和tau病理学和神经退行性的生物标志物接近临床使用,了解哪些因素会影响这些标记物的浓度以最好地解释结果是至关重要的(图1).从初级预防的角度来看,与侵入性和昂贵的CSF和神经影像标记物相比,基于血液的生物标志物更合适。年龄、性别、合并症、药物治疗、生活方式因素和遗传变异等因素都会影响血液生物标志物的临床结果。体重指数(BMI)、心血管合并症、肾脏疾病等也会影响血液中生物标志物的浓度。
图1:阿尔茨海默病的病理机制及其相关的生物流体生物标志物
3.与异质性相关的因素
随着血液Aβ和tau病理学和神经退行性的生物标志物接近临床使用,了解哪些因素会影响这些标记物的浓度以最好地解释结果是至关重要的(图1).从初级预防的角度来看,与侵入性和昂贵的CSF和神经影像标记物相比,基于血液的生物标志物更合适。年龄、性别、合并症、药物治疗、生活方式因素和遗传变异等因素都会影响血液生物标志物的临床结果。体重指数(BMI)、心血管合并症、肾脏疾病等也会影响血液中生物标志物的浓度。
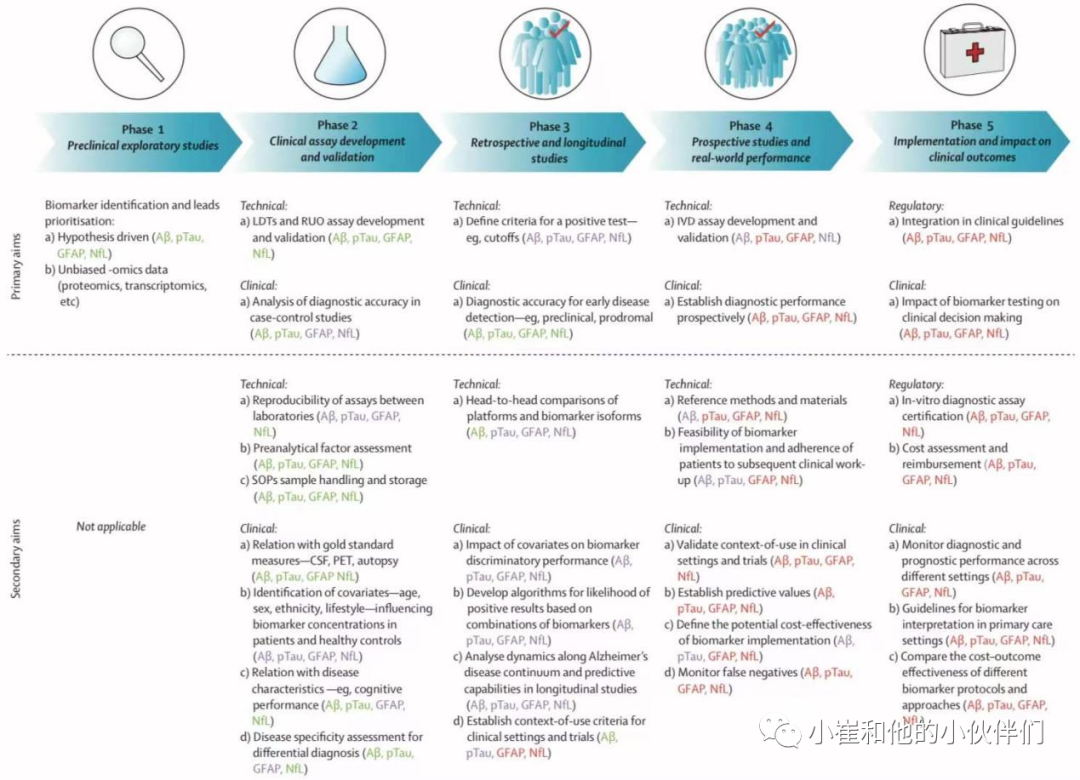 图2:诊断阿尔茨海默病的血液生物标志物的五个阶段发展路线图
图2:诊断阿尔茨海默病的血液生物标志物的五个阶段发展路线图
Part.03
走向临床实施之路
日内瓦路线图描述了生物标志物开发的五个阶段的框架,在最初的探索性研究(第一阶段)之后,需要进行生物标志物的临床检测开发和验证(第二阶段)。在第三阶段,应在回顾性和纵向队列中研究生物标志物的使用,然后在真实环境中的前瞻性验证研究中评估生物标志物(第四阶段),最后一个阶段 (第五阶段)侧重于临床实施。作者对这个路线图进行了调整,增加了血源性生物标志物的技术分析方面(图2).对于Aβ、pTau和NfL,实施路线图的第1和第2阶段已在很大程度上得到解决。GFAP的第1和第2阶段以及所有生物标志物的第3阶段生物标志物的研究正在进行。第4和第5阶段仍然需要解决所有生物标志物的问题。在检测要求方面,路线图的1-3阶段可以使用经过彻底验证的检测或仅用于研究的检测(组2)。 组2:体外生物标志物检测的术语
在试验或临床实践中实施生物标志物的另一个相关前提条件是:制定处理和储存的标准化操作程序。无论使用何种技术,都会对Aβ浓度产生负面影响。然而,这种减少可以通过保持样品低温来缓解,对pTau、NfL.或GFAP也没有观察到反复冻融的影响。一个特别具有挑战性的想法是,生物标志物在无症状和疾病前驱阶段的应用。考虑到血浆pTau181的预测价值与CSF pTau181的预测价值相似,这种个性化的模型也可以为血液生物标志物开发出来。向临床医生和患者传达生物标志物的结果将是施路线图第五阶段的关键,使用血液标志物的主要临床情况见表1。
组2:体外生物标志物检测的术语
在试验或临床实践中实施生物标志物的另一个相关前提条件是:制定处理和储存的标准化操作程序。无论使用何种技术,都会对Aβ浓度产生负面影响。然而,这种减少可以通过保持样品低温来缓解,对pTau、NfL.或GFAP也没有观察到反复冻融的影响。一个特别具有挑战性的想法是,生物标志物在无症状和疾病前驱阶段的应用。考虑到血浆pTau181的预测价值与CSF pTau181的预测价值相似,这种个性化的模型也可以为血液生物标志物开发出来。向临床医生和患者传达生物标志物的结果将是施路线图第五阶段的关键,使用血液标志物的主要临床情况见表1。
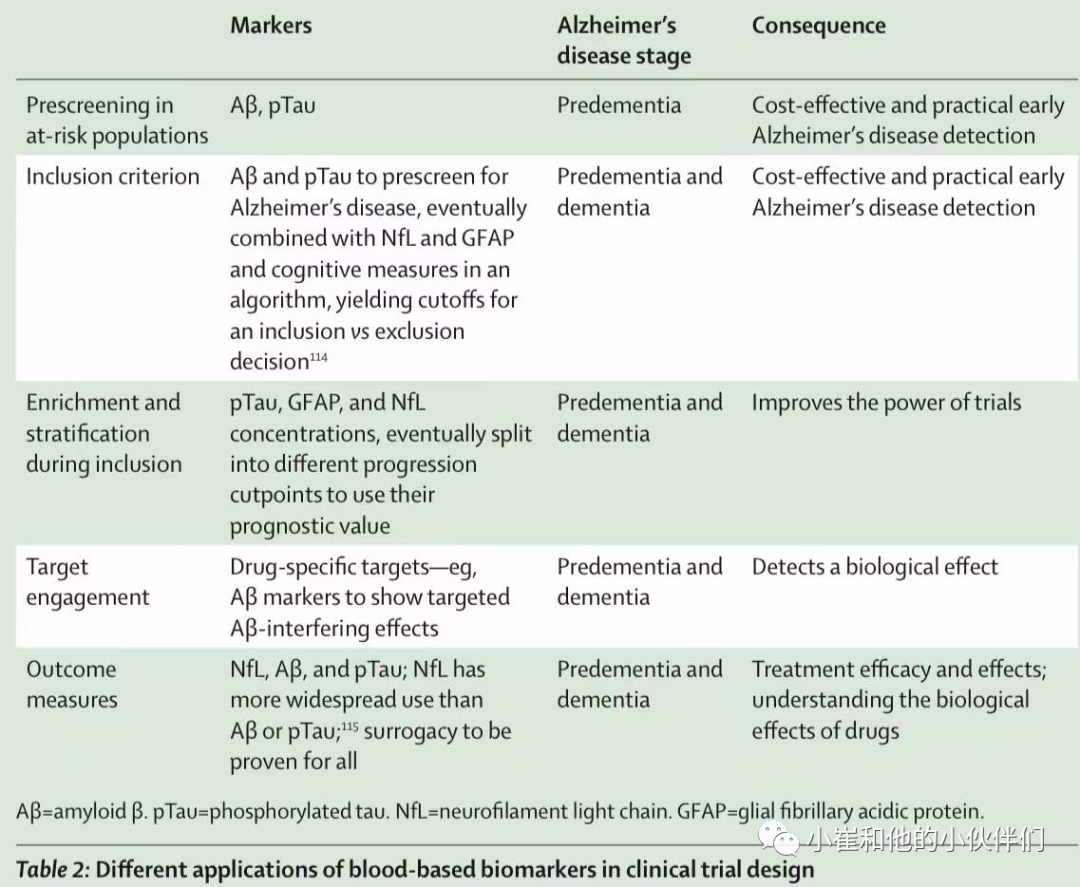 表1:基于血液的生物标志物的不同诊断应用场景
在记忆专科诊所使于血液标志物可以在未来3-5年内实施。由于高成本和低可用性,AD的生物标志物如Aβ PET和CSF生物标志物测试受到限制,因此,血液标志物可以实现对AD的广泛测试。预计阿库奴单抗(抗淀粉样蛋白药物)将在世界其他地区获得批准,处于高级测试阶段的其他类似候选药物也有望获得批准,这会加速将血液标志物引入诊所。
AD的新型血液标志物的问世,将会改善疾病的评估、疗法。血液标志物有可能被用作纳入标准或评估治疗效果(表2)。使用血液生物标志物来检测是否存在AD的病理特征(例如,淀粉样斑块和tau缠结 斑块和tau缠结),对选择符合治疗条件的人(如阿库奴单抗)非常重要。血液中的生物标志物有助于监测生物疗效(如血浆Aβ和pTau)、治疗效果、副作用以及延长用药间隔的安全性。在这种情况下,与CSF标志物和成像相比,血液标志物更具有优势,因为它们具有非侵入性,成本较低,对病人和医疗系统的负担较小。
表1:基于血液的生物标志物的不同诊断应用场景
在记忆专科诊所使于血液标志物可以在未来3-5年内实施。由于高成本和低可用性,AD的生物标志物如Aβ PET和CSF生物标志物测试受到限制,因此,血液标志物可以实现对AD的广泛测试。预计阿库奴单抗(抗淀粉样蛋白药物)将在世界其他地区获得批准,处于高级测试阶段的其他类似候选药物也有望获得批准,这会加速将血液标志物引入诊所。
AD的新型血液标志物的问世,将会改善疾病的评估、疗法。血液标志物有可能被用作纳入标准或评估治疗效果(表2)。使用血液生物标志物来检测是否存在AD的病理特征(例如,淀粉样斑块和tau缠结 斑块和tau缠结),对选择符合治疗条件的人(如阿库奴单抗)非常重要。血液中的生物标志物有助于监测生物疗效(如血浆Aβ和pTau)、治疗效果、副作用以及延长用药间隔的安全性。在这种情况下,与CSF标志物和成像相比,血液标志物更具有优势,因为它们具有非侵入性,成本较低,对病人和医疗系统的负担较小。
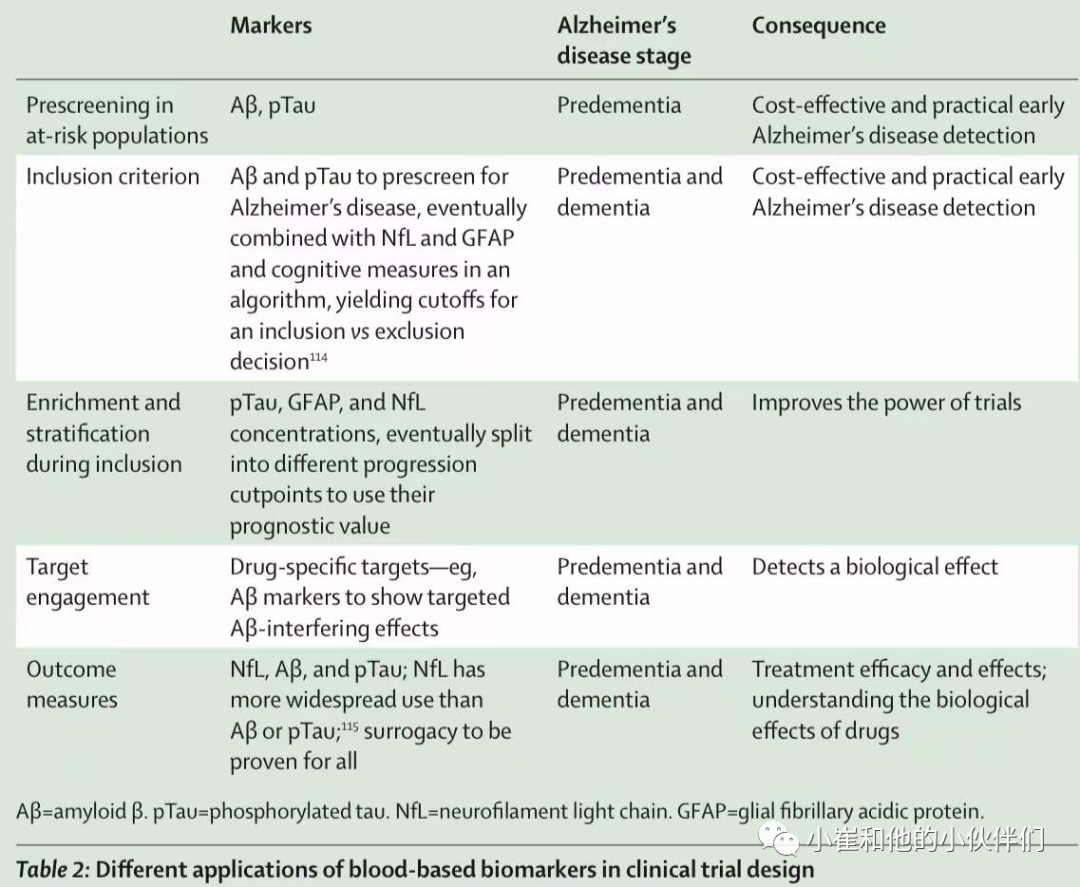 表2:血液生物标志物在临床试验设计中的不同应用
表2:血液生物标志物在临床试验设计中的不同应用
Part.04
总结与展望
由于有了超灵敏的检测方法,使血液生物标志物进行AD的诊断和预后已接近临床应用。作者认为血液AD生物标志物将很快好用于临床--甚至更早用于临床试验,这些进展也为开发新型神经特异性蛋白生物标志物带来了希望。反映AD病理全面复杂性的血液生物标志物相对缺乏(图1),如小胶质细胞激活或突触功能障碍的生物标志物。随着可行的基于血液的阵列和高通量蛋白质组学技术的出现,新的生物标志物可以被发现。血液生物标志物的验证和实施将促进精准医疗的发展。重要的是,从AD生物标志物领域获得的知识将为解决下一个重要的、未得到满足的临床需求铺平道路:确定特定的生物标志物,以支持其他类型的痴呆症的诊断和治疗方法的开发。 精读原文链接: Teunissen Charlotte E,Verberk Inge M W,Thijssen Elisabeth H et al. Blood-based biomarkers for Alzheimer's disease: towards clinical implementation.[J] .Lancet Neurol, 2021, undefined: undefined. 编 译 / 李传兴 校 审 / 梁春梅- END -



