Front Immunol:IgA肾病风险预测模型比较的验证研究
时间:2022-01-31 10:20:24 热度:37.1℃ 作者:网络

免疫球蛋白A肾病(IgAN),最早由Berger在1968年描述,是世界范围内最常见的肾小球肾炎类型,也是终末期肾病(ESRD)的重要原因。重要的是在诊断时确定高危患者,不仅对治疗策略和临床试验的选择,而且对患者健康教育。近几十年来,有报道称数十个临床危险因素,包括蛋白尿、高血压和肾活检时估计的肾小球滤过率(eGFR)与IgAN中较差的肾脏预后相关。除了基线临床参数外,诊断后随访前2年的蛋白尿或血压与IgAN的预后也有明显的相关性。在这些危险因素中,基线eGFR被确定为最一致的指标。该领域的一个突出问题是,结合系膜细胞增生、毛细血管内细胞增生、节段性硬化、间质纤维化等病理指标,能否提高临床指标预测预后的准确性。
我们的目的是验证一个国际合作研究提出的三个IgAN风险模型,以及一个扩展的CKD队列与我们的多中心中国IgAN队列产生的另一个CKD风险模型。
活检证实的IgAN患者基线时eGFR≥15 ml/min/ 1.73 m2,至少随访6个月。主要结果为综合结果(eGFR或ESRD下降50%)和ESRD。这些模型的性能是通过鉴别、校准和重新分类来评估的。
共有2300例符合条件的病例登记。在中位随访30个月期间,288例(12.5%)患者达到复合结局,214例(9.3%)患者达到ESRD。使用复合结果进行分析,临床、Limited、Full和CKD模型具有相对良好的性能,C统计量相似(分别为0.81、0.81、0.82和0.82)。以ESRD为终点时,4种预测模型的预测效果均较好(C统计量均为> . 0.9)。亚组分析显示,对于基线eGFR较高(≥60 ml/min/1.73 m2)的低危患者,包含临床和病理变量的模型(Full模型和Limited模型)比只包含临床指标的模型(clinical模型和CKD模型)具有更好的鉴别能力。
总之,我们在中国IgAN队列中验证了最近报道的IgAN和CKD风险模型。与单纯临床模型相比,添加病理变量可以提高基线eGFR≥60 ml/min/1.73 m2的低风险IgAN患者的ESRD预测能力。

表1 预测5年复合结局(50% GFR下降或ESRD)和ESRD的不同模型的拟合优度。
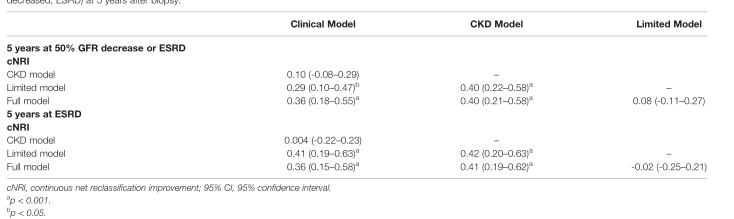
表2 对于总组,比较模型在活检后5年验证队列中预测两种结果风险的辨别性能(ESRD或50% GFR下降;ESRD)。
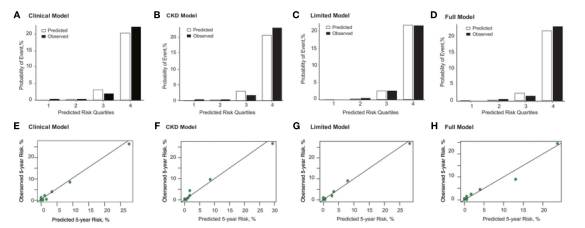
图1 |使用临床模型(A, E)、CKD模型(B, F)、有限模型(C, G)和完整模型(D, D)观察到的与预测的5年ESRD的概率和校准曲线H).预测和观测事件概率估计表示风险预测模型的平均预测概率和被分成预测概率四分位数的总体的平均观测概率。对于这些模型,风险组基于线性预测器的第16(最低风险)、第16 - 50(中等风险)、第50 - 84(较高风险)和高于第84(最高风险)百分位。在临床模型中,四分位数1至4的平均预测概率(%)vs.观察概率(%)类别分别对应0.02% vs. 0.35%、0.25% vs. 0.33%、3.14% vs. 2.00%和20.36% vs. 22.26%;CKD模型分别为0.03% vs. 0.35%、0.24% vs. 0.33%、3.01% vs. 1.67%和20.65% vs. 22.97%;有限模型分别为0.03%:0.00%、0.21%:0.33%、2.53%:2.50%、21.74%:21.55%;全模型分别为0.03%对0.00%、0.22%对0.50%、2.42%对1.50%和21.95%对23.32%。此外,Hosmer-Lemeshow检验表明,有种族的全模型p值>0.05,即模型拟合优度是可接受的。

图2 |不同亚组四种模型预测5年ESRD的生存ROC曲线。临床模型、CKD模型、有限模型和完全模型在总患者中的曲线下面积(AUC)和95% CI (A);基线eGFR < 60 ml/min/1.73 m2的患者(B);基线eGFR≥60 ml/min/1.73 m2的患者(C)。
原文出处:Ouyang Y, Zhao Z, Li G,et al.A Validation Study Comparing Risk Prediction Models of IgA Nephropathy.Front Immunol 2021;12


