ASH 2022:辉瑞CD3/BCMA双抗Elranatamab治疗RRMM结果公布
时间:2022-12-13 18:00:51 热度:37.1℃ 作者:网络
辉瑞的Elranatamab目前处于III期临床阶段,是继强生teclistamab之后,进展最快的CD3/BCMA双抗。本次大会上,辉瑞公布了2项关于Elranatamab的临床结果。Elranatamab前不久刚刚获得FDA突破性疗法认证。
MagnetisMM-1研究
MagnetisMM-1是正在进行的首个人体研究,截至2022年6月22日,共有55名患者接受了elranatamab(≥215μg/kg,SC)单药治疗。患者既往治疗中位线数为5(范围2-14)。
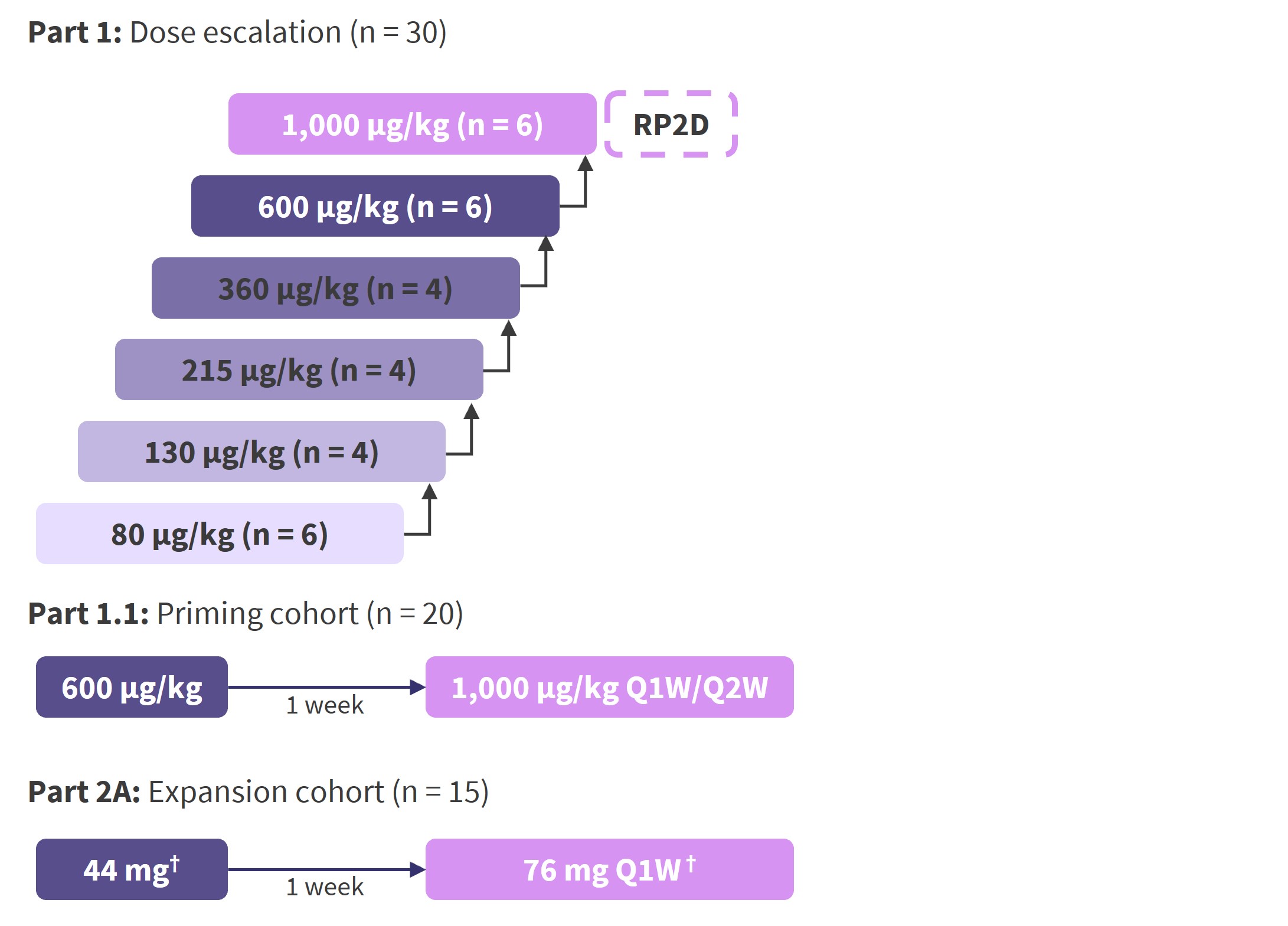
中位随访12.0个月(范围 0.3-29.0),根据国际骨髓瘤工作组(IMWG)确认的ORR为64%,56%患者达到VGPR或更好,38%(21/55)达到CR或更好。即使之前接受过BCMA靶向治疗(抗体药物偶联物、嵌合抗原受体T细胞治疗或两者)的13名患者中,也获得54% (7/13) 的缓解,其中46% (6/13)获得了VGPR或更好,初步证明了elranatamab仍具备了抢夺BCMA靶向疗法难治性患者的潜力。
最常见的TEAE包括CRS、中性粒细胞减少、贫血、注射部位反应和淋巴细胞减少。推荐剂量(1000µg/kg或76mg)的CRS总发生率为67%,仅限于1级 (33%) 或2级(33%),没有3级或更高级别的事件。
Magnetismm-3研究
MagnetisMM-3 研究的队列 A 招募了 123 名多发性骨髓瘤患者,这些患者至少对一种蛋白酶体抑制剂、一种免疫调节药物和一种抗 CD38 抗体无效。 患者接受过的既往治疗中位数为 5.0(范围 2-22),大多数为三级难治性 (96.7%),近一半为五级难治性 (42.3%)。
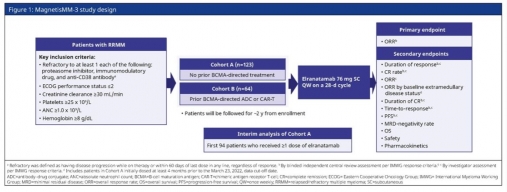
在治疗的第一周,患者接受了 elranatamab 递增皮下给药以减轻不良事件。 递增剂量包括第 1 天 12 mg elranatamab,然后第 4 天 32 mg。第一周后,每周一次皮下注射 elranatamab 76 mg。 递增剂量是在研究的后期开始的,123 名患者中有 119 名接受了这种方式的治疗。 对乙酰氨基酚、苯海拉明和地塞米松的术前给药也在前 3 剂 elranatamab 之前给药。
患者的中位年龄为 68 岁(范围 36-89),ECOG 体能评分为 0(36.6%)、1(57.7%)和 2(5.7%)。 大多数是男性 (55.3%),大多数是白人 (58.5%)。 四分之一的患者 (25.2%) 存在高危细胞遗传学,近三分之一的患者存在髓外疾病 (31.7%)。 根据修订后的多发性骨髓瘤国际分期系统,15.4% 的患者为 III 期疾病,其余患者为 I 期 (22.8%)、II 期 (55.3%) 或未知 (6.5%)。
在 ASH 报告的数据截止日期,即 2022 年 10 月 14 日,中位随访时间为 10.4 个月,中位治疗持续时间为 5.6 个月。 在分析时尚未达到中位反应持续时间,在数据截止时仍有 77.3% 的反应仍在进行中 (n = 58/75)。 9 个月持续缓解率为 84.4%,9 个月无进展生存率为 63.0%。
停用 elranatamab 的主要原因是疾病进展 (35.0%),其中 10.6% 因不良事件 (AE) 和 6.5% 因死亡而停用 elranatamab。 TEAE 导致 15.4% 的患者永久停用 elranatamab。 最常报告的严重程度为 3/4 级的 TEAE 是中性粒细胞减少症 (48.0%)、贫血 (36.6%)、淋巴细胞减少症 (24.4%)、血小板减少症 (22.0%)、COVID-19 (11.4%) 和低钾血症 (9.8%) ). 研究中有 21 例 5 级 TEAE,其中 2 例被研究人员认为与治疗相关(假单胞菌肺炎和发育迟缓)。
66.7% 的患者报告了任何级别的感染,其中 35.0% 的患者经历了 3/4 级感染。 25.2% 的患者经历过任何级别的 COVID-19 相关 TEAE。 感染导致 6.5% 的患者永久停用 elranatamab。 在研究过程中,40.7% 的患者接受了静脉注射免疫球蛋白以抵抗感染。 26% 的患者出现注射部位反应,严重程度均为 1/2 级。
使用美国移植和细胞治疗学会标准评估细胞因子释放综合征 (CRS) 和免疫效应细胞相关神经毒性综合征 (ICANS),所有事件的严重程度均被视为 1 级或 2 级。 在接受递增剂量的患者中,56.3% 的患者出现 CRS,3.4% 的患者出现 ICANS。 在 CRS 或 ICANS 患者中,分别有 22.7% 和 1.7% 接受了托珠单抗(Actemra)治疗,分别有 8.4% 和 1.7% 接受了类固醇治疗。 CRS/ICANS 的中位解决时间为 2.0 天,并且没有因这些 AE 而停药。 CRS 发生较早,90.6% 的病例发生在升级阶段,98.8% 的事件发生在前 3 剂中。
更多的研究
有几项正在进行的 3 期研究探索 elranatamab 单独或联合治疗多发性骨髓瘤患者。 3 期 MagnetisMM-5 研究 (NCT05020236) 正在评估 BCMA/CD3 双特异性药物作为单一药物,并与 daratumumab (Darzalex) 联合治疗复发/难治性多发性骨髓瘤患者。 3 期 MagnetisMM-7 研究 (NCT05317416) 正在研究将 elranatamab 作为新诊断多发性骨髓瘤患者的维持治疗与来那度胺进行比较。
参考资料:
- Bahlis NJ, Tomasson MH, Mohty M, et al. Efficacy and Safety of Elranatamab in Patients with Relapsed/Refractory Multiple Myeloma Naïve to B-Cell Maturation Antigen (BCMA)-Directed Therapies: Results from Cohort A of the Magnetismm-3 Study. Blood. 2022;140(suppl 1):391-393. doi:10.1182/blood-2022-162440
- Pfizer’s elranatamab granted FDA breakthrough therapy designation for relapsed or refractory multiple myeloma. News release. Pfizer Inc. November 3, 2022. Accessed December 10, 2022. bit.ly/3T20rbE


