【协和医学杂志】胸部增强CT结合支气管内超声诊断无症状支气管Dieulafoy病一例
时间:2023-08-17 17:47:45 热度:37.1℃ 作者:网络
Dieulafoy病由法国医生Dieulafoy于1898年首次提出,是一种相对罕见但可能危及生命的疾病,该病可能发生异常黏膜下小动脉(又称黏膜下恒径动脉,最常见于胃黏膜)出血,进而导致严重的胃肠道出血。
而支气管Dieulafoy病则更为罕见,直至1995年才由Sweerts等[1]首次报道,其典型特征为支气管黏膜下存在1条发育异常的动脉[2],多数患者由于反复咯血或支气管镜下活检不慎而导致大出血,通过血管造影术或病理诊断而确诊。
然而,有多例报道因支气管镜下活检而导致患者大出血死亡[3-4],严重威胁患者生命安全。与血管造影术及病理诊断相比,支气管内超声(EBUS)及彩色多普勒血流显像具有无创、安全且更加简单易行的优点,该病在胸部增强CT动脉期可见异常动脉血管强化以及支气管黏膜下病灶超声特征、血流情况,能够区分血管或实性病变。
本文报道1例采用胸部增强CT结合EBUS诊断的支气管Dieulafoy病,并结合相关文献对该病的临床表现、病理特点及治疗进行分析,以提高临床医生对该疾病的认识,防止行支气管镜下活检而导致严重出血,探索更为安全有效的临床诊断方法。
1 病例资料
患者男性,56岁,于2021年6月10日体检时行胸部CT平扫发现肺窗左主支气管内结节样新生物(直径约为0.5 cm),肺窗及纵隔窗皆可见(图1A,1B)。
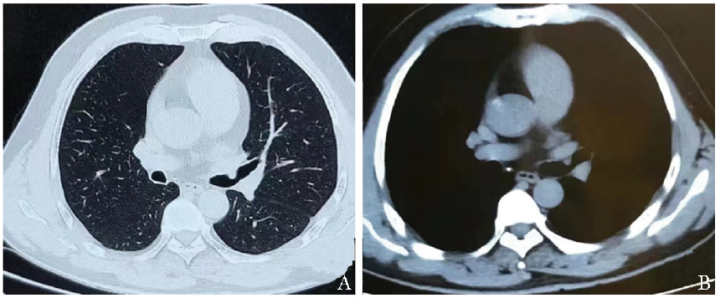
图1A,1B 胸部CT平扫
患者身体健康,偶有咳嗽,少量白痰,无咯血、痰中带血、胸痛等不适。既往史:每日吸烟40支,持续吸烟40余年。于当地医院行支气管镜检查,见左主支气管远端新生物,未行活检,为进一步诊治于2021年7月2日就诊于北京协和医院呼吸与危重症医学科。
门诊行胸部增强CT示左主支气管内结节样新生物,突入管腔的部分动脉期强化明显(图1C),行支气管镜检查示左主支气管远端黄豆粒大小结节样黏膜隆起,表面光滑,可见细小血管,未见搏动(图1D),支气管内超声探查该隆起部位黏膜下为粗大血管,可见明显彩色血流信号(图1E)。根据上述表现考虑诊断为支气管Dieulafoy病,为避免引发大出血,未行支气管镜下活检。
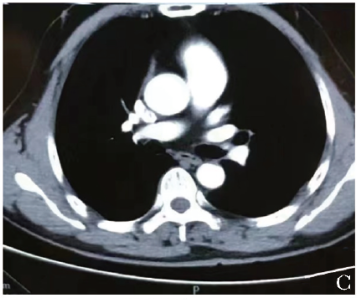
图1C 胸部增强CT扫描
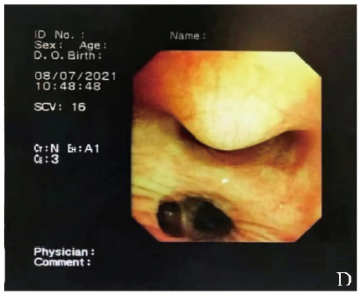
图1D 支气管镜检查
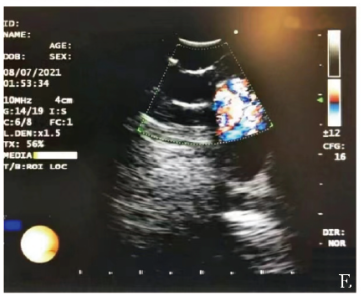
图1E 支气管内超声检查
2 讨论
以“Dieulafoy's disease”“bronchial Dieulafoy's disease”“支气管Dieulafoy病”“Dieulafoy病”为检索词,在PubMed、万方数据知识服务平台和中国知网数据库进行文献检索,检索时间为2010年1月至2022年7月,并进行文献复习。
目前支气管Dieulafoy病的发病机制尚不清楚,多数学者认为,该疾病属于先天性发育不良,且大部分患者有吸烟史或呼吸道疾病史,因此该病可能与长期吸烟或慢性感染所致的气道慢性炎症或损伤有关。该病的临床特点为男性多于女性(比例约为2:1),中年人发病率较高,右肺的发生率高于左肺[5-6]。
临床表现方面,该疾病不具有特异性,临床症状主要包括反复咯血、咳嗽、气短、胸部不适等,也可无任何症状表现而在体检时发现。大多数患者出现咯血症状[3],其原因可能是由炎症或损伤等外部因素所致,也可能是自发破裂出血,但高血压、糖尿病、心血管疾病或其他因素是否参与其中,目前尚不清楚[7]。
1 辅助检查方面:
病理诊断虽作为支气管Dieulafoy病诊断的金标准,术后病理或尸检提示支气管黏膜下结缔组织纤维内可见含弹力纤维的小动脉血管壁,但因活检具有潜在致死性,其必要性目前尚存有争议[8-9]。有研究报道19例支气管Dieulafoy病患者通过支气管活检进行病理诊断,仅5例可见动脉血管壁,17例发生出血,其中6例死亡[3]。
2 胸部CT平扫可表现为磨玻璃影、结节影、肺炎样渗出等。有病例报道,胸部CT平扫表现为肿块样改变、阻塞性肺不张,支气管镜检查发现管腔狭窄、黏膜肿胀,行活检后发生大出血,行支气管动脉栓塞术可见病灶处迂曲血管,最终因广泛血管内凝血及多器官功能衰竭而死亡[4]。
3 支气管镜检查更加直观,但镜下表现多种多样。一项纳入64例患者的研究显示,支气管镜下Dieulafoy病常表现为结节样隆起(39/64)、出血点或血凝块(15/64),仅1例病灶处为白色小点,2例表现为正常黏膜[3]。
4 对于怀疑Dieulafoy病的患者,可行胸部增强CT进一步明确病灶中是否存在血管强化,胸部增强CT动脉期可见异常动脉血管的强化,也能评估病灶及周围组织血供情况。
5 支气管动脉造影可见迂曲的肺内血管畸形、支气管动脉扩张、动脉异常、血管分流、瘘管和造影剂外渗入肺部,但无法显示肺动脉病变[10-11]。
6 目前,已有多项研究报道EBUS检查可见支气管黏膜下病灶的血流情况,能够区分血管性病变或实性病灶,有效诊断支气管Dieulafoy病[12-16]。对于黏膜结节样隆起性病变,如黏膜表面正常,可先行EBUS检查,如病灶黏膜下存在粗大彩色血流信号,则可辅助诊断,避免因盲目活检而导致的致死性大出血,但常规EBUS镜头难以到达上叶及远端支气管,可采用超声小探头支气管镜技术(R-EBUS)实现这一操作[8],由于EBUS检查同样会对支气管壁有摩擦,对于有大咯血的患者,不建议行EBUS检查[17]。
目前, 主要是针对出现咯血症状的支气管Dieulafoy病患者进行治疗,对于无咯血症状的患者可暂行观察或保守治疗。Qian 等[3]报道70例支气管Dieulafoy病患者,其中7例未出现咯血症状。
贾卫红等[18]报道30例支气管Dieulafoy病患者,其中26例发生咯血,其余4例无咯血症状,30例患者均进行支气管检查,多数行支气管动脉造影,检查结果显示局部黏膜隆起5例,结节样改变25例(其中光滑结节21例,桑葚样结节、蓝色蚯蚓状凸起、息肉样和新生物样结节各1例)。
杨瑞红等[19]报道的22例支气管Dieulafoy病患者中15例发生大咯血。对于支气管出血患者,虽反复出血但出血量不大,可经气管镜行氩等离子电凝止血治疗[20-21]。对于大咯血患者,由于出血来源于动脉,出血速度快且出血量较大,可行支气管动脉栓塞术或支气管电凝止血[7],但支气管动脉栓塞术成功率仅为71%[5],原因可能是支气管Dieulafoy病的动脉来源除大部分为支气管动脉,少部分来自于肺动脉[19],行支气管动脉栓塞术后,有可能血管再通导致再次出血,如果手术失败,可考虑行肺叶切除根治术[7]。
综上,由于支气管Dieulafoy病报道较少,易被忽视,对于不明原因咯血患者,应注意筛查该病,支气管动脉造影能够对该病进行诊断,且通过支气管动脉栓塞术达到治疗目的;对于未发生咯血的患者,仅有咳嗽等轻微症状,或通过体检及支气管镜检查时发现病灶,如支气管镜检查有主气道结节样新生物,如表面光滑、表面分布血管、可见搏动,可采用胸部增强CT扫描结合EBUS探查病灶支气管黏膜下血流情况,能够有效诊断支气管Dieulafoy病,避免因盲目活检而导致大出血风险,此方法无创、安全且有效易行,值得临床推广应用。
参考文献
[1]Sweerts M, Nicholson AG, Goldstraw P, et al. Dieulafoy's disease of the bronchus[J]. Thorax, 1995, 50: 697-698.
[2]Parrot A, Antoine M, Khalil A, et al. Approach to diagnosis and pathological examination in bronchial Dieulafoy disease: a case series[J]. Respir Res, 2008, 9: 58.
[3]Qian X, Du Q, Wei N, et al. Bronchial Dieulafoy's disease: a retrospective analysis of 73 cases[J]. BMC Pulm Med, 2019, 19: 104.
[4]Zhou P, Yu W, Chen K, et al. A case report and review of literature of Dieulafoy's disease of bronchus: A rare life-threatening pathologic vascular condition[J]. Medicine (Baltimore), 2019, 98: e14471.
[5]Liao SX, Sun PP, Li BG, et al. A rare and fatal respiratory disease: bronchial Dieulafoy's disease[J]. Ther Adv Respir Dis, 2020, 14: 1753466620929236.
[6]Padilla-Serrano A, Estrella-Palomares V, Martínez-Palacios B, et al. A case of massive hemoptysis related to a smoking-history: an acquired form of the Dieulafoy's disease?[J]. Rev Port Pneumol, 2015, 21: 276-279.
[7]Chen W, Chen P, Li X, et al. Clinical characteristics and treatments for bronchial Dieulafoy's disease[J]. Respir Med Case Rep, 2019, 26: 229-235.
[8]van der Werf TS, Timmer A, Zijlstra JG. Fatal haemorrhage from Dieulafoy's disease of the bronchus[J]. Thorax, 1999, 54: 184-185.
[9]Gurioli C, Casoni GL, Gurioli C, et al. Endobronchial ultrasound in Dieulafoy's disease of the bronchus: an additional application of EBUS[J]. Monaldi Arch Chest Dis, 2010, 73: 166-168.
[10]Ganganah O, Guo S, Chiniah M, et al. Endobronchial ultrasound and bronchial artery embolization for Dieulafoy's disease of the bronchus in a teenager: A case report[J]. Respir Med Case Rep, 2015, 16: 20-23.
[11]潘峰, 王芳, 刘卓, 等. 支气管Dieulafoy病的支气管动脉CT造影特点[J]. 中华结核和呼吸杂志, 2018, 41: 949-953.
[12]Colt HG, Davoudi M, Murgu S. Scientific evidence and principles for the use of endobronchial ultrasound and transbronchial needle aspiration[J]. Expert Rev Med Devices, 2011, 8: 493-513.
[13]Mincholé E, Penin RM, Rosell A. The Utility of Linear Endobronchial Ultrasound for the Incidental Finding of Dieulafoy Disease of the Bronchus[J]. J Bronchology Interv Pulmonol, 2018, 25: e48-e50.
[14]Casoni GL, Gurioli C, Romagnoli M, et al. Diagnosis of pulmonary thromboembolism with endobronchial ultrasound[J]. Eur Respir J, 2008, 32: 1416-1417.
[15]胡惠蓉, 曾奕明, 洪苓苓. 气道内超声检查对气道黏膜隆起病变的诊断价值[J]. 中华结核和呼吸杂志, 2016, 39: 514-518.
[16]张建峰, 叶健, 陈灏, 等. 结合气道内超声诊断支气管Dieulafoy病1例[J]. 中国乡村医药, 2015, 24: 70-74.
[17]Chen Y, Mao Y, Cheng X, et al. Case Report: A Case of Infant Bronchial Dieulafoy's Disease and Article Review[J]. Front Pediatr, 2021, 9: 674509.
[18]贾卫红, 杨栋才, 侯飞飞, 等. 支气管Dieulafoy病30例临床误诊分析[J]. 临床误诊误治, 2019, 32: 4-8.
[19]杨瑞红, 李剑锋, 刘军, 等. 支气管Dieulafoy病三例并文献复习[J]. 中华结核和呼吸杂志, 2013, 36: 577-580.
[20]Dalar L, Sökücü SN, Özdemir C, et al. Endobronchial argon plasma coagulation for treatment of Dieulafoy disease[J]. Respir Care, 2015, 60: e11-e13.
[21]刘丽琼, 李艳丽, 刘艳红, 等. 支气管Dieulafoy病的诊治进展[J]. 中华结核和呼吸杂志, 2016, 39: 127-130.


