慢性光化性皮炎发病机制及治疗
时间:2023-08-20 23:38:49 热度:37.1℃ 作者:网络
慢性光化性皮炎(Chronic Actinic Dermatitis,CAD) 旧称光线性类网织细胞增生症,是一多见于中老年男性的以慢性光敏性为特征的病谱性疾病。临床上共分四种类型:持久性光反应、光敏性皮炎、光敏性湿疹及光线性类网织细胞增生症。本病病因机制不清,使CAD的预防和治疗颇为困难。

发病机制
目前CAD发病机制尚未完全阐明,在临床上普遍认为与接触外源性光敏物质、紫外线辐射及自身免疫有关。
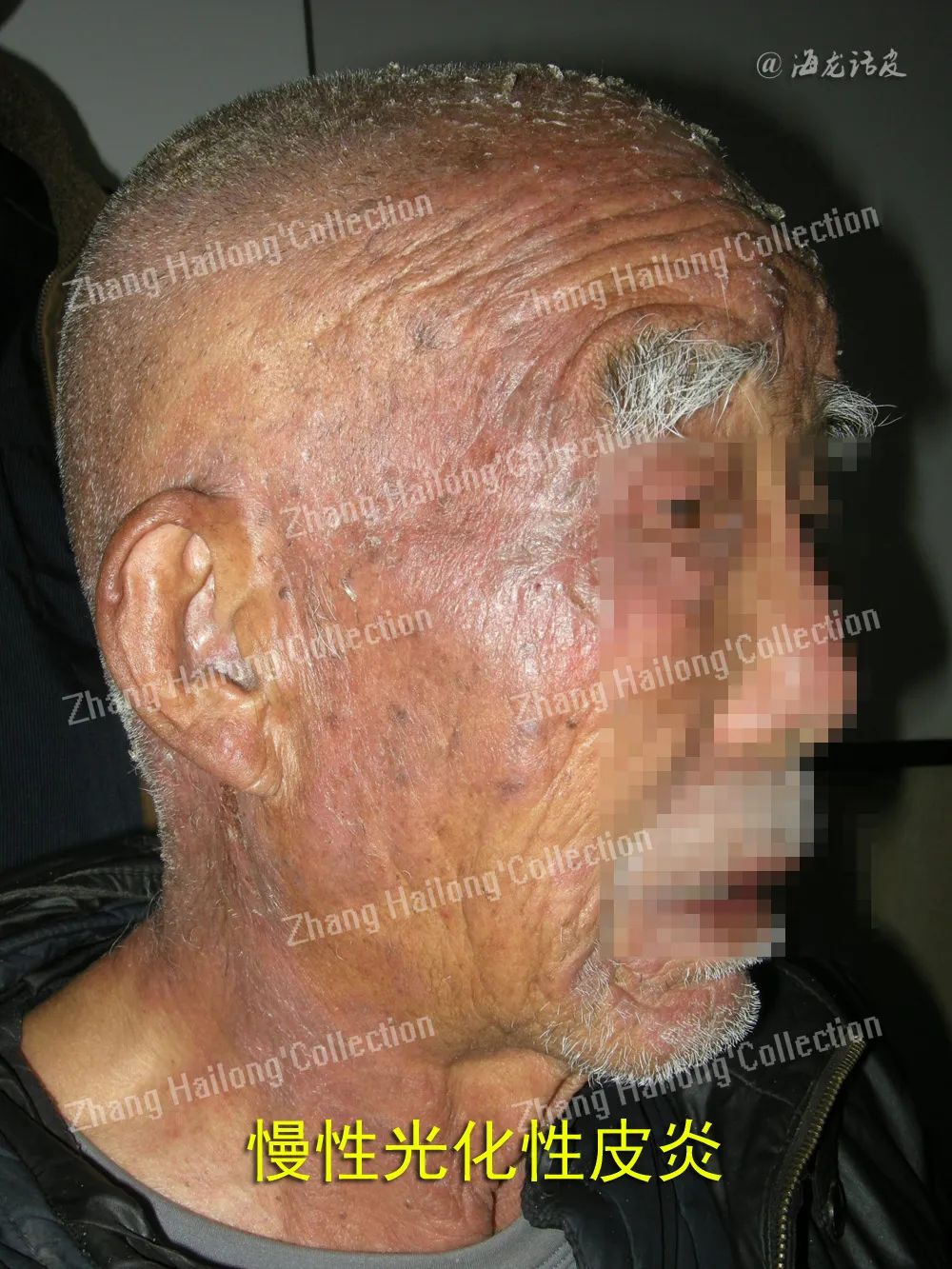
1、光敏物质:
目前认为与外源性光敏物质的接触是诱发CAD发生的因素之一,约75%患者存在光变应原敏感。皮肤吸收或接触外源光敏物质后,在紫外线的作用下与皮肤中某些成分形成半抗原,与机体内生蛋白共价结合形成全抗原,引起湿疹样迟发超敏反应。随着疾病的进展,人体任何部位的皮肤一旦处于紫外线照射下即能形成足够的内源性抗原而引起迟发性超敏反应,在临床上避免接触光敏物质可减轻临床症状。
2、环境因素:
CAD分布广泛,在世界范围内皆有发现,但在肤色深,且日照时间长、气候温暖地区发生率更高。CAD患者数量与空气湿度、日照时间呈正相关,与PM10呈负相关;CAD的发生可根据日照时间和日照强度的增加,提示环境因素在其中的作用。日光主要有三种成分组成,即紫外线(UV)、可见光及红外线;在CAD病人致病因素中UV及可见光占据主要部分。地面紫外线辐射的光谱及强度伴随着海拔变化,Prue H等研究发现地面紫外线辐射约有5%为UVB其余则为UVA。随着环境污染的加重,少数UVC可通过臭氧层空洞到达地表。但部分研究表明短期照射UVC对皮肤的损害有限。
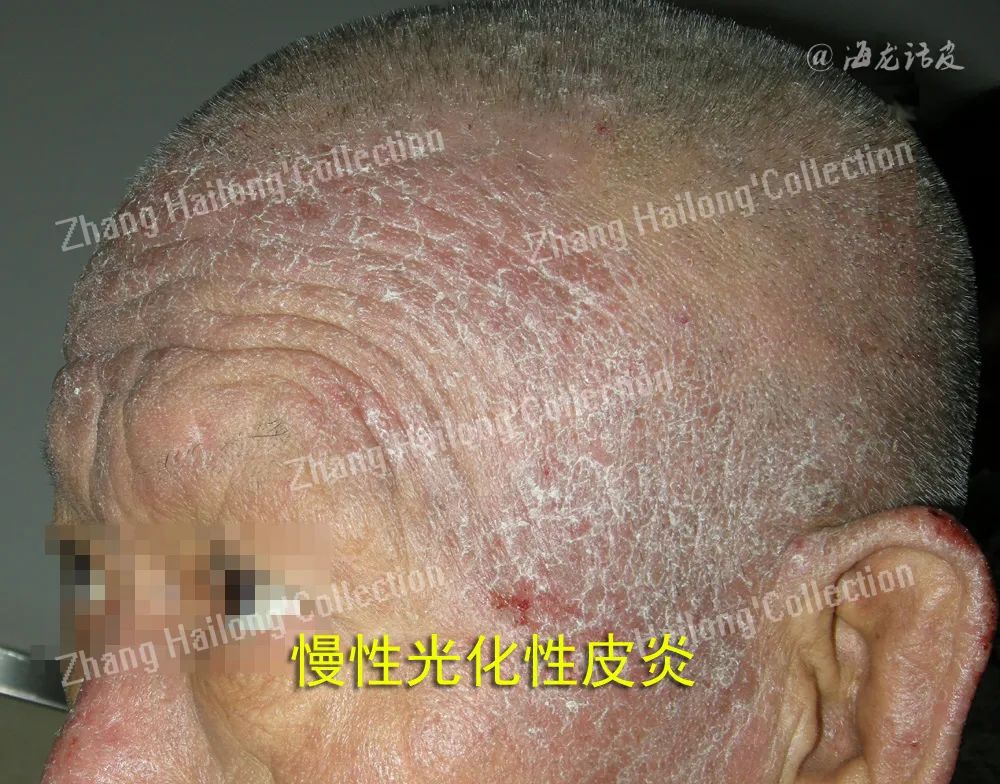
3、免疫反应与免疫应答:
目前认为CAD的发生与机体接触光及光敏物质导致的T淋巴细胞介导的Ⅳ型迟发型变态反应有关。Dongyun L等对mRNA及长链非编码核糖核酸(Long non-coding RNA)进行全基因分析,首次应用核糖核酸测序(RNA-Seq) 评估了CAD患者和健康个体的阳光照射部位皮肤lncRNA和mRNA谱。发现基于lncRNA的顺式调节靶mRNA的KEGG分析中的前20条途径与炎症和免疫反应有关,提示lncRNA相关的炎症和免疫反应功能障碍在CAD的发生中起重要作用。Alafiatayo等发现,在经紫外线处理的正常人皮肤成纤维细胞中观察到趋化因子信号传导途径中MAPK途径相关基因表达上调提示CAD与UV引起的皮肤免疫反应及炎症相关。此外通过免疫抑制药物如硫唑嘌呤、环孢素等对该疾病良好的治疗效果,也在一定程度上反映了本病与免疫反应高度相关。
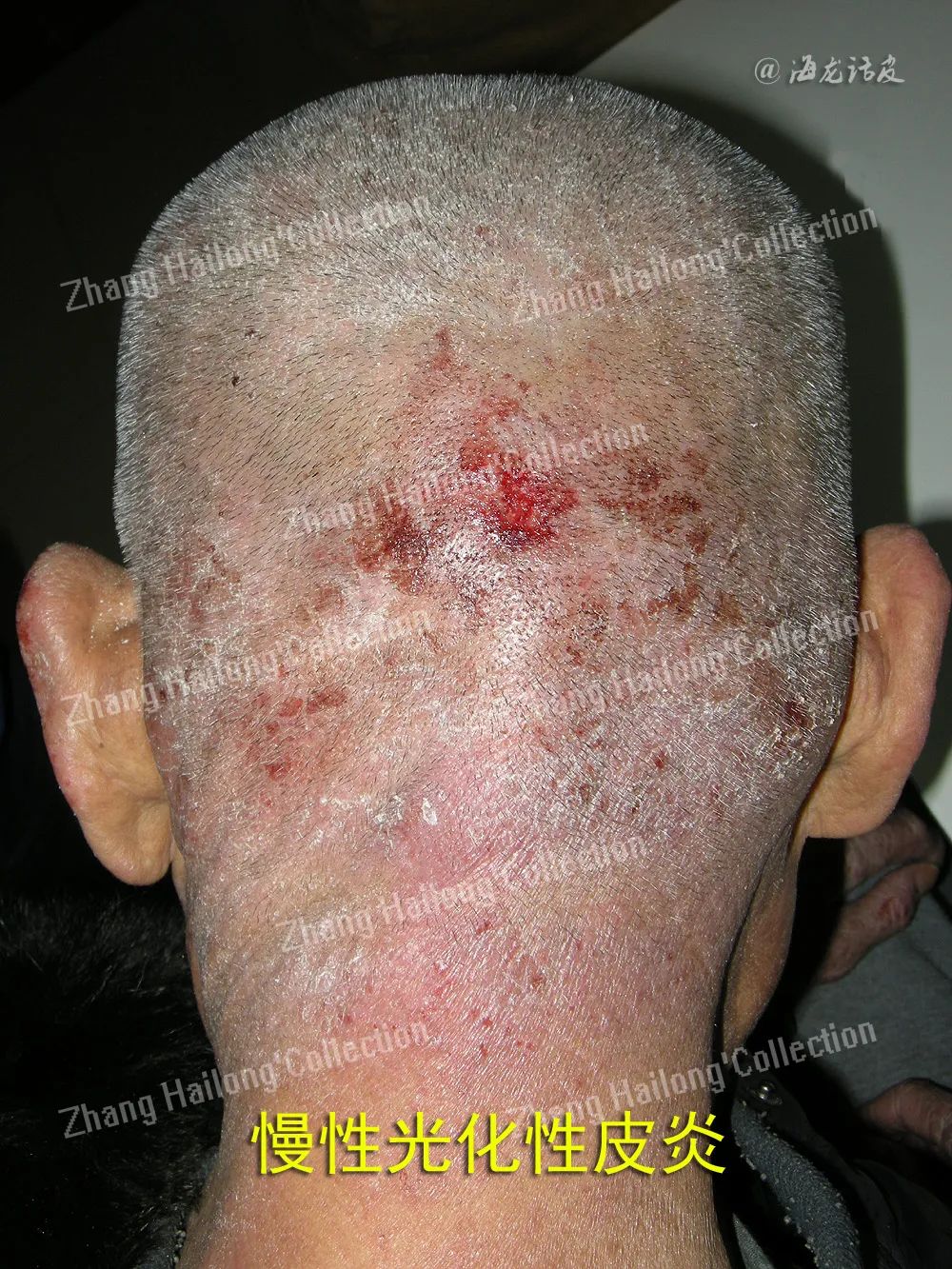
研究表面CAD的发展可能与Caspase-14的异常表达有一定程度的相关。试验表明Caspase-14敲除小鼠对紫外线易感,而在CAD患病因素占主要地位的紫外线也可通过去甲基化的方式对 Caspase-14mRNA以及蛋白的表达产生影响。正常皮肤角质层细胞的细胞核及细胞质表达Caspase-14,且表达最明显部位在角质层,但CAD患者通常在颗粒层及棘层表达Caspase-14,在角质层中的表达不明显。CAD患者角质层中的丝聚合蛋白减少,皮肤屏障功能的受损,将进一步降低患者对UV的抵抗力,加重病情。有趣的是这与特应性皮炎(AD)患者在Caspase-14的表达上存在一定的相似性。且有研究表明AD病程中存在光敏性,10%的患者可被日光照射后引起疾病加重,但这类患者大部分最小红斑量测定无明显异常,而其中3%~10%患者会发生CAD。
治疗
1、预防措施:
CAD患者需减少UV暴露,减少接触可疑光敏物质及减少光敏性食物药物的使用。
一般措施:应避免在强烈日晒时间段外出,如因工作需要等特殊情况,需进行物理防晒,如遮阳伞、太阳镜、口罩及穿戴长袖密织衣物,减少UV和可见光辐射。室内荧光灯的UV辐射也可加重患者病情,因此在室内使用灯光时也应使用UVR最低、带有灯罩的灯。对患者建议行光斑贴检测,嘱避免接触阳性表达的光敏物质,减少光敏性食物及药物的使用。

遮光剂:研究表明,紫外线可加重CAD患者病情,促进皮肤癌的发生。多数CAD患者对UV敏感,因地表紫外线主要有UVA及UVB两大类;在相同的SPF下广谱防晒剂对UVA及UVB的防护有更好的表现,减少了UV引起的免疫反应;因此推荐使用对UVA及UVB均有保护作用的广谱遮光剂。推荐每隔(2~3)h补涂一次在暴露部位、流汗、清洗等情况下也需重复涂抹遮光剂。需注意应根据患者光斑贴结果选择遮光剂,避免遮光剂内成分加重患者病情。
饮食建议:既往研究表明,许多成分可以抵抗UV的损害作用,且因成分天然,对患者有较好的吸引力。如水飞蓟素、姜黄、白藜芦醇及绿茶提取物等被证实具有抗氧化作用,胡萝卜素及白绒水龙骨提取物也被证实可预防光线性皮肤病。但植物提取物的治疗作用偏弱,食用相关成分食物,虽无法取代传统防晒措施,却可以作为辅助治疗手段使用。
心理及健康教育:CAD患者病情常控制不佳、迁延不愈;CAD属于慢性皮肤病,患者身心健康摧残较为严重,对自身病情恢复极不满意,并对诊疗医生持有怀疑态度。因此在对患者进行诊疗期间,需进行一 定的健康教育及心理安抚,有助于患者配合治疗及病情恢复。
2、药物治疗:
局部用药:CAD的局部治疗药物,主要包括糖皮质激素软膏及钙调神经磷酸酶抑制剂软膏两种外用药物。外用糖皮质激素通过抑制免疫反应及炎症反应产生治疗作用,具有价格低、见效快等优点,是目前治疗CAD的一线用药。但长期使用激素类药物会导致涂抹药膏部位的皮肤出现菲薄、萎缩、及毛细血管扩张等不良反应。因此病情缓解后应减量使用或改用弱效激素。在使用激素的同时联合保湿剂治疗可有效降低激素药膏的不良反应。

钙调神经磷酸酶抑制剂,如他克莫司可用于CAD患者治疗,通过阻断淋巴细胞和其他免疫系统细胞的活化,并抑制皮肤肥大细胞及嗜碱性粒细胞释放细胞因子来产生治疗作用。此外,长期使用钙调神经磷酸酶抑制剂不良反应少见,但因其价格较高,其使用受到限制。他克莫司局部使用安全年限被证明为3年,故长期使用时,需对患者进行随访。其他外用药物如阿魏酸:广泛应用于皮肤科,可改善L-抗坏血酸和α-生育酚制剂的稳定性,消除自由基,对细胞内抗氧化体系具有一定的保护作用从而作为皮肤光老化延迟剂及光保护剂。但未在CAD领域进行规模性使用。
系统用药:CAD患者可短期口服糖皮质激素进行短期治疗,如泼尼松(30~50)mg/d,连用2周。欲行光硬化治疗的CAD患者可使用5mg复方倍他米松肌肉注射,预防治不良反应发生。羟氯喹具有抗炎、抑制免疫反应及光保护的作用,但每日使用剂量如大于6.5mg/kg或使用总剂量大于100g有引发眼部损害的风险,因此使用前建议完善眼底检测,患者每次复诊时需计算药物使用剂量,避免副反应的发生。在临床上使用沙利度胺100mg/d对治疗严重、难治性CAD有良好效果。
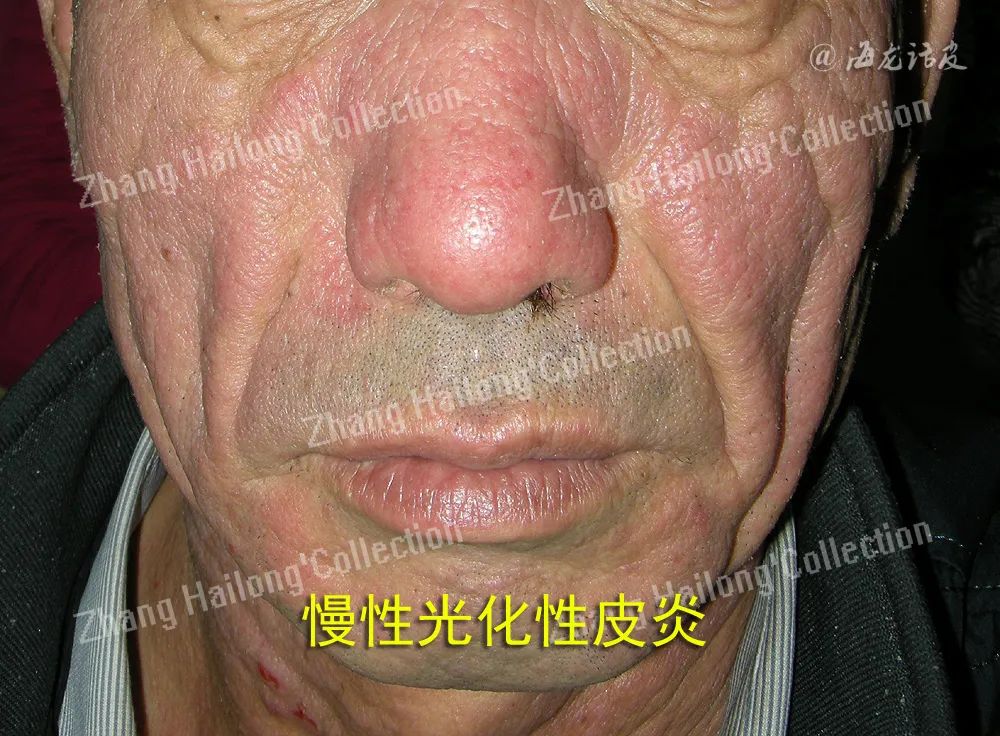
严重CAD患者可以将硫唑嘌呤为治疗首选,150mg/d即可产生良好治疗效果,且价格合理。但硫唑嘌呤可产生药物相关副反应:包括血液系统损伤、肝损伤、胃肠道功能紊乱、感染等。硫唑嘌呤不良反应多见于老年人群,在使用前对患者进行TPMT酶活性检测,避免患者相关酶活性过低,引起严重药物不良反应;并需对患者进行血常规及肝功能检测,动态观察患者血常规/肝功能变化,避免严重副反应的发生。环孢素对大剂量激素治疗效果不佳CAD患者有良好治疗效果,且不良反应较硫唑嘌呤等降低,但价格偏高。值得注意的是,PUVA治疗与环孢素联合使用存在光致癌风险,治疗CAD时应避免联合使用。据报道托法替尼对难治性慢性光化性皮炎疗效较好,每次5mg,2次/d,治疗2个月后,对阳光耐受增加;但停用药物后,再次出现相关临床症状,继续服用托法替尼后症状可再次好转。
生物制剂:国外报道在完善相关检查后(肝炎病毒学及结核相关)对使用口服药物无明显改善的CAD患者予以度普利尤单抗注射液(dupilumab)初始剂量600mg治疗,后每2周300mg维持治疗患者病情得到明显改善。
光硬化治疗:光硬化治疗对CAD患者有预防和治疗的效果。既往研究表明大剂量的紫外线辐射会破坏皮肤屏障,但反复低剂量的紫外线辐射会促使角质层和表皮增厚,增强屏障功能;同时下调皮肤抗原呈递细胞功能和抑制角质形成细胞促炎症细胞因子的分泌,从而阻止或降低CAD患者的异常免疫应答等。因此,光疗和光硬化疗法可有效治疗CAD改善CAD患者的生活质量。波长单一为311nm的NB-UVB,可避免很多紫外线不良反应,如皮肤老化、皮肤晒伤等,现被广泛应用于皮肤科领域;但治疗前应进行测定MED,根据患者MED值来决定的NB-UVB治疗初始剂量。
外科治疗:对各种药物疗效不明显或不耐受,且有强烈改善皮肤状况意愿的CAD患者,可选择外科手段进行治疗。Reichenberger等通过人工磨削术对1例严重CAD 患者进行了治疗,并取得了成功。
总结与展望
综上所述,虽然近年来对CAD的认识不断增加,但对其发生机制仍未认知完全;认为免疫反应、炎症反应及紫外线与该病相关。CAD顽固难愈,需结合患者自身情况,以防晒为基础,辅以传统与现代治疗相结合治疗。
参考文献:
[1]孙思昊,李晔,农祥等.慢性光化性皮炎发病机制及治疗[J].皮肤病与性病,2021,6(43):345-347.


