深度剖析一例新辅助治疗方案联合手术治疗食管癌的临床疗效
时间:2023-11-27 11:28:58 热度:37.1℃ 作者:网络
食管癌是临床常见的消化系统恶性肿瘤,发病率和死亡率分别占全部肿瘤的第7位和第6位。食管癌患者的3年生存率仅为20%-25%,对患者的生命健康造成极大的威胁。研究显示,由于食管解剖位置特殊,早期食管癌无明显症状,而进展期食管癌大部分预后不佳。手术是食管癌的首选治疗方式,但对于进展期,单纯手术肿瘤完全切除(R0)率在30%-50%之间i,病灶难以彻底清除,复发率高是手术治疗的难点所在ii。
如何降低术后复发率、提高远期生存率是食管癌治疗的重点。据研究显示,术前新辅助化疗联合手术可进一步改善食管癌患者的预后,提高生存率。近年来,免疫联合化疗已经成为晚期食管癌一线治疗标准,多项局部晚期食管癌III期免疫联合放疗研究正在进行中。研究结果显示,新辅助免疫联合化疗后行食管癌切除术具有良好的有效性和安全性,且患者有较高的病理完全缓解(pCR)率和R0切除率iii。本文将分享一例斯鲁利单抗联合化疗用于进展期食管癌患者术前新辅助治疗的真实临床病例,供广大同道参考。
病例介绍
一、 基本情况
基本信息:患者男性,59岁;体重57.5kg、身高167cm。
主诉:进行性吞咽困难10天余。
既往史:无特殊,无吸烟、饮酒史。
二、 入院相关检查
2023-01-11胸部CT平扫+增强示:
食管胸中下段管壁增厚,局部呈软组织块影,大小约2.7cmX5.2cmX3.3cm,增强见强化,相应管腔变窄,周围脂肪间隙模糊,纵隔及双侧锁骨下区见多发淋巴结影,增强强化不均匀,大者直径约1.5cm。
颅脑+上腹部CT:未见转移。
三、 临床诊断
胃镜病理示:
1. 诊断:食管CA伴不完全梗阻
2. 病理:食管恶性肿瘤(鳞状细胞癌)
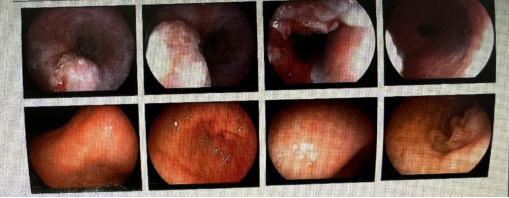
胃镜病理诊断图
影像学资料示:临床诊断为食管恶性肿瘤(cT3NxM0)
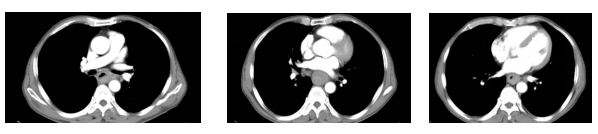
影像学诊断图
四、 治疗经过
新辅助化疗联合免疫治疗
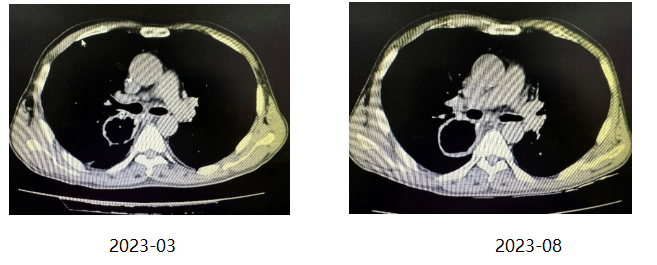
术前给予紫杉醇(白蛋白结合型)400mg+奈达铂100mg+斯鲁利单抗300mg的新辅助治疗方案。(下图为新辅助治疗前后对比)
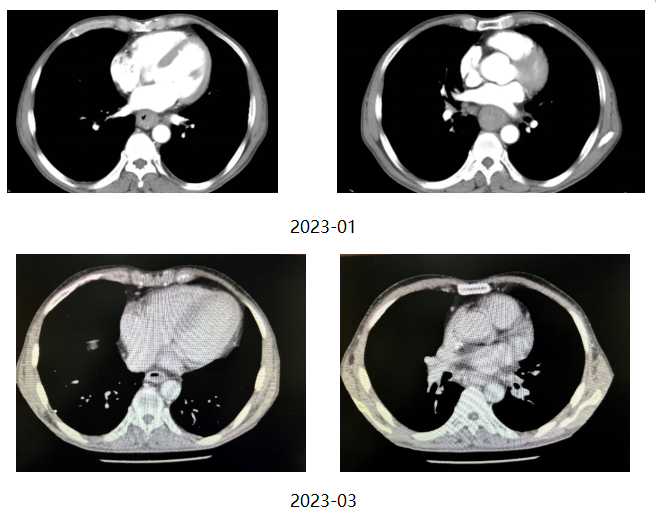
新辅助治疗后第三次入院讨论:食管胸中下段管壁增厚,局部呈软组织块影,较前缩小,患者手术意愿强烈。
术前准备:心脏彩超+左心功能测定:未见明显异常。
肺功能:轻度限制性通气功能障碍。
浅表彩超:双侧锁骨上淋巴结未见明显肿大。
手术治疗
2023.03.17行“颈胸腹三切口全食管切除术(食管癌根治术)+胸内食管-胃颈部吻合术+胸腔镜纵隔淋巴结清扫术+腹腔淋巴结清扫术”。
探查病变部位情况:经右第4、6、6、8四个肋间小切口约1cm进胸,二氧化碳气体人工气胸。胸腔镜探查见中下段食管见一肿物,大小约2.5*1.5*1.0cm,质稍硬,侵及全层,与食管中下段周围组织黏连紧密,食管旁、隆突下、左、右喉返神经旁,右锁骨上、下见多个淋巴结肿大,约黄豆至花生大,质硬。术中诊断:食管恶性肿瘤 。胸腔镜下于食管中段开始向上游离直至颈部食管处,向下游离至膈肌食管裂孔处,游离食管时清扫食管旁、隆突下、右喉返神经旁淋巴结。清扫淋巴结时同时探查双侧喉返神经。检查胸腔无明显出血后,于右胸腋中线第6肋间安置胸引流管一条。将病人改平卧位,头偏右侧,左肩部稍垫高,双下肢展开。取上腹部正中切口长约15cm,探查见膈面光整,肝胃胰脾、大小肠,大小网膜、盆腔无肿块,无腹水,贲门旁、胃左动脉旁等见多个淋巴结肿大,约黄豆至花生大,质硬。
探查进腹后分别游离、切断、结扎大网膜、胃短血管、膈胃韧带、胃网膜左血管等,保留胃网膜右血管弓。打开小网膜孔,游离、切断、结扎、缝扎胃左血管,保留胃右血管弓。腹腔淋巴结清扫。沿食管裂孔将切断的胃拖拉至腹腔,用6个EndoGIA制作管状胃并用丝线加固。颈部经左胸锁乳突肌前缘做长5cm斜切口,逐层切开,分离左颈前肌肉,分离显露颈部食管,部分组织与颈外静脉粘连紧密,普理灵缝合修补,用电刀离断食管,远端食管用长带子固定。将远端食管经食管床送入腹腔,剪断固定于食管断端的长条带,并固定于管状胃顶端,返管状胃于腹中。用长条带牵引,将管状胃经食管裂孔、食管床提至颈部与近端食管吻合,食管残端置入吻合器中心杠,经管状胃置入吻合器机身,行食管胃底器械吻合术,1号丝线间断缝合食管胃吻合口浆肌层4针,吻合满意,1个EndoGIA闭合并切除胃残端。1号丝线间断缝合浆肌层。留置胃管至胸腔胃,留置鼻肠管到空肠。查颈部及腹腔无活动性出血,用可吸收止血纱1962覆盖。颈部、纵隔留置引流管,逐层缝合颈部及腹部切口。
患者情况:手术顺利,麻醉平稳,术中出血约200ml,输液1500ml,未输血。
术后病理情况
1. 食管及肿物切除标本:送检食管及部分胃组织切除标本,大体见一蕈伞型肿物,大小2.5*1.3*1.0cm,镜下为中分化鳞状细胞癌,侵及肌层,间质纤维组织增生,伴多量淋巴细胞浸润,符合化疗后少部分退缩改变(TRG分级2级:<50%癌残留,Becker系统)。
(上切端)未见癌累及。
(下切端)未见癌累及。

食管及肿物切除标本
2. 各组淋巴结:中段食管旁LN(0/5)、下段食管旁LN(0/2)、胃左LN(0/12)、贲门旁LN(0/2)、左喉返神经起始部(0/12)、左喉返神经旁LN(0/12)、右喉返神经旁LN(0/4)、隆突下LN(0/4)、右锁骨上LN(0/2)、食管周围淋巴结(0/2)、胃周淋巴结(0/7)未见转移癌。
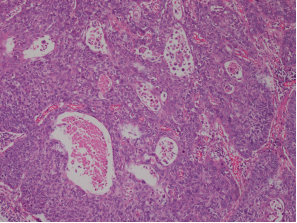
淋巴结示意图
3. 术后诊断:食管恶性肿瘤(中分化鳞状细胞癌,yPT2N0M0 ,I期)。
4. 术后维持治疗:新辅助化疗联合免疫治疗(紫杉醇400mg+奈达铂100mg+斯鲁利单抗300mg)
五、 病例小结
该病例为鳞状细胞癌cT3NxM0患者,接受新辅助化疗联合免疫治疗方案(紫杉醇、奈达铂、斯鲁利单抗)后食管肿块缩小,随后患者表达强烈手术意愿。手术为全食管切除术+胸内食管-胃颈部吻合术,手术顺利,术中出血约200ml,未输血。术后病理显示肿块为中分化鳞状细胞癌,化疗后部分退缩(TRG分级2级)。淋巴结未见癌转移。患者术后康复良好,无明显并发症。
讨论
既往研究表明,由于食管解剖位置特殊,多数食管癌患者确诊时病情已处于中晚期,且多数发生转移。因此,术前综合治疗对改善食管癌患者的预后至关重要,有学者提出,术前新辅助化疗可降低肿瘤活性,抑制肿瘤生长与转移,进而提高患者的术后生存率,改善预后ii。
免疫检查点抑制剂(ICIs)的诞生开启了食管癌治疗的新纪元。随着相关研究的增加,已发现通过在癌细胞表面过表达程序性死亡配体-1(PD-L1) 或通过诱导宿主免疫细胞上的PD-L1表达,肿瘤细胞利用程序性死亡受体-1(PD-1) /PD-L1 途径进行增殖。因此PD-1抑制剂通过靶向 PD-1 / PD-L1,使得 T 淋巴细胞恢复其功能,激活抗原杀灭肿瘤细胞。
免疫治疗联合新辅助化疗已被证实具有协同效应,根据ASTRUM-007研究,斯鲁利单抗联合化疗一线治疗在晚期食管癌患者中,可显著延长总生存期和无进展生存期,且安全性良好,是食管癌患者的安心之选。综合来看,本案例通过新辅助化疗联合免疫治疗+手术的方案取得了令人满意的疗效,为进一步的康复和生存提供了良好基础。
参考文献:
i 张云波,李敬,于会明,等. 食管癌新辅助放化疗与新辅助化疗对比Meta分析[J]. 中华转移性肿瘤杂志,2023,06(2):128-133.
ii 何金龙,王保收,朱岩. 新辅助化疗联合手术治疗食管癌的临床疗效及对患者预后的影响[J]. 癌症进展,2022,20(16):1687-1689.
iii 徐嫚嫚,孙晶晶,陆方晓. 局部晚期食管癌新辅助化疗联合免疫治疗后病理完全应答的影响因素分析[J]. 现代实用医学,2022,34(2):154-157.
iv 高鑫,李庆新,胡尕伟. 局部晚期食管癌新辅助治疗策略的研究进展 [J]. 现代肿瘤医学, 2023, 31 (21): 4083-4088.
v Song Y, Zhang B, Xin D, et al. First-line serplulimab or placebo plus chemotherapy in PD-L1-positive esophageal squamous cell carcinoma: a randomized, double-blind phase 3 trial. Nat Med. 2023;29(2):473-482.


