Gastroenterology:ALKBH5通过瞄准AXIN2来促进免疫抑制,以促进结直肠癌,是促进免疫治疗的目标
时间:2023-07-24 19:19:55 热度:37.1℃ 作者:网络
结直肠癌(CRC)是全球最常见的癌症之一,2018年新增180万例。由于肿瘤转移和复发,CRC的死亡率仍然很高。CRC的启动和进展涉及一系列遗传和表观遗传改变,也受到肿瘤免疫微环境(TIME)的影响。尽管CRC的化疗和免疫治疗取得了很大进展,但CRC患者的预后并不令人满意。免疫检查点封锁疗法(例如,抗PD1)只受益于微卫星不稳定性(MSI)高的免疫“热”CRC的一小部分。因此,需要阐明CRC内在事件和宿主免疫反应之间的串扰,以制定新的抗CRC免疫治疗策略。

N6-甲基腺苷(m6A)RNA修饰是肿瘤生物学中的表转录组调节机制。它是信使RNA(mRNA)中最丰富的修饰,并调节mRNA剪接、降解和翻译。m6A修饰由m6A写手(METTL3/METTL14/WTAP)和橡皮擦(ALKBH5/FTO)动态调节,分别诱导m6A甲基化和脱甲基化。m6A阅读器,如YTHDF1/2/3,YTHDC1/2和IGF2BP1/2/3,可以直接与m6A修饰的mRNA结合,导致mRNA剪接、出口、稳定性和翻译的变化。最近的研究暗示了m6A写手的关键作用。然而,RNA m6A修饰在调节时间中的作用在很大程度上仍未被探索。
肿瘤免疫微环境是肿瘤细胞和肿瘤浸润免疫细胞之间相互作用的关键。它与肿瘤的启动、进展和免疫治疗的反应密切相关。在肿瘤免疫微环境中,CD8+ T细胞和自然杀伤者(NK)细胞是促进抗肿瘤免疫的主要细胞群。髓源性抑制细胞(MDSC)强烈抑制T和NK细胞的功能,以损害抗肿瘤免疫,并使CRC患者对免疫检查点抑制产生抗药性。
2023年5月9日发表在Gastroenterology上的文章,研究人员确定了原发性CRC中ALKBH5的高表达,这与CRC患者的生存率低有关。然后,在一系列体外和体内实验中阐明了ALKBH5对肿瘤免疫微环境的功能重要性。除此之外,研究人员发现CRC细胞中ALKBH5的过度表达使用共生肿瘤和肠道特异性Alkbh5 knockin小鼠显著重塑了肿瘤免疫微环境中免疫细胞的组成。特别是,在CD34+人性化小鼠中进一步证实了ALKBH5促进免疫抑制的作用,推断其在人类CRC中的影响。
通过综合甲基化RNA免疫沉淀测序(MeRIP-seq)和RNA测序(RNA-seq)分析,探索了ALKBH5的直接下游靶和信号通路。最后,研究人员使用基于囊泡状聚(乳酸共糖酸)的纳米颗粒(VNPs)系统将靶向ALKBH5的小干扰(si)RNA输送到体内的CRC细胞中,以评估ALKBH5抑制与CRC抗PD1治疗相结合的治疗效果。

本文总结图
研究人员在人类样本中评估了ALKBH5的临床意义(n=205)。在同种异体移植、CD34+人性化小鼠和Alkbh5敲击小鼠中研究了ALKBH5的功能。通过流式细胞仪、免疫荧光和功能调查来确定免疫变化。使用甲基化RNA免疫沉淀测序和RNA测序来识别ALKBH5靶点。构建了囊泡样纳米颗粒封装的ALKBH5-小干扰RNA,用于在体内靶向ALKBH5。
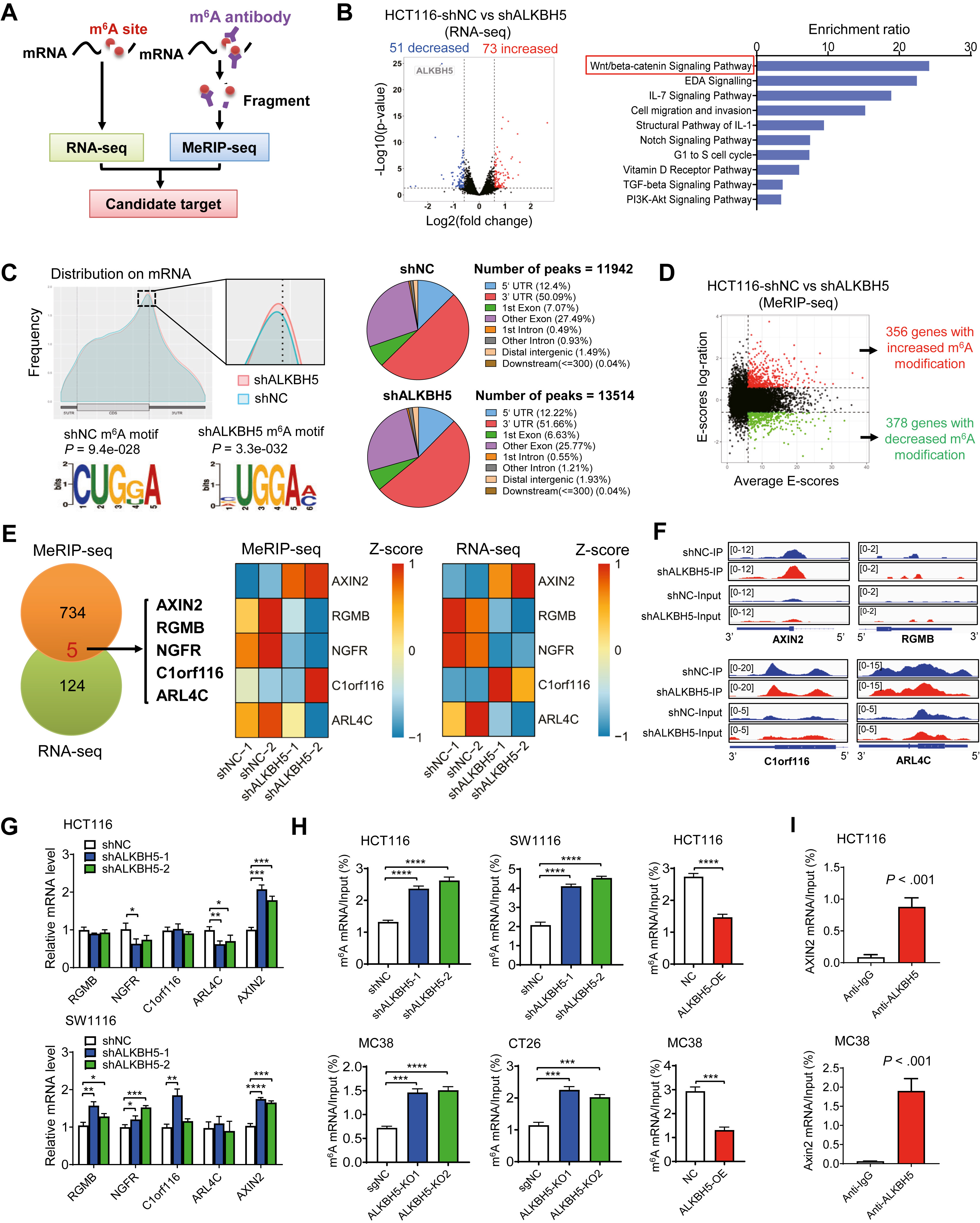
AXIN2被确定为ALKBH5的候选目标
实验结果表明,高ALKBH5表达预测CRC预后不良。ALKBH5诱导骨髓源性抑制细胞积累,但减少了自然杀伤细胞和细胞毒性CD8+ T细胞,以诱导同种异体移植、CD34+人性化小鼠和肠道特异性Alkbh5 knockin小鼠的结直肠肿瘤发生。从机械上讲,Wnt抑制器AXIN2被确定为ALKBH5的目标。ALKBH5结合和脱甲基AXIN2信使RNA,导致其与N6-甲基腺苷读取器IGF2BP1分离并降解,导致Wnt/β-catenin超活化。
随后,ALKBH5诱导了Wnt/β-catenin靶点,包括Dickkopf相关蛋白1(DKK1)。ALKBH5诱导的DKK1招募了骨髓源性抑制细胞来驱动CRC中的免疫抑制,这种效果被体外和体内的抗DKK1所消除。最后,囊泡状纳米颗粒封装ALKBH5小干扰RNA,或抗DKK1增强抗PD1治疗,通过增强抗肿瘤免疫力来抑制CRC生长。
这项研究存在几个局限性。首先,在肠道特异性Alkbh5敲击小鼠中进行了azoxymethane/DSS模型,但在ApcMin/+模型中没有。还将对生理相关模型进行进一步研究,如肠道特异性Alkbh5敲除小鼠。其次,研究重点是T细胞、NK细胞和MDSC,以及参与CRC的其他免疫细胞群体的作用,包括T辅助17细胞和调节性T细胞,没有被评估。
最后,抗Gr1可能针对其他髓样衍生细胞,如中性粒细胞以及MDSCs。通过对CRC患者独立队列的分析证实了我们的实验发现,在mRNA和蛋白质水平上,ALKBH5是CRC患者生存率低下的独立预测因素。此外,ALKBH5与AXIN2呈负相关,而与DKK1呈正相关,这意味着ALKBH5-m6A-AXIN2-DKK1轴在人类中也有活动。
综上所述,本文发现了ALKBH5在塑造CRC免疫抑制景观中的作用。ALKBH5通过m6A-AXIN2-Wnt-DKK1轴促进CRC,以招募免疫抑制MDSC,这限制了NK和CD8+T细胞的抗肿瘤活性。ALKBH5可以作为CRC患者有前途的预后因素和治疗目标。
原文出处
Zhai, J.; Chen, H.; Wong, C. C.; Peng, Y.; Gou, H.; Zhang, J.; Pan, Y.; Chen, D.; Lin, Y.; Wang, S.; Kang, W.; To, K. F.; Chen, Z.; Nie, Y.; He, H. H.; Sung, J. J.-Y.; Yu, J., ALKBH5 Drives Immune Suppression Via Targeting AXIN2 to Promote Colorectal Cancer and Is a Target for Boosting Immunotherapy. Gastroenterology 2023, 165 (2), 445-462.


