论文解读|重庆医科大学李秋教授团队:儿童激素敏感型肾病激素应答亚型全基因组关联分析多中心队列研究
时间:2024-05-30 13:01:06 热度:37.1℃ 作者:网络
原发性肾病综合征(PNS)是儿童常见的原发性肾小球疾病之一,口服糖皮质激素是PNS公认的一线治疗方法。根据糖皮质激素的治疗差异,儿童PNS分为两种类型:占80%左右的激素敏感型肾病综合征(SSNS)和20%激素耐药型肾病综合征(SRNS),其中50-60%的SSNS在感染、炎症及免疫微环境变化等情况下,会出现激素依赖及频复发肾病状态(SDNS/FRNS),造成治疗困难,甚至发生迟发性激素耐药,部分患者最终进展至终末期肾病。虽然现有研究多数认为复杂免疫分子网络协同参与SSNS的发生、发展,但因缺乏大规模SSNS患者遗传层面研究,因此SSNS的疾病机制仍不清楚,同时对SSNS疾病诊治的研究是国内外肾脏病学家关注的热点。
因既往缺乏大量临床资料及全基因组遗传数据,全球范围内针对SSNS不同激素应答亚型这一重要科学问题处于研究真空地带。由国家儿童健康与疾病临床医学研究中心(重庆医科大学附属儿童医院)肾脏病诊治中心李秋教授牵头,联合深圳市儿童医院、成都妇女儿童中心医院、昆明市儿童医院、华中科技大学武汉儿童医院等5家中心单位开展了一系列国内外、原创性的针对儿童SSNS的队列研究。其中,由重庆医科大学附属儿童医院陈汉主治医师、深圳市儿童医院倪芬芬主治医师、昆明市儿童医院赵波教授作为共同第一作者,重庆医科大学附属儿童医院阳海平副教授、李秋教授作为共同通讯作者在本刊发表题为“A genomic association study revealing subphenotypes of childhood steroid-sensitive nephrotic syndrome in a larger genomic sequencing cohort”的文章,通过该研究更新了国内外关于SSNS疾病机制的认知,即通过我国大规模独立SSNS患者群体,证实HLA基因群在SSNS不同激素应答亚型的产生发挥了重要效应,这种效应是导致SDNS/FRNS发生、发展的关键因素。此外,研究也发现了若干激素敏感无复发型肾病(SSNSWR)、SDNS/FRNS相关的风险基因/位点及其临床意义。
研究成果展示:(具体临床队列实施方案、生信分析流程参见原文)
1. 基于多中心队列研究(360名SSNS儿童和1835名对照)结合GWAS策略(significance threshold P<5.0×10-8)证实HLA-DQA1中的rs1047989是激素依赖频复发(SDNS/FRNS)的风险位点,而其余类型的SSNS患者不具备HLA依赖性(图1)。SSNSWR患者的风险位点包括:rs117962550(OR=4.13, 95%CI 2.63-6.49, P=7.17×10-10),2:97909692(OR=2.62, 95% CI 1.86-3.68, P=3.37×10-8);SDNS/FRNS患者的风险位点包括:rs1047989(OR=0.389, 95%CI 0.299-0.566, P=2.08×10-12),2:171713702(OR=5.70, 95% CI 3.13-10.40, P=1.37×10-8),以上研究结果均需要通过Scalable and Accurate Implementation of GEneralized mixed model广义混合模型(SAIGE)独立验证。
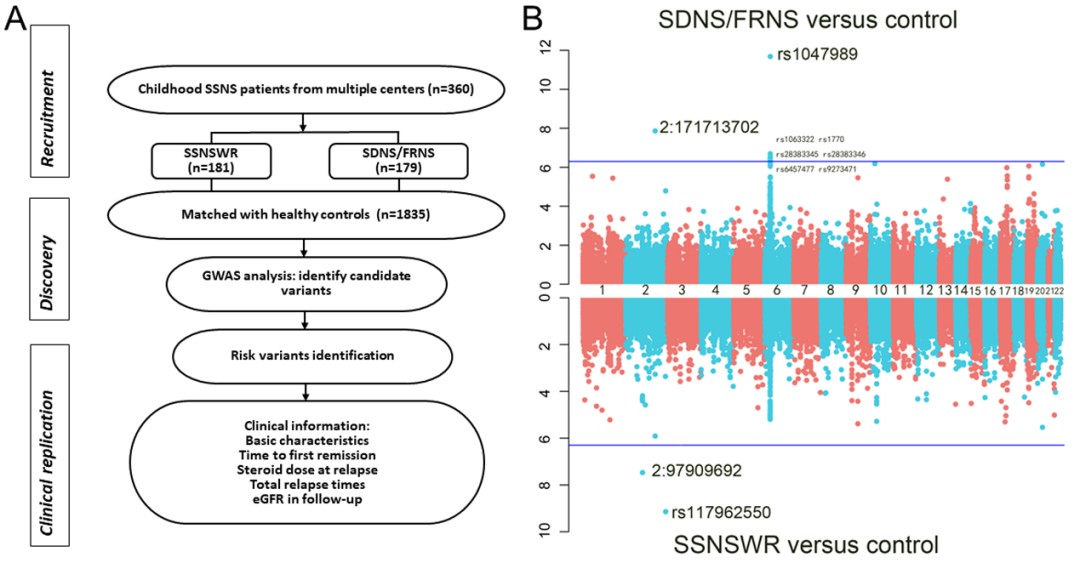
图1 队列研究流程图及曼哈顿图
2. Gene-Based Association (GBA)分析提示:与健康对照组相比较,SSNSWR和SDNS/FRNS患者的罕见突变位点(MAF<1%)均在CPNE4基因富集 (P=1.28×10-30, SSNSWR vs. control; P=1.32×10-10, SDNS/FRNS vs. control)。以上分析采用基因负荷检验SKAT-O检验模型验证。
3.表达数量性状基因座(eQTL)分析揭示:通过NephQTL browser过滤, rs1047989与HLA-DQB1, HLA-DRB5, HLA-DRB1, HLA-DQB2, HLA-DQA2, PSMB9, HCG23, PSMB8-AS1,HLA-DPB2存在顺式eQTL效应(图2),其余显著性SNP未获得在肾脏组织中有eQTL效应数据支撑。
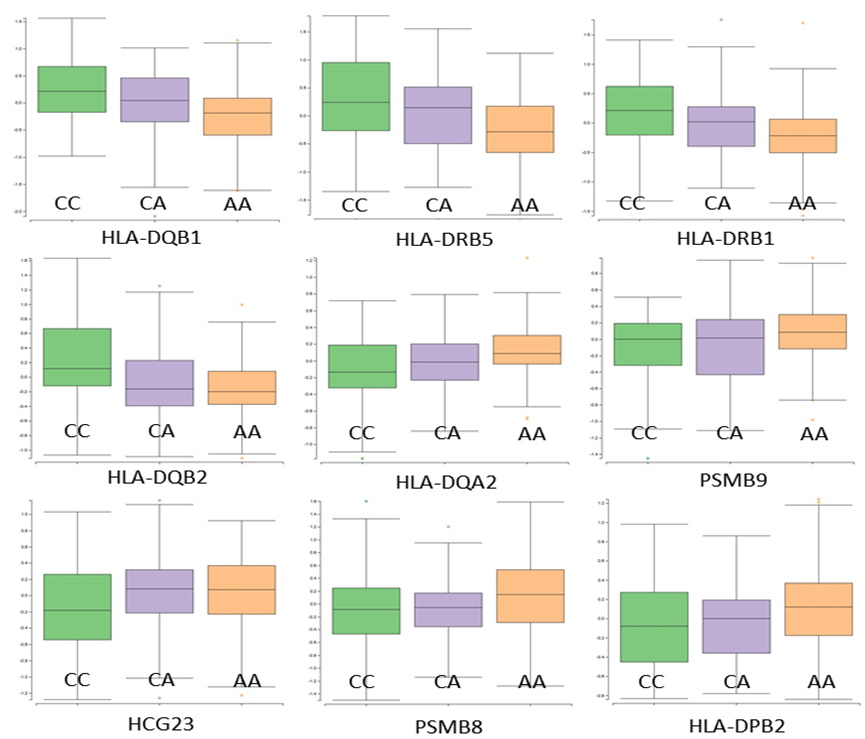
图2 rs1047989的秩标准化、调整后的肾小球表达
4. 通过遗传模型(隐性、显性和加性模型)分析所有观察到的显著SNPs(significance threshold P<5.0×10-5)。加法模型为rs117962550提供了最佳拟合。优势模型为rs746236012、2:97909692、2:171713702、rs1047989、rs139880713、rs774409792和rs117014418提供了最佳拟合。这些结果表明,杂合和纯合状态患者的临床风险显著增加。
5. SSNS患者临床性状特征分析:1)初次糖皮质激素应答时间(d)与显著性SNP位点无相关性;2)疾病复发时激素平均剂量(mg/kg/d):2:171713702与SDNS/FRNS患者复发至首次缓解时更大的类固醇剂量(>0.75 mg/kg/d)重要相关(OR=3.14;95%CI,0.97-9.87;P=0.034);3)疾病复发总次数(n):rs117014418(APOL4)和rs139880713(FRG1JP)SDNS/FRNS患者复发风险有显著关联(rs117014418, n>3, OR=0.40, 95% CI, 0.16-1.01, P=0.043; rs139880713, n>3, OR=0.29, 95% CI, 0.09-0.92, P=0.025)。有趣的是,2:171713702(GAD1)与SDNS/FRNS患者低复发风险有关(n=2, OR=4.98; 95% CI, 1.12-46.13; P=0.022),导致这种现象的原因,推测携带2:171713702患者更易受到医生的关注,并接受更积极的治疗,如免疫抑制剂治疗或加强感染预防。
6. 临床预后问题:由于SDNS/FRNS的复杂性和不良预后,本研究在随访中评估显著的SNPs与肾小球滤过率(eGFR)之间关联。结果提示在随访期间,总体SSNSWR或SDNS/FRNS组均未观察到eGFR显著下降,但携带rs117014418(APOL4)的SDNS/FRNS患者eGFR在随访期间内存在20%的基线值显著降低(隐性模型P=0.0001;显性模型P=0.00038),蛋白三维结构预测提示突变蛋白第259个氨基酸是胱氨酸,其与第256个苏氨酸和第258个甘氨酸没有氢键相互作用,导致APOL4的二级结构受到干扰(图3)。
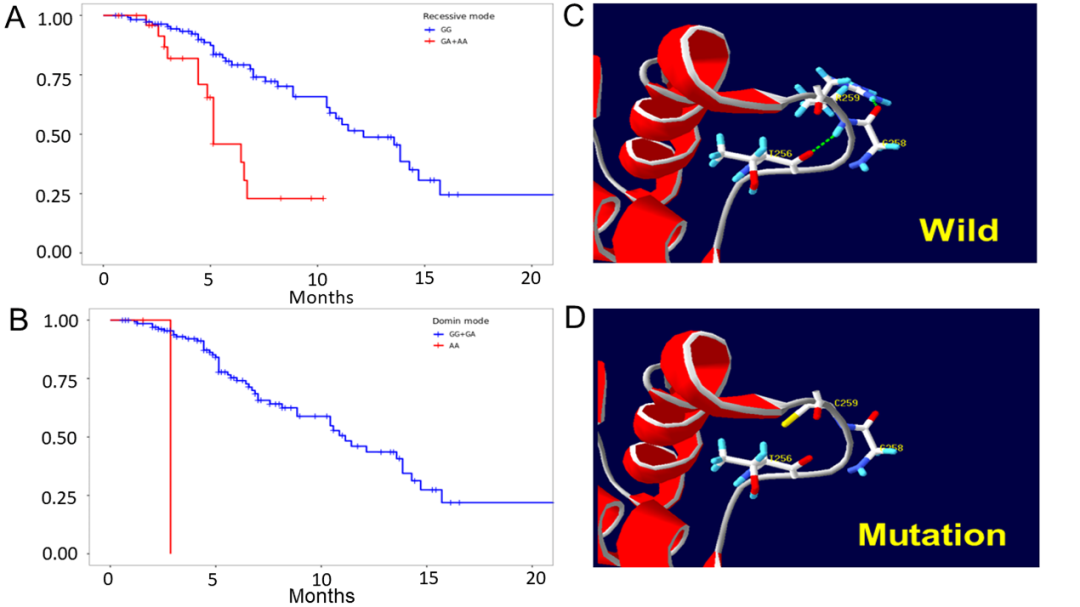
图3 rs117014418在APOL4中的结构和功能变化。(A)rs117014418的Kaplan-Meier生存分析(上图隐性;下图显性模型)。(B)rs117014418的计算机预测模型中(上图野生型;下图突变型)
本研究创新总结:
1. 首次建立大规模、多中心儿童激素敏感型肾病综合征不同激素应答亚型(SSNSWR和SDNS/FRNS患者例数)临床队列。
2. 本研究更新了现有国内外关于SSNS疾病机制的认知,通过分层次纳入SSNS不同激素应答亚型患者的方案,证实HLA基因群在SSNS不同激素应答亚型的产生发挥了重要效应,而这种效应是导致SDNS/FRNS发生、发展的关键。
作者介绍
李秋,国家二级教授,博士生导师,享受国务院特殊津贴,全国人大代表,国家卫健委中青年突出贡献专家,中华医学会儿科分会常委、秘书长,中华医学会儿科分会肾脏学组副组长,主要研究方向:儿童肾小球疾病遗传机制、免疫发病机制。获教育部科技进步二等奖、重庆市科技进步一等奖、重庆市教学成果一等奖。先后主持及指导自科及国家级科技攻关项目10多项、省部级项目20多项、发表论文160余篇。
文章来源
免费全文下载链接:
https://www.sciencedirect.com/science/article/pii/S2352304223004099
引用这篇文章:
Chan H, Ni F, Zhao B, et al. A genomic association study revealing subphenotypes of childhood steroid-sensitive nephrotic syndrome in a larger genomic sequencing cohort. Genes Dis. 2024; 11(4):101126


