Nat Commun:郑州大学夏总平团队发现线性多泛素化控制疱疹病毒裂解性再激活和感染的作用机制
时间:2024-07-07 23:04:49 热度:37.1℃ 作者:网络
与许多其他病毒一样,卡波西肉瘤相关疱疹病毒(KSHV)有两种生命周期模式:潜伏期和裂解期。来自KSHV的RTA蛋白对于裂解性再激活至关重要,但尚不完全清楚其调控机制。
2024年6月29日,郑州大学夏总平团队在Nature Communications 在线发表题为“Linear ubiquitination regulates the KSHV replication and transcription activator protein to control infection”的研究论文,该研究报道在KSHV裂解性再激活和感染过程中,线性泛素化调节RTA的活性。过度表达OTULIN抑制KSHV裂解性再激活,而敲除OTULIN或过度表达HOIP则强化该过程的发生。
有趣的是,该研究发现RTA在K516和K518位点被HOIP线性多泛素化,这些修饰过程控制RTA的核定位。OTULIN从细胞质RTA中去除线性多泛素链,阻止其核输入。EB和MHV68病毒编码的RTA直系同源物通过发生线性多泛素化并受OTULIN调控。结果显示,线性多泛素化在疱疹病毒感染中起着关键作用,表明该病毒同样具备由已知线性多泛素化控制的生物过程。

卡波西肉瘤相关疱疹病毒(KSHV)或人类疱疹病毒8(HHV8)是γ疱疹病毒亚家族的成员,与三种类型的恶性肿瘤有关:卡波西肉瘤(KS)、原发性积液淋巴瘤(PEL)和多中心Castleman病(MCD。与其他疱疹病毒类似,KSHV具有两个阶段的生命周期模式:潜伏期和裂解期。KSHV主要维持在潜伏期,其特征在于特定的基因表达谱。然而,KSHV可以在暴露于缺氧等压力源或12-O-十四烷酰佛波醇-13-乙酸酯(TPA)、丁酸钠(NaB)和丙戊酸钠(VPA)等化学试剂下被裂解重激活,其特征是裂解基因的顺序表达,包括即刻早期(IE)、早期(E)和晚期(L)基因。KSHV裂解再激活对于病毒传播和KSHV诱导的肿瘤发生都至关重要,为KSHV相关恶性肿瘤提供了治疗机会。
潜伏期引起的KSHV裂解再激活由其ORF50(复制和转录激活因子(RTA)编码的蛋白质控制。研究表明,RTA表达启动KSHV,使其从潜伏期过渡到裂解期。RTA在γ-疱疹病毒家族(如EB病毒(EBV)和鼠疱疹病毒68(MHV68))中高度保守。RTA在其N末端(NLS1,aa6-12)和C末端(NLS2,aa514-528)具有富含精氨酸和赖氨酸的NLS(细胞核定位信号)基序,NLS2对其核定位至关重要。RTA是一种IE基因,作为转录因子与RTA反应元件(RRE)相互作用,促进裂解基因的序贯表达,从而产生活病毒颗粒。RTA可以驱动多种病毒基因的表达,包括PANRNA、Ori-Lyt相关RNA、ORF57、K8和RTA自身,RTA还促进泛素-蛋白酶体介导的RTA阻遏蛋白的降解。
RTA还作为泛素E3连接酶发挥作用,靶向MyD88和IRF7的泛素化和随后的降解,从而使KSHV能够逃避宿主细胞的免疫攻击。有趣的是,这种E3连接酶活性可以催化RTA自泛素化,从而将RTA水平维持在相对较低的水平,以限制不必要的病毒再激活。值得注意的是,RTA的转录功能受多种翻译后修饰(PTM)的负调控,包括PARP-1介导的聚(ADP-核糖基化)、激酶hKFC介导的磷酸化和O-GlcNAc转移酶(OGT)在其富含Ser/Thr的基序处促进O-GLC酰基化。尽管在RTA活性的调节方面取得了一定进展,但尚未完全了解其活性调控机制。
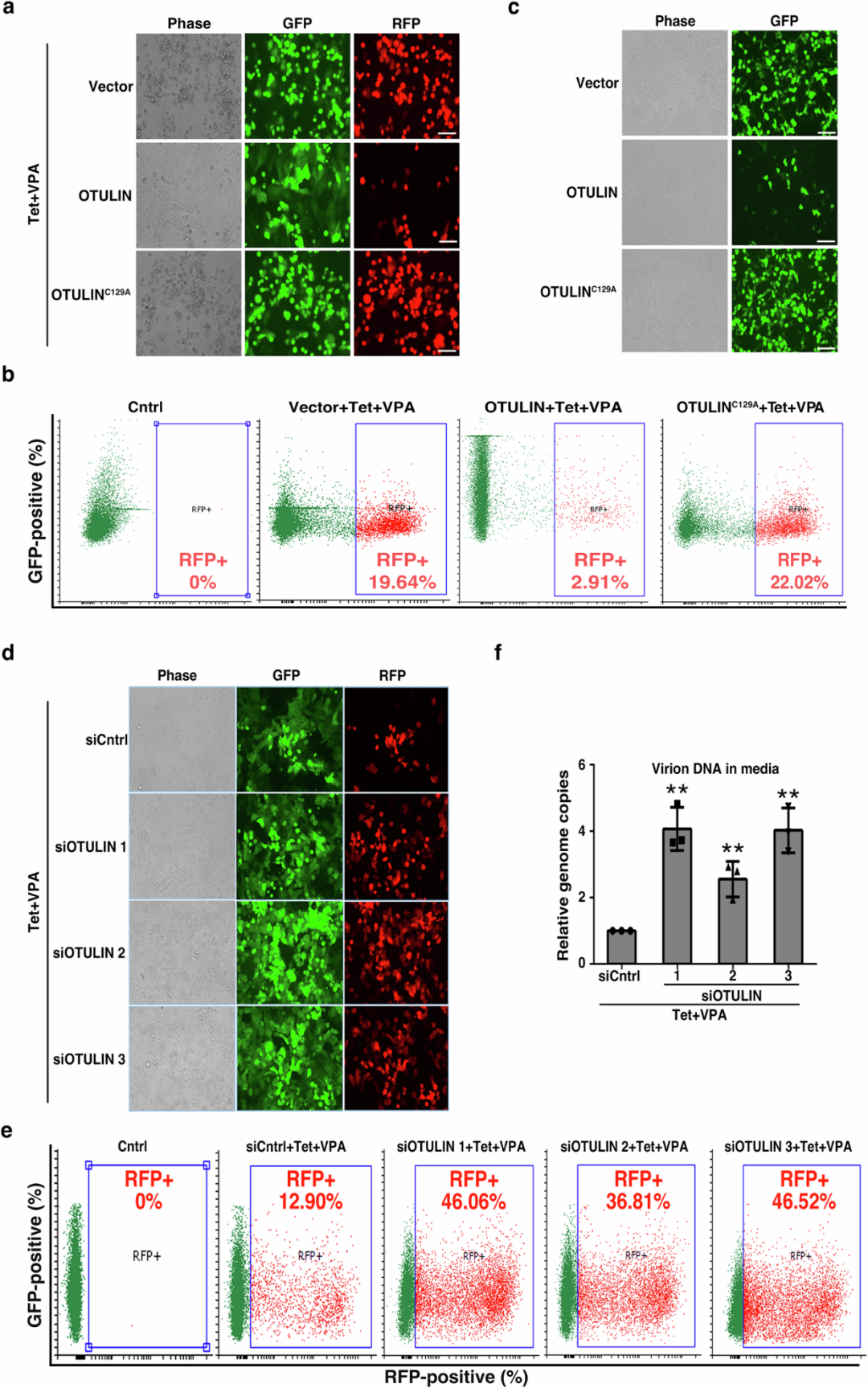
线性去泛素化酶OTULIN抑制KSHV裂解再激活(摘自Nature Communications )
蛋白质泛素化是许多细胞过程(包括蛋白质降解、DNA损伤反应、蛋白质运输和细胞内信号传导)所必需的PTM,涉及不同类型的泛素链与靶蛋白上的赖氨酸残基的偶联。已知的泛素链由七条经典赖氨酸连接的聚合物链和最近发现的线性Met1连接的多泛素(M1polyUb)链组成。M1泛素化已被证明在免疫和炎症信号传导过程中的信号激活通路(如NF-κΒ和RIG-I)中尤为重要,调节细胞死亡、T细胞和B细胞发育、小鼠胚胎发育、癌症和自身免疫性疾病。当一种泛素的氨基末端与另一种泛素的羧基末端偶联时,就会形成M1polyUb链。
E3连接酶“线性Ub链组装复合物(LUBAC)”是目前唯一发现的能够产生M1polyUb链的连接酶。LUBAC由HOIP、HOIL-1L和Sharpin三个亚基组成,其中HOIP负责调控连接酶活性。此外,细胞编码去泛素化(DUB)酶OTULIN(具有线性连锁特异性的卵巢肿瘤去泛素化酶,也称为FAM105B或Gumby),该酶能够特异性拮抗M1polyUb链。LUBAC和OTULIN的相反活性共同决定了细胞中M1polyUb链的总丰度。研究表明,M1polyUb链参与了多个生物过程。值得注意的是,M1polyUb链已被报道用于调节HTLV Tax的功能。
该研究探索了泛素化在控制KSHV裂解再激活中的作用机制。研究发现M1泛素化在KSHV感染期间调节RTA。具体而言,在iSLK/rKSHV.219细胞中,OTULIN的过表达抑制KSHV裂解性再激活,而OTULIN敲低和HOIP的过表达均能够增强该过程。RTA在K516和K518位点被HOIPM1多泛素化,这些修饰控制了RTA在细胞核中的定位。作者发现OTULIN可以从RTA中去除M1多泛素链,从而使RTA从细胞核转移到细胞质。研究还揭示了由EBV和MHV68病毒编码的RTA直系同源物也是M1多泛素化的,并受OTULIN调节。除阐明M1多泛素化在调节病毒感染中的生物学功能,该研究还为治疗KSHV感染和KSHV相关恶性肿瘤提供了潜在靶点。
参考消息:
https://www.nature.com/articles/s41467-024-49887-6


