干货:紫杉类抗肿瘤药物在肿瘤科的应用全解析,建议收藏!
时间:2024-07-30 14:00:42 热度:37.1℃ 作者:网络
紫杉类抗肿瘤药物作为化疗领域的明星药物,以其显著的生物学活性、独特的抗肿瘤机制广泛应用于肺癌、乳腺癌、卵巢癌和头颈癌等多种实体瘤的治疗。
目前上市的紫杉类抗肿瘤药物包括经典的紫杉醇和改良后的多西他赛、紫杉醇脂质体、紫杉醇(白蛋白结合型)以及新兴的紫杉醇聚合物胶束。
本文总结了紫杉类抗肿瘤药物的用法(禁忌症、适应症、预处理、配置要求、输注要求、给药顺序)、注意事项(特殊人群用药建议、与西药及中药相互作用)、不良反应等[2],旨在和大家一同学习进步。
一、药物简介
1、紫杉醇
紫杉醇是从红豆杉树皮中提取的天然新型抗肿瘤药物,它通过促进微管蛋白聚合并抑制解聚,使细胞周期停滞于G2/M期,阻碍肿瘤细胞复制使癌细胞无法继续分裂而死亡。紫杉醇难溶于水,需采用聚氧乙烯蓖麻油和无水乙醇助溶,聚氧乙烯蓖麻油在体内降解时释放组胺,可导致严重的过敏反应[3]。
2、多西他赛
紫杉醇天然提取含量非常低,多西他赛是在紫杉醇的基础结构上进行改造合成的第二代紫杉类抗肿瘤药物,作用机制和紫杉醇相同,与微管蛋白的亲和力更强,抗肿瘤活性更高[4]。
3、紫杉醇脂质体
脂质体是由磷脂、胆固醇等材料构成的类似于细胞膜的磷脂双分子层结构, 紫杉醇包被在其中能够提高水溶性而无需添加聚氧乙烯蓖麻油。紫杉醇脂质体疗效与紫杉醇相当, 但不良反应有所降低[5]。
4、紫杉醇(白蛋白结合型)
紫杉醇(白蛋白结合型)是将人血白蛋白与紫杉醇通过高压振动技术制成的纳米微粒冻干粉针,以白蛋白作为载体,能够利用细胞膜上的白蛋白受体Gp60、细胞膜穴样内凹以及富含半胱氨酸酸性分泌性蛋白,促进药物进入肿瘤细胞, 提高靶向作用。与传统注射剂或多西紫杉醇相比,紫杉醇(白蛋白结合型)不仅提高了耐受剂量、去除了过敏反应, 同时还使治疗效果得到明显改善, 是国际公认的紫杉醇最先进的制剂[5]。
5、紫杉醇聚合物胶束
紫杉醇聚合物胶束为聚乙丙交酯包裹紫杉醇形成的胶束,不含有聚氧乙烯蓖麻油。聚乙二醇作为聚合物胶束的外壳,,能够避免网状内皮系统的吞噬, 延长体内循环时间[5]。
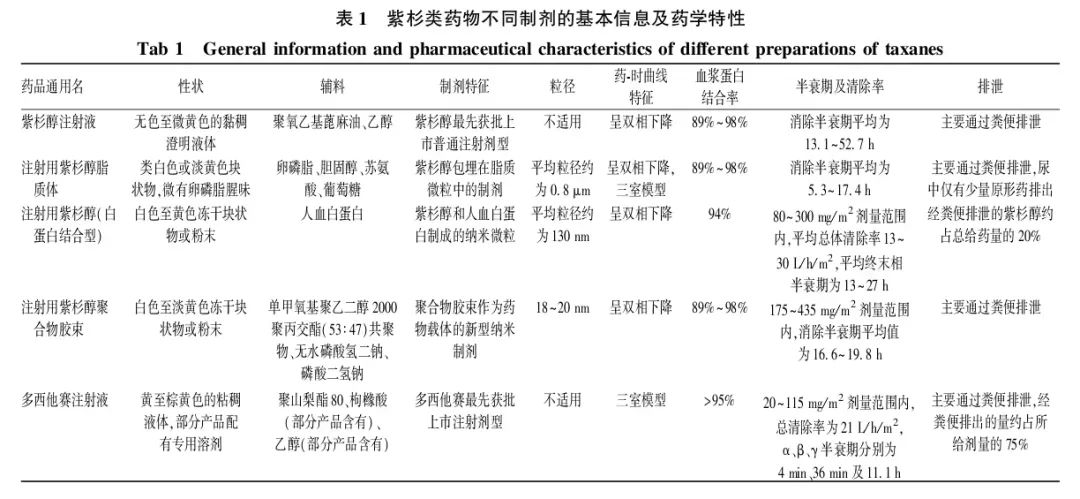
表1 紫杉类药物不同制剂的基本信息及药学特性
二、药物用法
1、禁忌症

表2 紫杉类抗肿瘤药物的禁忌症
2、适应症

表3 紫杉类抗肿瘤药物的适应症及用法用量
3、预处理

表4 紫杉类抗肿瘤药物预处理
4、配置要求

表5 紫杉类抗肿瘤药物配置要求
5、输注要求

表6 紫杉类抗肿瘤药物的输注要求
6、给药顺序
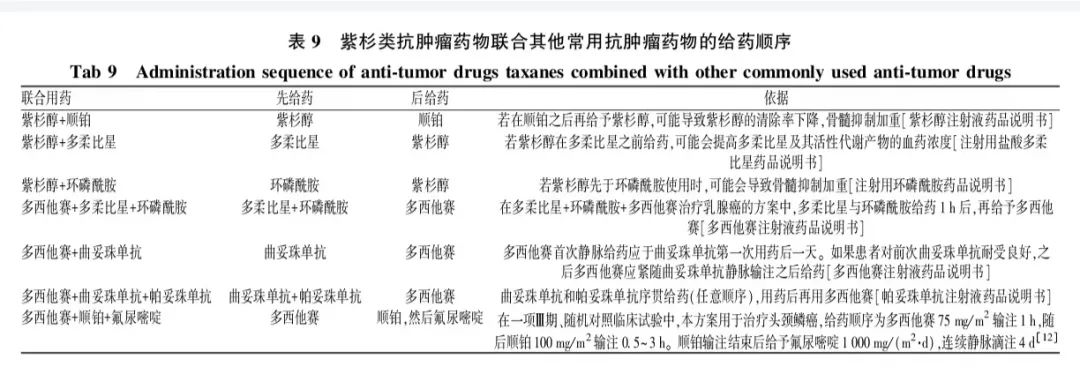
表7 紫杉类抗肿瘤药物联合其他抗肿瘤药物的给药顺序
三、注意事项
1、特殊人群紫杉类抗肿瘤药物用药建议

表8 特殊人群紫杉类抗肿瘤药物的用药建议
2、药物相互作用
2.1紫杉类抗肿瘤药物与西药的相互作用

表 9 紫杉醇抗肿瘤药物与西药的相互作用
2.2紫杉类抗肿瘤药物与中药的相互作用
临床使用紫杉醇135~175 mg/m2静脉化疗期间给予复方苦参注射液治疗,部分患者出现骨髓抑制加重、Ⅱ度甚至Ⅲ度神经毒性发生率增加[2]。
2.3预处理方案中所含药物与其他药物的相互作用

表10 预处理方案中所含药物与其他药物的相关作用
四、不良反应
紫杉类抗肿瘤药物有效成分相似,不良反应大致相同,主要表现为过敏反应、血液毒性、神经毒性、肌肉关节痛、心血管毒性、肝肾毒性和消化道反应等,需要对其进行监测,。
1、过敏反应
1.1过敏反应的机制及临床表现
接受紫杉醇治疗的患者易出现Ⅰ型超敏反应,发生率高达30%~41%,其中严重超敏反应的发生率为2%~5%,多在用药后2~3min,几乎全部发生在输注的最初10min,大多数发生在第1次或第2次输注后。
一般表现为皮疹、皮肤潮红、荨麻疹等,严重时可表现为胸闷、呼吸困难、低血压、心动过速等。此外,也可能有血管肿痛、胸部和四肢疼痛等其他症状。多西他赛过敏反应发生率低于紫杉醇注射液。紫杉醇脂质体、注射用紫杉醇(白蛋白结合型)因剂型改进发生过敏反应相对较少。
1.2过敏反应的处理
首先询问并评估患者过敏史,向患者说明紫杉类药物输注后可能出现的过敏反应及对策,配合医护人员进行预处理和药品输注。预处理不能完全消除过敏反应,药物输注期间仍需密切观察。
若用药后出现过敏反应,需对其进行级别的评估和分层处理:若出现潮红、皮疹等轻微症状,可以不停止治疗,仅需对症处理;若出现呼吸困难、低血压、血管神经性水肿和全身荨麻疹为特征的严重过敏性反应,需要立即停止输注,并积极地进行对症治疗。
轻中度过敏反应患者情况稳定后,可尝试再次缓慢输注药物,若再次发生过敏反应,建议使用同类别的其他药物或不同类别的药物替代;重度过敏患者则不再建议使用原药物,生命体征平稳24h后,可在严密监护下使用同类别的其他药物或不同类别的药物。其中紫杉醇或多西他赛可考虑使用紫杉醇(白蛋白结合型)替代。
2、血液学毒性
血液学毒性是紫杉类药物主要的剂量限制性毒性,包括中性粒细胞减少、贫血、血小板减少,其发生风险与药物种类、剂量和输注时间相关。
中性粒细胞减少症指外周血中性粒细胞绝对计数(ANC)<2.0×109 /L,中性粒细胞减少性发热是最主要的临床并发症。多西他赛的血液毒性发生风险和严重程度相对较高。紫杉醇(白蛋白结合型)与普通紫杉醇的血液毒性发生情况相似,等剂量的紫杉醇(白蛋白结合型)相较于普通紫杉醇,4级中性粒细胞减少症的不良反应发生率较低。
贫血常见主诉有晕厥、活动后呼吸困难、头痛、眩晕、胸痛、工作和日常活动乏力,明显的皮肤、黏膜苍白,以及女性患者月经异常,还可能有黄疸的症状表现。肿瘤相关性贫血的发生率和严重程度可能会随着化疗周期增多而升高和加重。紫杉类药物治疗期间肿瘤相关性贫血事件较为常见,但多数为1/2级。
肿瘤化疗相关性血小板减少症是指抗肿瘤化疗药物对骨髓巨核细胞产生抑制作用,导致外周血中血小板计数低100×109 /L。紫杉类药物单药引起的血小板减少较为常见,但3/4级较为少见。
3、神经毒性
神经毒性是紫杉类药物的常见不良反应,发生率高达70%~80%,临床表现为手和/或脚的感觉异常、麻木或神经性疼痛,呈累积及剂量依赖性特点,通常随着剂量的增加和治疗时间的延长而加重。与紫杉醇相比,多西他赛所致周围神经病变(CIPN)临床发生率较低,症状较轻。有meta分析显示紫杉醇脂质体治疗乳腺癌较紫杉醇神经系统毒性发生率低。紫杉醇(白蛋白结合型)的CIPN发生率略高于紫杉醇。周围神经毒性的预防可使用冷冻疗法(冰手套或袜子等)或加压手套等方式,治疗可采用度洛西汀等抗抑郁药。
4、肌肉关节痛
紫杉烷急性疼痛综合征(TAPS)临床较为常见,其特征是在紫杉类药物化疗后1~3d发生并持续 5~7d的关节痛和肌痛。TAPS发生率在2.8%~72%,多西他赛的TAPS比紫杉醇或紫杉醇(白蛋白结合型)更为常见,且TAPS在乳腺癌患者中可能比非乳腺癌患者更常见。阿片类药物、对乙酰氨基酚和非甾体抗炎药可用于治疗TAPS,但效果并不显著。
5、肝肾毒性
紫杉类药物大部分通过肝脏代谢和胆汁排泄进行清除,可见肝功能指标如胆红素和氨基转移酶的升高,但肝损伤较少发生。紫杉类药物肾脏代谢占比较少,对于轻中度肾功能异常无需调整紫杉醇(白蛋白结合型)和紫杉醇聚合物胶束的初始剂量。
6、消化道反应
紫杉类药物为低度致吐风险,呕吐发生率为10%~30%,但是联合用药时,致吐风险等级由组合中风险最高的药物决定。
7、其他不良反应
其他不良反应包括乏力、头痛、脱发等,一般无明确处置推荐。紫杉类药物静脉给药还可引起注射部位反应,包括静脉和局部炎症、药物渗出等。
参考文献
[1] 紫杉醇类抗肿瘤药物药品说明书.
[2] 国家癌症中心,中国药师协会肿瘤专科药师分会.紫杉类抗肿瘤药物药学服务中国专家共识[J].中国医院用药评价与分析,2022,22(12):1409-1427.
[3] 陈坤成,冯思良,刘克良.紫杉烷类抗肿瘤药物临床研究进展[J].国际药学研究杂志,2013,40(3):271-276.
[4] 李苏,徐兵河.乳腺癌治疗中紫杉类药物的选择——从药学机制到临床研究[J].临床肿瘤学杂志,2021,26(11):1046-1051.
[5] 徐佳茗,夏学军,刘玉玲. 紫杉醇新型制剂及临床研究进展[J]. 实用药物与临床, 2016, 19 (04): 510-517.


