NCB:清华大学郑撼球、青岛大学岳斌揭示了淋巴毒素-β在促进乳腺癌骨转移定植和进展的关键作用!
时间:2024-08-18 06:00:38 热度:37.1℃ 作者:网络
骨转移是乳腺癌的致命后果。
2024年8月15日,清华大学郑撼球、青岛大学岳斌共同通讯在Nature Cell Biology在线发表题为”Lymphotoxin-β promotes breast cancer bone metastasis colonization and osteolytic outgrowth“的研究论文,该研究表明淋巴毒素-β促进乳腺癌骨转移、定植和溶骨生长。
在这里,研究人员使用单细胞转录组学来研究骨转移定殖的分子机制,这是转移级联中的限速步骤。研究发现淋巴毒素-β (LTβ)在骨微环境中的肿瘤细胞中高度表达,这种表达与骨无转移生存率低有关。LTβ在多种乳腺癌模型中促进肿瘤细胞定植和生长。机制上,肿瘤源性LTβ通过核因子-κB2信号激活成骨细胞,分泌CCL2/5,促进肿瘤细胞粘附成骨细胞,加速破骨细胞形成,导致骨转移进展。在体内,用诱骗受体阻断LTβ信号传导可显著抑制骨转移,而临床样本分析显示,LTβ在骨转移中的表达明显高于原发肿瘤。

骨转移是乳腺癌常见的破坏性并发症,超过70%的患者会发生骨转移。此外,骨龛内的癌细胞可以作为癌症的种子,扩散到其他器官并导致广泛的转移。即使手术成功切除原发肿瘤后,惰性细胞仍可残留并引起骨复发。尽管大量癌细胞释放到血液循环中,但许多癌症患者仍然没有复发或经历延迟转移,循环肿瘤细胞数量超过显性转移灶。这一现象表明骨转移的定殖效率非常低,并强调了了解其分子机制的重要性。
先前的研究强调了肿瘤细胞与骨微环境(主要由成骨细胞、破骨细胞和血管周围细胞组成)相互作用在骨转移发展中的重要性。关键分子,如甲状旁腺激素相关肽、血管细胞粘附蛋白1 (VCAM-1)和整合素β3和JAGGED1-NOTCH信号通路介导这些相互作用,促进骨降解和转移性生长的恶性循环。在多步转移级联反应中,对于成功的骨转移,定植是效率最低的,但可能是最关键的。然而,尽管晚期溶骨信号研究得很好,早期骨定植信号仍然知之甚少。
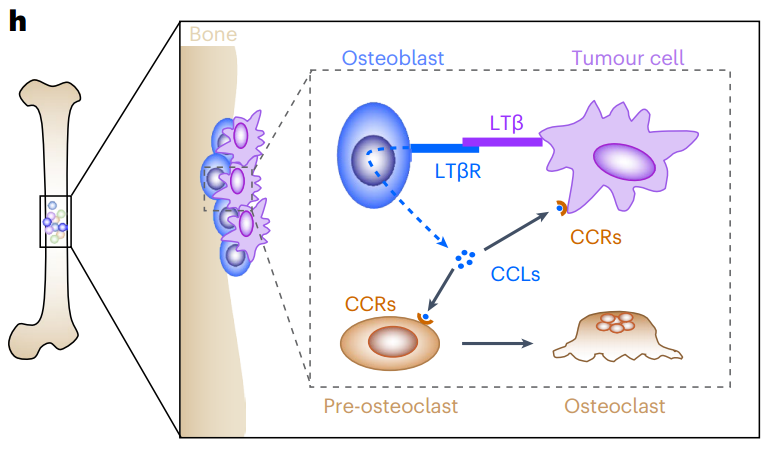
LTβ在骨转移、定植和休眠再激活中的作用(图源自Nature Cell Biology)
基因表达谱通过体内或体外选择产生的骨转移倾向细胞的培养研究,确定了参与骨转移的基因。癌细胞系的异质性表明,一个罕见的亚群可以在骨微环境中启动骨转移。骨源性线索可以影响肿瘤状态和基因表达,对骨定植和转移至关重要,但可能无法通过体外分析确定。因此,骨癌细胞的原位和体内基因谱分析是必不可少的。然而,有限数量的定植肿瘤细胞阻碍了对其转录组谱的理解。单细胞RNA测序(scRNA-seq)技术提供了一种揭示骨转移过程中定植信号的方法。
在该研究中,作者对实验性骨转移模型中早期骨定植获得的癌细胞进行了scRNA-seq分析,并确定了在定植阶段促进肿瘤细胞存活的潜在因素。利用体内迷你互补DNA (cDNA)文库筛选和验证,发现肿瘤坏死因子(TNF)超家族成员淋巴毒素-β (LTβ)可促进乳腺癌骨定植和最终的溶骨生长。该研究结果强调了LTβ是一种骨龛诱导因子,可促进肿瘤细胞定植和溶骨生长,并强调其作为骨转移性疾病患者的治疗靶点的潜力。
参考消息:
https://www.nature.com/articles/s41556-024-01478-9


