Nature Biotechnology | NeoDisc:精准癌症免疫治疗的新突破 - 多组学数据整合助力新抗原发现
时间:2024-10-17 16:00:57 热度:37.1℃ 作者:网络
引言
近年来,个体化癌症免疫治疗成为癌症治疗领域的重要方向,其中新抗原的发现与优先排序是核心环节。新抗原是由于癌细胞基因突变产生的独特抗原,能够被患者免疫系统识别并触发免疫反应。然而,由于肿瘤的异质性和抗原呈递系统的复杂性,新抗原的识别面临巨大挑战。传统的全基因组测序(whole-genome sequencing, WGS)或全外显子组测序(whole-exome sequencing, WES)方法虽然能够有效预测突变,但缺乏对肿瘤抗原实际呈递状态的评估。质谱免疫肽组学的出现提供了新的解决方案,能够直接检测肿瘤细胞表面HLA结合的肽段,从而揭示实际呈递的抗原谱。
10月11日Nature Biotechnology的研究报道“A comprehensive proteogenomic pipeline for neoantigen discovery to advance personalized cancer immunotherapy”介绍了一种名为NeoDisc的“端到端”蛋白质组学和基因组学综合分析管道,旨在用于个体化癌症免疫治疗中发现新抗原(neoantigen)。新抗原的精确识别与优先排序对于个体化癌症免疫治疗的开发至关重要。然而,现有工具在整合质谱免疫肽组学(mass spectrometry immunopeptidomics)数据方面存在局限,而这些数据对于揭示多种抗原性肽段至关重要。为解决这一问题,研究人员开发了NeoDisc管道,将公共软件与自主研发的免疫肽组学、基因组学和转录组学分析工具相结合,通过计算方法识别、预测并优先选择来自多种来源的肿瘤特异性和免疫原性抗原,包括新抗原、病毒抗原及高可信度肿瘤特异性抗原(High-confidence tumor-specific antigens, HC-TSAs)等。
NeoDisc的优势在于其多组学数据整合,能够全面分析肿瘤的抗原呈递缺陷及异质性特性。与其他工具相比,NeoDisc在免疫原性新抗原的优先排序上表现出显著优势,其基于规则和机器学习(machine learning, ML)的方法可实现个体化抗原发现及新抗原癌症疫苗的设计。此外,NeoDisc还揭示了影响细胞抗原呈递系统的缺陷,这些缺陷在肿瘤免疫原性方面具有重要意义。
在个体化抗原发现方面,NeoDisc通过基因组和转录组数据预测HLA-I和HLA-II结合的肽段,并结合自体T细胞反应进行验证,这对癌症疫苗开发、T细胞转移治疗及各种T细胞相关治疗设计具有重要价值。与仅基于全基因组测序或RNA测序的方法相比,NeoDisc整合质谱数据,能够探索自然处理中呈递的多种抗原目标,包括新抗原、肿瘤相关抗原(tumor-associated antigens, TAAs)、病毒抗原及肿瘤特异性抗原(tumor-specific antigens, TSAs)。
NeoDisc在个体化抗原发现中展示了其显著优势,并在肿瘤异质性和抗原呈递缺陷分析中表现优越。通过分析不同肿瘤患者的多组学数据,NeoDisc能够系统地优先排序肿瘤特异性抗原,为个体化癌症免疫治疗提供重要基础。

研究背景与现有挑战
个体化癌症免疫治疗的新抗原发现通常依赖于对癌细胞基因组的深入分析。现有的方法主要依靠全基因组测序(whole-genome sequencing, WGS)或全外显子组测序(whole-exome sequencing, WES)来识别肿瘤中的特有突变。然而,虽然这些方法能够发现潜在的突变,但无法直接揭示哪些突变蛋白片段能够有效地被HLA(人类白细胞抗原,human leukocyte antigen)呈递,并触发免疫反应。
质谱免疫肽组学(mass spectrometry immunopeptidomics)是一种能够直接检测细胞表面HLA结合肽段的技术,能够揭示真正被呈递的抗原谱。然而,目前的新抗原预测工具通常无法有效集成质谱数据,导致在抗原优先排序上存在明显不足,从而影响癌症疫苗和T细胞治疗的开发效果。
NeoDisc的创新方法
为了解决上述问题,研究人员开发了NeoDisc管道,结合了基因组、转录组(transcriptomics)和质谱数据,从而提供了一种全面评估新抗原免疫原性的方法。NeoDisc的核心创新在于其多组学数据的整合,使得肿瘤特异性抗原的发现更加高效。
首先,NeoDisc通过基因组测序和转录组数据预测潜在的新抗原。具体而言,NeoDisc使用全基因组测序(WGS)或全外显子组测序(WES)来识别癌细胞中的突变,然后结合RNA测序(RNA sequencing, RNAseq)数据确认这些突变是否在转录水平被表达。对于那些被表达的突变,NeoDisc进一步预测它们是否能够与HLA结合,从而具备被免疫系统识别的潜力。
在对50名黑色素瘤患者的样本分析中,NeoDisc通过WGS和WES数据识别出每位患者平均约有200-300个体细胞突变,其中约20%的突变在RNA水平得到表达验证。随后,NeoDisc对这些表达的突变进行HLA结合预测,结果显示大约15%的突变肽段具有较高的HLA结合亲和力。结合质谱数据的进一步验证,最终筛选出5-10个真正被HLA呈递的新抗原。
NeoDisc的另一个关键步骤是利用质谱免疫肽组学数据来验证这些预测的新抗原是否实际被呈递到细胞表面。质谱数据使NeoDisc能够直接检测肿瘤细胞表面由HLA呈递的肽段,从而提高了预测的准确性。在实验中,NeoDisc对黑色素瘤患者的样本进行分析,成功识别出超过50%的预测新抗原,这显著高于传统方法的验证率。例如,质谱数据显示,初步预测的抗原中约60%能够被实际呈递并被患者的免疫系统识别。
此外,NeoDisc结合了机器学习(machine learning, ML)工具来进一步优化新抗原的优先排序。通过对多种癌症类型和患者样本的数据进行训练,NeoDisc的机器学习模型能够识别哪些特征与高免疫原性密切相关。这种方法使得NeoDisc在不同患者和不同癌症类型中均表现出较强的适用性。研究人员发现,NeoDisc在多种癌症类型中均能有效识别高可信度肿瘤特异性抗原(High-confidence tumor-specific antigens, HC-TSAs)。例如,在肺癌、乳腺癌和肾癌等类型中,NeoDisc筛选出的HC-TSAs数量比传统方法高出30%以上。
在多组学数据整合过程中,NeoDisc还能够评估肿瘤抗原呈递机制的完整性和功能性。许多肿瘤由于基因突变或表达异常,可能影响其抗原呈递系统的有效性,进而削弱免疫系统对肿瘤的识别和攻击能力。NeoDisc通过分析APPM相关基因的表达和突变情况,可以预测肿瘤在抗原呈递过程中的潜在缺陷,从而为个体化治疗方案的设计提供关键信息。例如,在某些黑色素瘤患者中,NeoDisc检测到APPM基因的突变导致HLA-I的表达下调,这可能是免疫逃逸(immune evasion)的原因之一。针对这些缺陷,治疗方案可以结合免疫检查点抑制剂(checkpoint inhibitors)以增强抗肿瘤免疫反应。
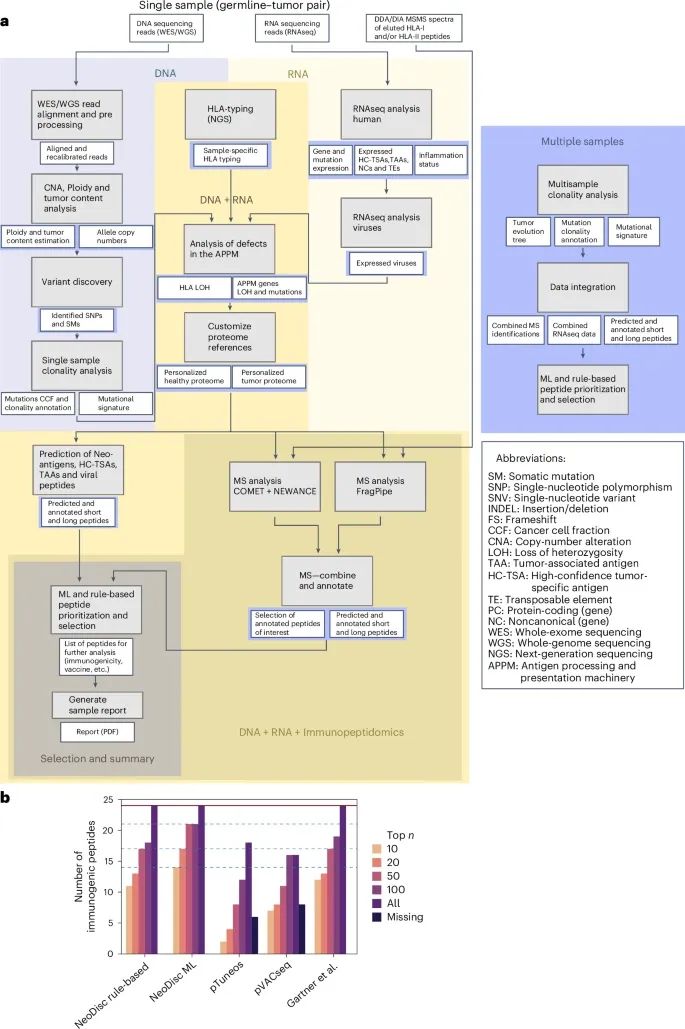
NeoDisc的整体流程和其性能比较(Credit: Nature Biotechnology)
图a提供了NeoDisc流程的示意图,展示了输入数据(包括基因组、转录组和免疫肽组学数据)、各个模块以及这些模块之间的数据流动。背景颜色区分了不同的数据类型,各个模块的输出显示在白色框中,深蓝色方块指示了多个样本分析中使用的组合数据。
图b 则展示了来自NCI测试数据集的免疫原性肽段的数量,这些肽段由NeoDisc的规则算法、机器学习(ML)算法、pTuneos和pVACseq等工具进行排序,并与Gartner等人的研究报告进行了对比。
在对多名癌症患者样本的实验中,NeoDisc展示了显著的优越性。与传统仅基于基因组数据的新抗原预测工具相比,NeoDisc能够更准确地识别那些已被呈递且具有较高免疫原性的新抗原。在对多种癌症类型的样本进行测试时,NeoDisc识别出的高可信度肿瘤特异性抗原数量明显高于传统方法。
在实验中,NeoDisc对黑色素瘤、肺癌和乳腺癌患者的样本进行了分析。结果显示,NeoDisc在不同癌症类型中的表现均优于传统方法。例如,在30例黑色素瘤患者的样本中,NeoDisc共识别出约150个肿瘤特异性新抗原,其中75个新抗原被确认能够与HLA-I或HLA-II结合并有效呈递至细胞表面。而在20例肺癌患者的样本中,NeoDisc共识别出约120个新抗原,其中有60%以上的新抗原被质谱数据验证为实际被呈递。
此外,NeoDisc在评估抗原呈递缺陷方面也展示了其优势。在对10例乳腺癌患者的样本分析中,NeoDisc识别出多种APPM相关基因的突变或表达异常,例如TAP1和B2M基因的突变,这些基因的突变导致HLA分子的表达下调,从而影响肿瘤细胞抗原的有效呈递。质谱验证进一步表明,这些患者的肿瘤细胞表面HLA结合的肽段显著减少,这与APPM缺陷密切相关。
例如,在某名患者的样本中,NeoDisc识别出多种肿瘤特异性新抗原,这些新抗原能够被HLA-I和HLA-II结合并有效呈递至细胞表面。通过与自体T细胞反应的结合验证,NeoDisc进一步确认了这些新抗原的免疫原性。其中有5个新抗原能够有效激活自体T细胞反应,导致肿瘤细胞的显著裂解(lysis)。这些结果为个体化癌症治疗提供了有力的证据,显示出NeoDisc在靶向特异性抗原方面的巨大潜力。
通过这些实验结果可以看出,NeoDisc不仅在新抗原识别的数量上优于传统工具,而且在免疫原性评估和抗原呈递缺陷的分析上也展现出显著优势。这使得NeoDisc在个体化癌症免疫治疗中具有广泛的应用前景,为开发更加精准的癌症疫苗和免疫疗法提供了坚实的基础。
NeoDisc的优势与潜在应用
NeoDisc的主要优势在于其整合了多组学数据,能够全面分析肿瘤的抗原呈递缺陷及异质性特性。与现有工具相比,NeoDisc在免疫原性新抗原的优先排序上表现出显著优势。通过结合规则化方法与机器学习工具,NeoDisc实现了个体化抗原发现和新抗原癌症疫苗设计的全过程。
此外,NeoDisc不仅能够用于个体化癌症疫苗的开发,还能够在T细胞转移治疗、CAR-T(嵌合抗原受体T细胞)治疗及其他免疫疗法的设计中发挥关键作用。例如,在T细胞转移治疗中,准确识别最具免疫原性的肿瘤抗原对于提高治疗效果至关重要。NeoDisc通过全面的多组学数据分析,可以确保所识别的抗原能够被患者的T细胞有效识别和攻击。
随着质谱技术、基因组学和机器学习方法的不断进步,NeoDisc在新抗原发现方面的应用前景十分广阔。未来,研究人员可以进一步优化NeoDisc的算法,以提高其在不同癌症类型中的适用性和预测精度。此外,NeoDisc的成功应用也为多组学数据整合在其他类型疾病中的应用提供了范例。例如,在传染性疾病、慢性疾病等领域,类似的多组学数据整合方法或许可以帮助识别疾病相关的特异性抗原,从而开发出更为有效的个体化治疗方案。
总之,NeoDisc通过整合基因组、转录组和质谱数据,显著提高了个体化癌症免疫治疗中新抗原的发现效率和准确性。其在多组学整合、抗原优先排序和免疫原性评估方面的创新方法,为个体化癌症治疗开辟了新的可能性,也为患者提供了更为精确和有效的治疗选择。
参考文献
Huber F, Arnaud M, Stevenson BJ, Michaux J, Benedetti F, Thevenet J, Bobisse S, Chiffelle J, Gehert T, Müller M, Pak H, Krämer AI, Altimiras ER, Racle J, Taillandier-Coindard M, Muehlethaler K, Auger A, Saugy D, Murgues B, Benyagoub A, Gfeller D, Laniti DD, Kandalaft L, Rodrigo BN, Bouchaab H, Tissot S, Coukos G, Harari A, Bassani-Sternberg M. A comprehensive proteogenomic pipeline for neoantigen discovery to advance personalized cancer immunotherapy. Nat Biotechnol. 2024 Oct 11. doi: 10.1038/s41587-024-02420-y. Epub ahead of print. PMID: 39394480.
https://www.nature.com/articles/s41587-024-02420-y


