JCI子刊:细胞内补体系统驱动肺动脉高压中血管成纤维细胞的代谢和促炎重编程
时间:2025-02-28 12:08:45 热度:37.1℃ 作者:网络

近日,一项突破性研究揭示了补体系统,特别是细胞内补体系统(“complosome”),在肺动脉高压(PH)发病机制中的关键作用。该研究为 PH 的免疫炎症机制提供了新视角,并可能为未来精准治疗提供新的靶点。
肺动脉高压是一种严重的心肺疾病,其主要特征是肺血管重塑,导致肺动脉压力升高、血管阻力增加,最终引发右心衰竭。近年来,科学界已广泛认识到炎症在 PH 进展中的重要作用,而补体系统作为免疫系统的重要组成部分,其具体作用仍未被充分探索。
研究揭示炎症与补体系统的紧密联系
研究团队利用先进的数字空间分析技术,对肺动脉高压患者的血管病变进行了深入研究。结果显示,多个炎症相关信号通路(包括干扰素信号、TNF 信号、移植物排斥、缺氧及 IL2/IL6/Jak-Stat 信号通路)在 PH 患者的血管外膜和丛状病变中显著富集。这一发现与成纤维细胞介导的炎症在 PH 发病机制中的作用相一致。
进一步研究发现,在特发性肺动脉高压(IPAH)患者的肺动脉外膜中,多种补体级联反应的核心成员(如 C3、C1Q、C1S、C7、CFD 及调节蛋白 CFH)表达水平明显升高,提示补体系统在 PH 炎症反应中的潜在关键作用。
细胞内补体系统(complosome)或成关键调控因子
补体系统传统上被认为主要在血浆中循环发挥作用,而最新研究表明,它在细胞内同样具有重要功能。在 T 细胞、B 细胞、中性粒细胞及巨噬细胞等免疫细胞中,complosome 在维持细胞稳态和调节效应功能方面起着核心作用。此外,其活性还涉及上皮细胞、内皮细胞、间皮细胞及成纤维细胞。
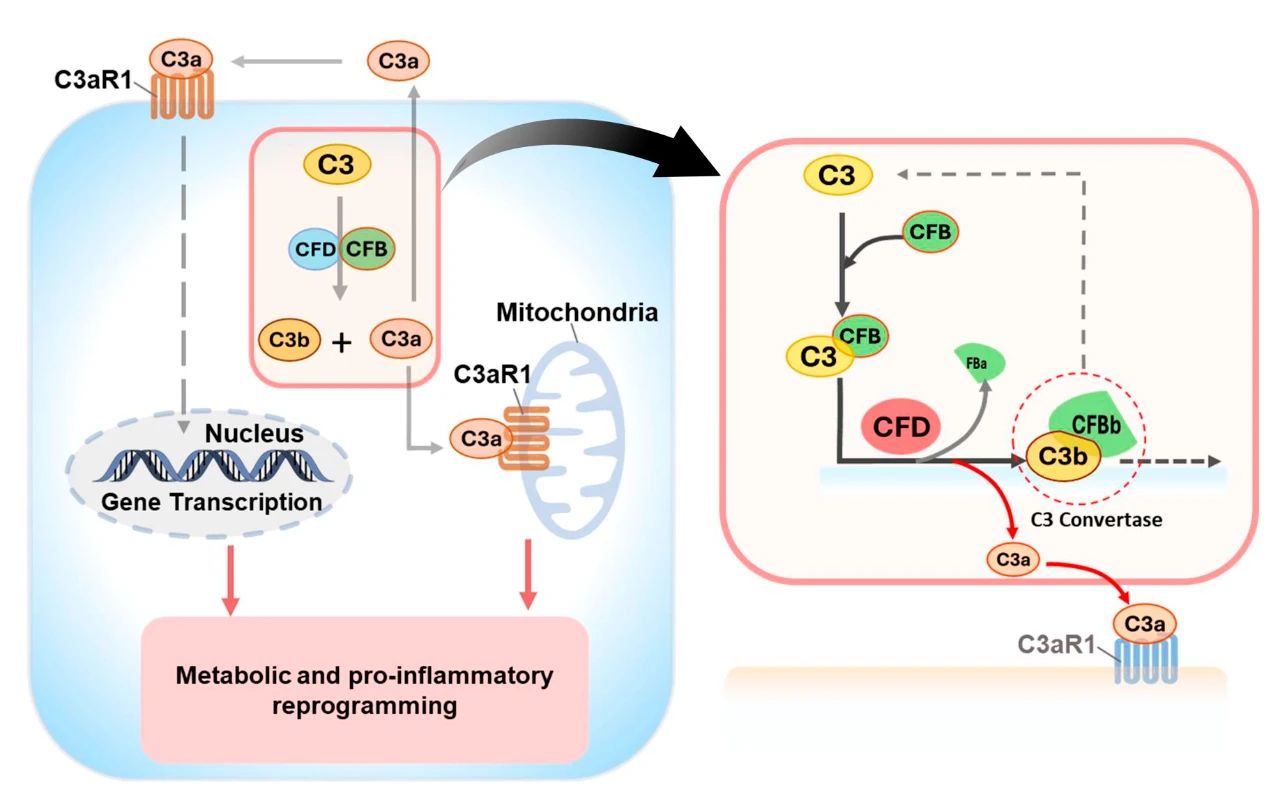
研究人员通过体外实验发现,肺动脉成纤维细胞可自主产生多种补体成分(包括 C3、CFB 和 CFD)。当 C3 在细胞内被激活后,其活化片段 C3b 可与 CD46 结合,进一步激活 mTOR 营养感应通路并促进葡萄糖摄取。此外,补体 C3a 受体(C3aR1)和 C5a 受体(C5aR1)定位于线粒体外膜,调节活性氧(ROS)生成与 ATP 产生的平衡,从而影响细胞代谢。
研究或为 PH 治疗提供新靶点
为了深入探讨补体系统在 PH 发病过程中的具体机制,研究团队采用了肺动脉成纤维细胞的体内外模型,并结合基因操作、药物阻断、蛋白质相互作用分析、转录分析及质谱代谢组学分析等多种技术手段。研究发现,CFD 介导的 C3 及其片段的激活可显著调节肺动脉外膜成纤维细胞的代谢功能,并促使其维持持续的促炎表型。
这一发现表明,补体系统,尤其是细胞内补体系统,可能在 PH 的慢性炎症和代谢失衡中发挥重要作用。这为未来开发针对 PH 的免疫干预策略提供了新的方向。
研究团队表示:“我们的研究揭示了补体系统在肺动脉高压中的新作用,特别是其在成纤维细胞内的活性及代谢调控功能。未来,针对补体系统的精确干预可能成为 PH 免疫治疗的新策略。”
这项研究为 PH 研究领域带来了新的突破,并为未来的个性化治疗提供了重要的理论基础。随着科学家们对补体系统功能的深入探索,期待未来能够开发出更有效的治疗方案,造福全球 PH 患者。


