Lancet Oncol:抗PD-L1抗体Avelumab是否可用于卵巢癌的一线治疗?
时间:2021-08-08 23:01:44 热度:37.1℃ 作者:网络
虽然大多数上皮性卵巢癌患者采用以铂类为基础的一线化疗可获得缓解,但约70%的患者会在3年内复发。3期JAVELIN Ovarian 100试验对比了初治的上皮性卵巢癌患者采用抗PD-L1单克隆抗体avelumab联合化疗继以avelumab维持治疗,或化疗后继以avelumab维持治疗,或单纯化疗的效果和安全性。
JAVELIN Ovarian 100试验是一项全球的、开放标签的、三组治疗臂的随机化3期试验,在25个国家的159家医院和癌症中心招募年满18岁的III-IV期上皮性卵巢癌、输卵管癌或腹膜癌患者。受试患者被随机(1:1:1)分成三组,接受相应的治疗。主要终点是无进展生存期(PFS)。
2016年5月19日至2018年1月23日期间,共998位患者被随机分至三组:avelumab维持组 n=332、avelumab联合组 n=331和对照组 n=335。在预定的中期分析时(截止2018年9月7日),无进展生存分析结果超过了预定的无效界限,试验因此而终止。
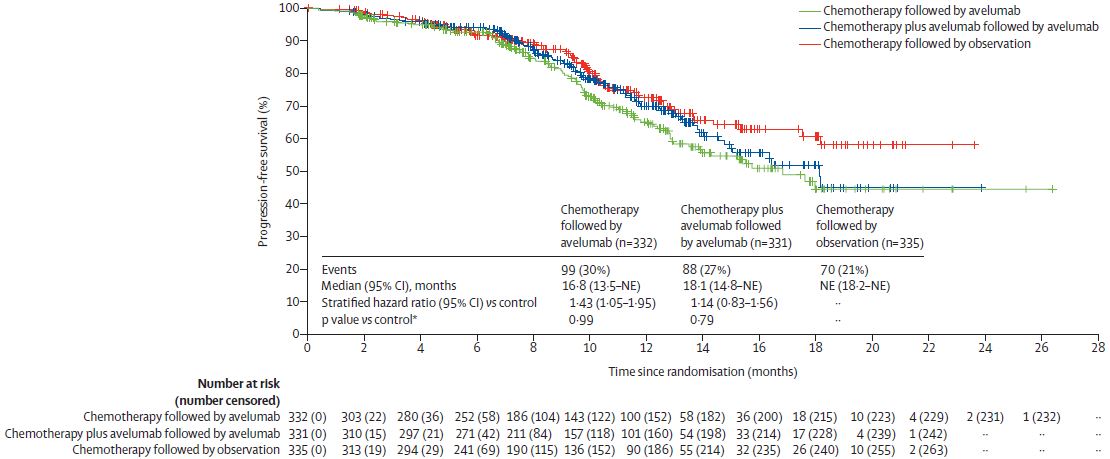
三组患者的无进展生存期
所有患者的中位随访时间为10.8个月:avelumab维持组、avelumab联合组和对照组的中位随访时间分别是11.1个月、11.0个月和10.2个月。avelumab维持组、avelumab联合组和对照组的中位PFS分别是16.8个月、18.1个月和1未达到。与对照组相比,avelumab维持组和avelumab联合组的PFS的分层危险比分别是1.43(p=0.99)和1.14(p=0.79)。
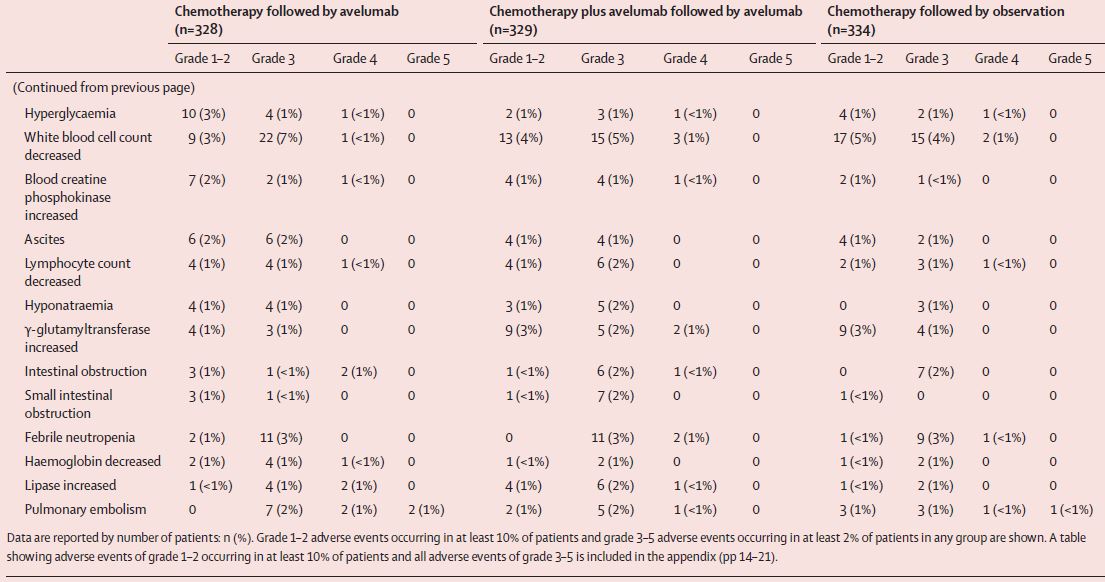
不良反应
最常见的3-4级不良反应有贫血(21% vs 19% vs 16%)、中性粒细胞减少(28% vs 30% vs 26%)和中性粒细胞计数减少(15% vs 14% vs 18%)。avelumab维持组、avelumab联合组和对照组分别发生了92例(28%)、118例(36%)和64例(19%)重度不良反应。avelumab维持组和avelumab联合组各有一例治疗相关死亡(维持组死于房颤、联合组死于疾病进展)。
综上所述,虽然没有观察到新的安全性问题,但该研究结果不支持在上皮性卵巢癌患者的一线治疗中使用avelumab。需要替代治疗方案来改善晚期上皮性卵巢癌患者的预后。
原始出处:
Bradley Monk, et al. Chemotherapy with or without avelumab followed by avelumab maintenance versus chemotherapy alone in patients with previously untreated epithelial ovarian cancer (JAVELIN Ovarian 100): an open-label, randomised, phase 3 trial. The Lancet Oncology. August 04, 2021. https://doi.org/10.1016/S1470-2045(21)00342-9