Nat Immu:李斌团队揭示胰岛素信号调控脂肪组织驻留Treg不同亚型分化及功能调控的机制
时间:2021-08-26 10:02:06 热度:37.1℃ 作者:网络
人体组织如皮肤、肌肉、大脑和结肠等组织特异性Treg细胞发育及其生理病理功能与多种重大疾病临床治疗密切相关,也是近年来本领域研究热点。单细胞测序发现部分外周组织Treg细胞染色质甲基化区域及其转录组与淋巴器官来源的Treg细胞有较大不同,表明外周组织Treg细胞存在组织适应性发育。同时,外周组织Treg细胞有着调节组织代谢、干细胞维持和促进伤口愈合等非经典作用,在多种疾病的治疗中具有重要的临床应用前景。
脂肪组织驻留调节性T(Regulatory T, Treg)细胞对维持机体免疫稳态和代谢平衡至关重要。Treg细胞在正常脂肪组织中大量存在,而在肥胖小鼠中数量明显减少,在肥胖导致的脂肪组织炎症及代谢紊乱中起重要调控作用,为治疗肥胖、2型糖尿病及其他代谢综合征提供新思路。
脂肪组织微环境中,在抗原、IL-33、IFN-α、胰岛素、雄性激素等多种生理信号刺激下,Treg细胞表达多种独特的基因模块,并呈现出组织适应性发育和功能多样化。
2021年8月24日,上海交通大学医学院上海市免疫学研究所李斌课题组及合作团队在国际著名期刊Nature Immunology 在线发表了题为“Insulin signaling establishes a developmental trajectory of adipose regulatory T cells”的研究论文。该研究发现胰岛素信号直接调控Treg细胞脂肪组织适应性发育及其代谢调控功能。

本研究利用单细胞ATAC测序以及可匹配的单细胞RNA和TCR测序追踪Treg细胞组织适应性发育,鉴定出具有不同生理功能的CD73hi和ST2hi脂肪组织驻留Treg细胞亚群。此外,CD73hi和ST2hi脂肪组织驻留Treg细胞亚群共享部分TCR克隆,提示亚群间存在细胞状态相互转化(图A)。
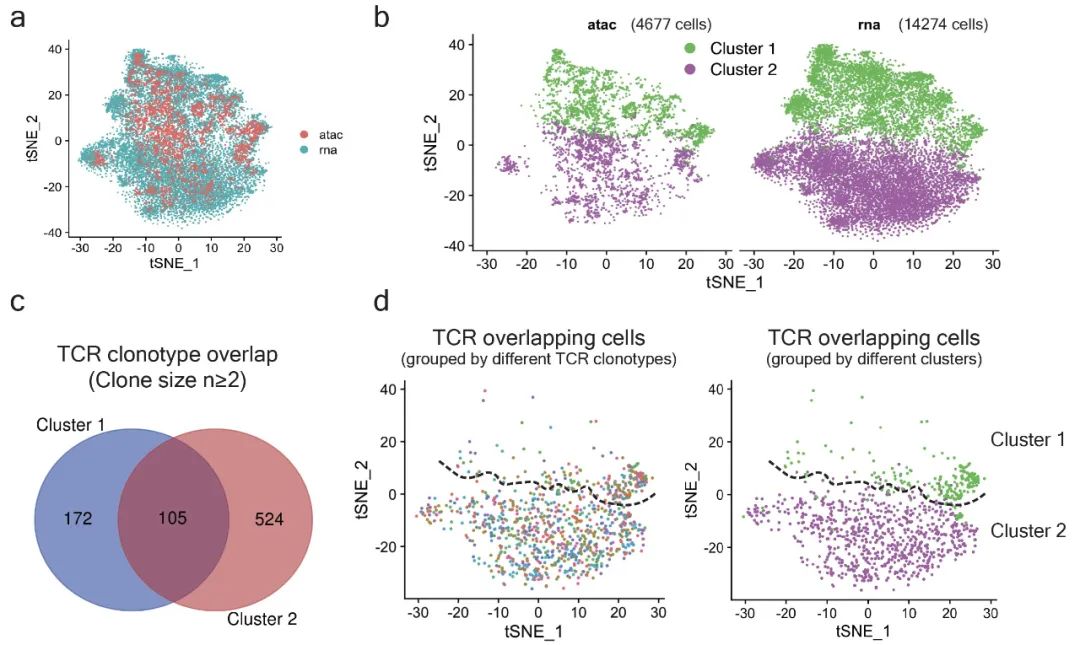 图A 单细胞测序揭示肪组织驻留Treg细胞亚群
图A 单细胞测序揭示肪组织驻留Treg细胞亚群
团队进一步研究发现胰岛素信号通过HIF-1α-Med23-PPAR-γ 轴驱动CD73hiST2lo 向CD73loST2hi 脂肪Treg细胞亚群转化。在Treg细胞中敲除胰岛素受体(Insr)、Hif1α或Med23等基因将下调转录因子PPAR-γ 表达,并促进CD73hiST2lo 脂肪Treg细胞亚群富集以及代谢产物腺苷的积累,从而改善机体胰岛素敏感性并激活米色脂肪产生。ST2hi脂肪Treg细胞亚群分泌sST2蛋白,通过中和细胞因子IL-33抑制米色脂肪产生。
此项工作建立了胰岛素信号调控脂肪组织驻留Treg细胞的发育轨迹模型,揭示生理和病理环境中胰岛素信号如何通过HIF-1α/Med23-PPAR-γ轴来调节脂肪Treg不同亚群间的动态变化和生理功能(图B),客观解释了之前其他国际团队以组织驻留Treg细胞整体作为研究对象时得出的相互矛盾性结果及疑惑。该发现为胰岛素抵抗性糖尿病重症患者临床免疫治疗提供了新思路新手段。
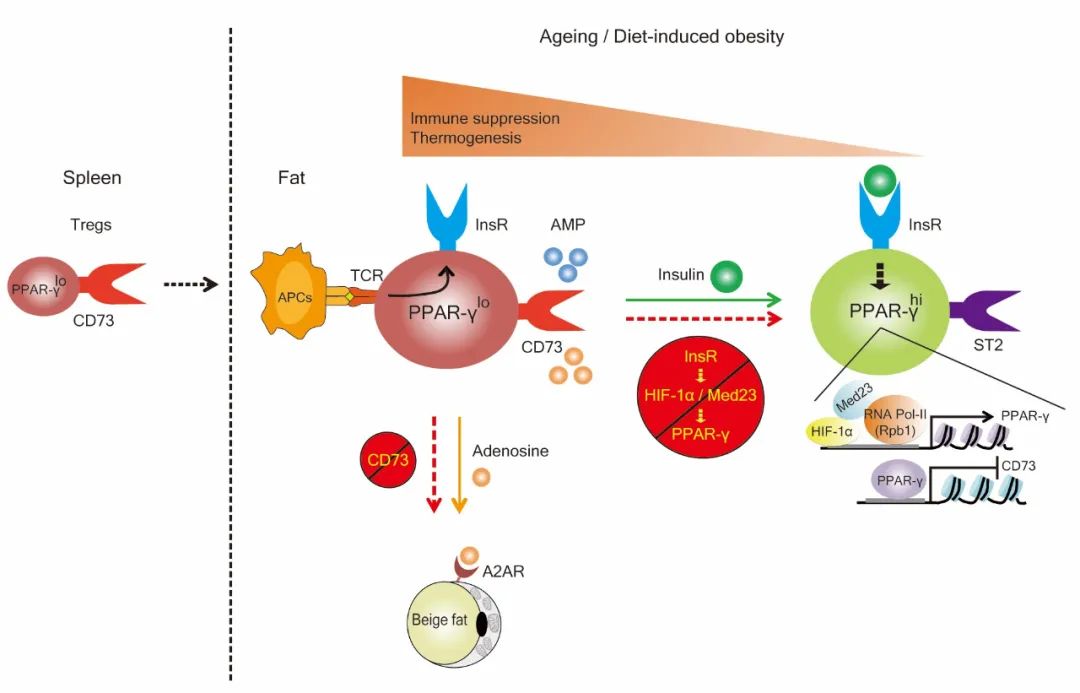 图B 胰岛素信号调控脂肪组织驻留Treg细胞的发育轨迹模型
图B 胰岛素信号调控脂肪组织驻留Treg细胞的发育轨迹模型
上海市免疫学研究所博士后李扬扬和上海交通大学基础医学院博士后卢颖为该研究论文的共同第一作者,通讯作者为上海市免疫学研究所李斌研究员、上海交通大学基础医学院童雪梅研究员和复旦大学生命科学学院王纲教授。本研究受到国家自然科学基金、国家重点研发计划、上海市科学技术委员会科学基金、上海交通大学与香港中文大学合作研究计划、余㵑学者计划等项目资助,依托上海市免疫学研究所公共平台、上海交通大学医学院基础医学院公共技术平台、上海交通大学医学院动科部、赛业生物动科部等的技术支持,得到来自上海交通大学医学院附属瑞金医院、上海交通大学医学院附属第九人民医院、中国科学院上海巴斯德研究所、华中科技大学、上海中医药大学附属光华医院关节炎研究所、郑州大学第一附属医院肝胆胰疾病及消化器官移植重点实验室等单位的大力协助。特别致谢免疫所苏冰教授、陈磊研究员及相关课题成员等在本研究中给予大力支持帮助的所有老师同学。
【通讯作者简介】
李斌研究员是上海市免疫学研究所科研副所长&课题组长,二级研究员、余㵑学者、上海交大特聘教授、国家基金委免疫学杰青、上海市领军人才、上海市优秀学科带头人,普米斯生物联合创始人&科学委员会主席,姑苏领军人才;高探生物科学委员会主席;中国细胞生物学学会科学普及工作委员会主任委员&免疫细胞生物学分会副会长、欧美同学会上海生物医药分会会长;Science Bulletin副主编 (2018)、European Journal of Immunology执行委员会成员(2020)、Cellular & Molecular Immunology 编委 (2018)。
李斌研究员长期从事调节性T细胞相关基础及临床基础研究,近年来在炎症条件下Treg细胞功能稳定性及组织特异性Treg亚型分化,抗病毒广谱宿主限制性因子翻译后修饰及其相关酶类的活性调节等方面的研究取得了突出成绩。2009年回国至今,相关研究成果在国际学术刊物如NATURE IMMUNOLOGY、IMMUNITY、GASTROENTEROLOGY、PNAS、NAT COMMS、J BIOL CHEM、J IMMUNOL、J VIROL、PLOS Pathogens 、EMBO Rep 等发表通讯及共同通讯作者文章60余篇。先后承担国家自然科学基金杰出青年基金、重点项目(3项)、中美及中波国际合作项目、国家重点研发计划子课题负责人等重大科研任务多项。
原始出处:
Li Y, Lu Y, Lin SH, Li N, Han Y, Huang Q, Zhao Y, Xie F, Guo Y, Deng B, Tsun A, Du J, Li D, Sun J, Shi G, Zheng F, Su X, Duan S, Zheng SG, Wang G, Tong X, Li B. Insulin signaling establishes a developmental trajectory of adipose regulatory T cells.Nat Immunol. 2021 Aug 24. doi: 10.1038/s41590-021-01010-3.


