Front Oncol:信迪利单抗(Sintilimab)二线或以上治疗晚期或转移性胃癌疗效的回顾性研究
时间:2021-09-23 22:01:32 热度:37.1℃ 作者:网络
胃癌是我国常见的恶性肿瘤之一,而且诊断时大部分处于局部晚期或转移性,导致治疗效果差,预后差。免疫治疗已经被用于多种肿瘤的治疗。基于ATTRACTION-02和KEYNOTE-059研究,nivolumab和pembrolizumab已分别在日本和美国被批准用于晚期胃癌的三线治疗。信迪利单抗(Sintilimab)是我国国产的PD-1抑制剂。在中国已经获批复发/难治性霍奇金淋巴瘤,而且在多种肿瘤中,包括胃癌,也正在进行研究。近期,来自我国河南省肿瘤医院的团队开展了回顾性研究,评估信迪利单抗(Sintilimab)二线或以上治疗晚期或转移性胃癌的疗效和安全性。相关结果发表在Frontiers in Oncology杂志上。

该研究回顾性分析了2019年3月至2020年7月在既往全身治疗后进展并接受sintilimab治疗的晚期或转移性胃癌患者。主要终点为无进展生存期(PFS)。次要终点包括客观缓解率(ORR)、疾病控制率(DCR)、总生存率(OS)和安全性。
研究纳入52例患者,中位年龄64岁(范围30 80岁),其中女性17例,男性35例。所有患者均诊断为晚期或复发;转移部位包括腹内淋巴结(65.4%)、肝脏(42.3%)、腹膜(28.8%)和肺(25%)。19例(36.5%)患者接受sintilimab作为二线治疗,33例患者(63.5%)为三线或以上治疗。8例患者接受sintilimab单药治疗,44例患者接受sintilimab联合治疗。44例患者接受联合治疗,24例患者接受sintilimab联合阿帕替尼治疗,20例患者接受sintilimab联合白蛋白-紫杉醇或伊立替康治疗。
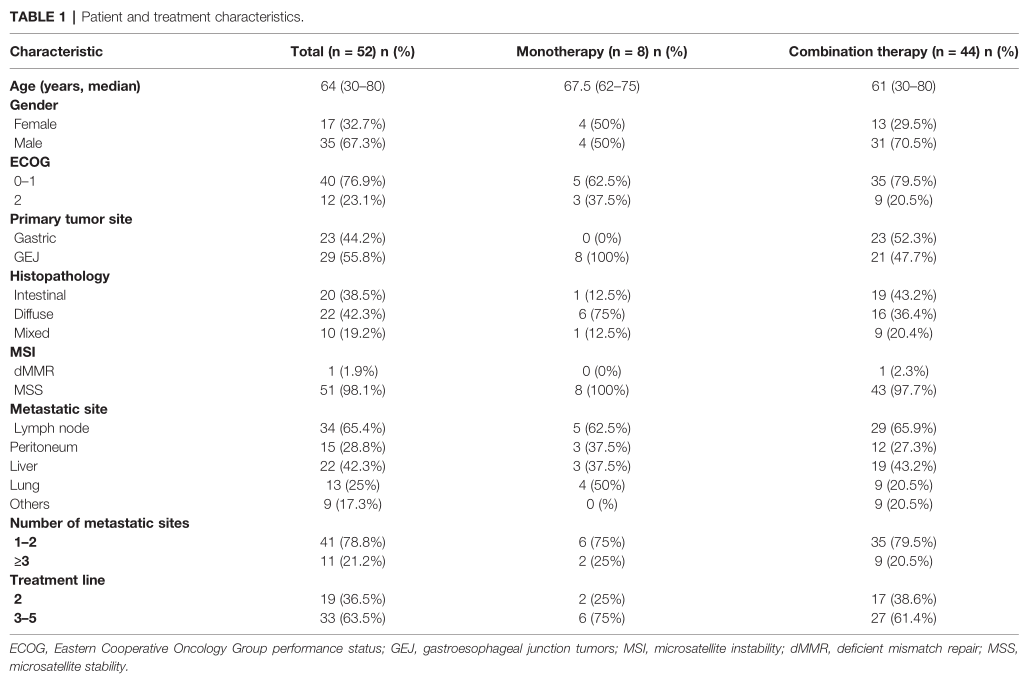
临床特征
在总体人群中,未观察到CR, 8例患者达到PR, 26例患者达到SD, 18例患者出现PD。ORR和DCR分别为15.4%(8/52)和65.4%(34/52)。在肠型人群中, ORR和DCR分别为30.0%(6/20)和80.0%(16/20)。非肠型人群中, ORR和DCR分别为6.3%(2/32)和56.3%(18/32)。PD- L1阳性人群中,ORR和DCR分别为57.1%(4/7)和100%(7/7)。在PD- L1阴性人群中, ORR和DCR分别为7.1%(1/14)和64.3%(9/14)。在sintilimab单药治疗人群中,ORR和DCR分别为12.5%(1/8)和50.0%(4/8)。在联合治疗人群中,ORR和DCR分别为15.9%(7/44)和68.2% (30/44)。
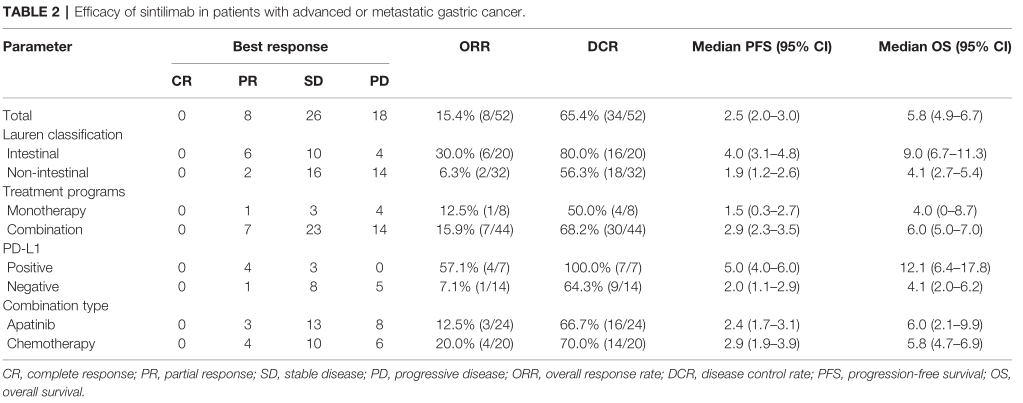
疗效评估
总体人群的中位PFS和OS分别为2.5个月(95% CI = 2.0 3.0)和5.8个月(95% CI = 4.9 6.7)。
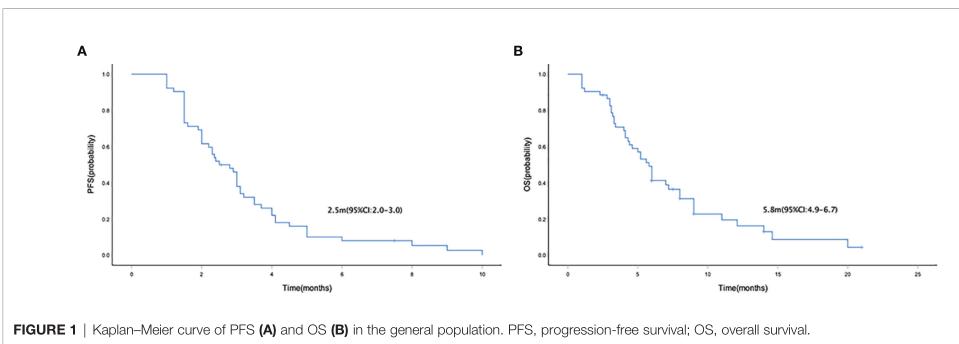
PFS和OS
sintilimab单药和联合组的中位PFS分别为1.5 个月(95% CI = 0.3–2.7) 和2.9个月 (95% CI =2.3–3.5) ,没有统计学差异(p = 0.088);而两组的OS分别为4.0个月 (95% CI = 0 8.7)和6.0 个月(95% CI = 5.0 7.0),也没有统计学差异(p = 0.133)。
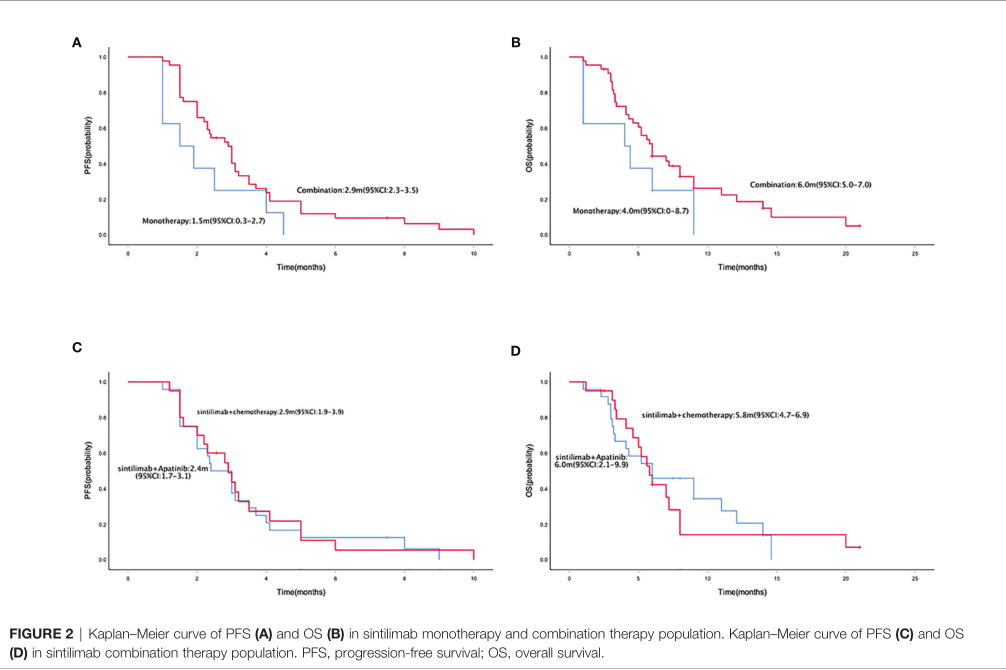
单药和联合治疗的PFS和OS
肠型和非肠型患者的中位PFS分别为4.0个月(95% CI = 3.1 4.8)和1.9个月(95% CI = 1.2 2.6) (p = 0.000);而中位OS分别为9.0个月(95% CI = 6.7 11.3)和4.1个月(95% CI = 2.7 5.4)(p = 0.000)。PD - L1阳性和阴性患者的中位PFS分别为5.0个月(95% CI = 4.0 6.0)和2.0个月(95% CI = 1.1 2.9)(p = 0.000)。PD-L1阳性和PD-L1阴性患者的中位OS分别为12.1个月(95% CI = 6.4 17.8)和4.1个月(95% CI = 2.0 6.2)(p = 0.027)。
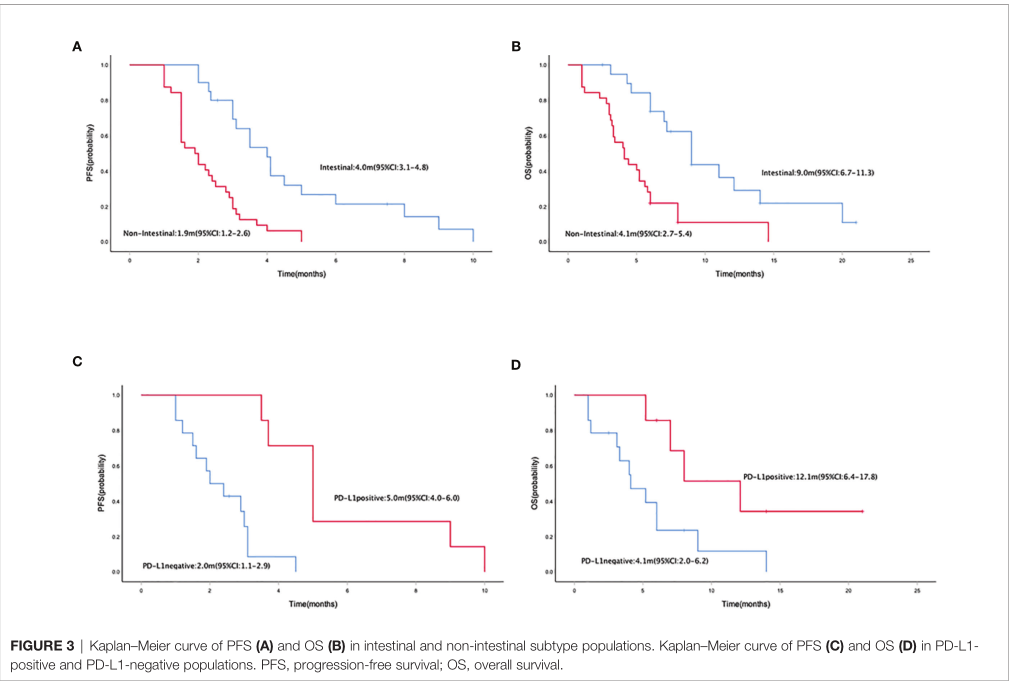
亚组分析PFS和OS
所有患者都发生不良反应。大多数不良反应(AEs)为1-2级。3-4级不良反应发生在23例(44.2%)患者中。
综上,研究表明,信迪利单抗(Sintilimab)二线或以上治疗晚期或转移性胃癌是可行的治疗策略,而且在肠型患者中要优于非肠型患者。
原始出处:
Nie C, Lv H, Liu Y, et al (2021) Clinical Study of Sintilimab as Second-Line or Above Therapy in Patients With Advanced or Metastatic Gastric Cancer: A Retrospective Study. Front. Oncol. 11:741865. doi: 10.3389/fonc.2021.741865


