JACC:心力衰竭引起的肺动脉高压
时间:2021-11-04 12:02:00 热度:37.1℃ 作者:网络

左心疾病相关的肺动脉高压 (PH-LHD) 是PH中最常见的形式,也被分成毛细血管后或第2大类PH。人们对PH-LHD的病理生理学、临床演变和治疗非常感兴趣。特别是在过去十年中,PH 和右心室功能障碍 (RVD) 一直是射血分数保留的心力衰竭 (HFpEF) 的关注焦点,这种情况与射血分数降低的心力衰竭 (HFrEF) 具有相似的临床表现和事件发生率,但在病因、心脏重构、病理生理学、共存疾病和对治疗的反应方面有所不同。在 HFrEF 中,PH的研究一直处于患者末期阶段(即等待左心室辅助装置 [LVAD] 或心脏移植的患者)。然而,在 HFpEF 中,PH 的作用受到严格审查,鉴于高流行病学影响和缺乏有效管理,需要彻底识别假定的机制。
因此,尽管血流动力学特征和结果相似,但在这 2 种情况下,PH 的分子途径、病理生理学和临床表现可能会有所不同,因此存在一些值得特别关注的有趣问题。 这在预防和治疗方面具有明显的意义。强调了 PH-HFrEF 和 PH-HFpEF 之间的潜在差异,主要目的是指导新疗法的研究工作。具体而言,就是关注在2种 HF 条件下观察到的左心驱动力生物途径、血流动力学和临床表型的特征性紊乱。
PH-LHD的定义、特征和流行病学
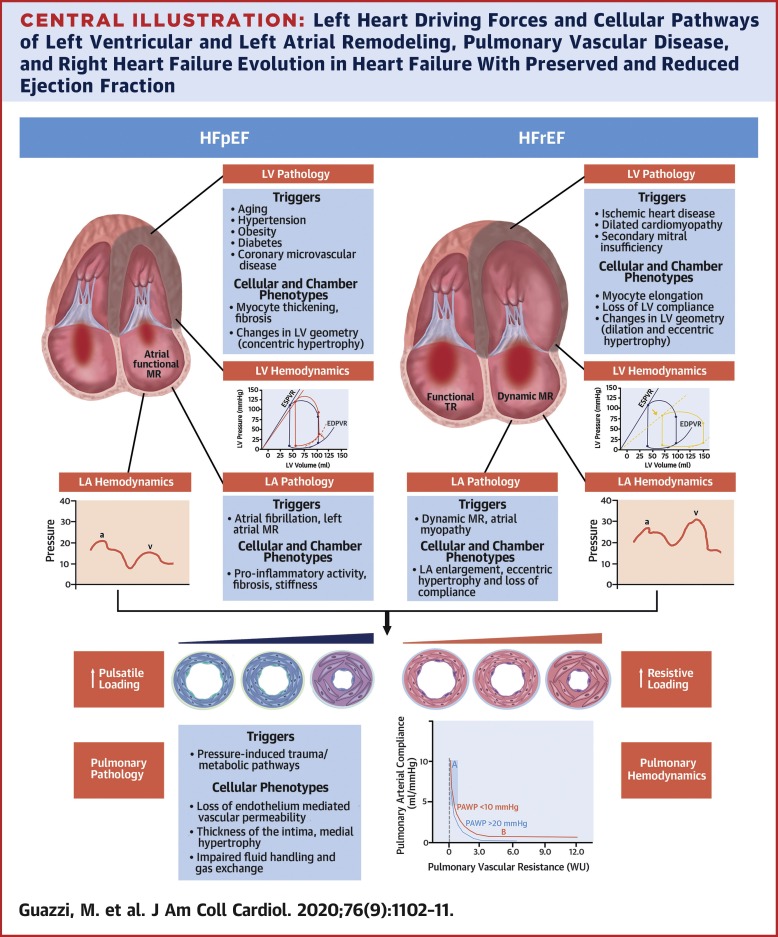
2018年 WHO会议上,PH-LHD被定义为平均肺动脉压 (mPAP)>20 mmHg和肺动脉楔压 (PAWP)>15 mmHg。孤立的毛细血管后 (Ipc)-PH 或毛细血管前和毛细血管后 (Cpc)-PH 的组合分别定义为肺血管阻力 (PVR)<3 WU 或≥3 WU。常见的左心疾病包括瓣膜病或先天性心脏病。但是对于PH-HFrEF 和 PH-HFpEF 却存在着差异。通常,PH-HFpEF 患者是具有代谢综合征特征的老年女性 ,当代谢综合征和肥胖并存时,会观察到更差的 PH 表型。PH-HFpEF 的其他触发因素包括微血管冠状动脉疾病、心房颤动 (AF)、慢性肾病和慢性阻塞性肺病。PH-HFrEF 在患有冠心病或扩张型心肌病的中年男性中更为常见。
左心驱动力和血液动力学
在HFrEF和HFpEF中,PH 的主要血流动力学驱动因素是 LV 松弛和充盈受损,这会导致左心房压力 (LAP) 向后传输到静脉系统、毛细血管和动脉,并最终传输到右心。LAP抬高是LV重构类型与左心房 (LA) 尺寸和动态适应之间相互作用的结果。事实上,LV 肌细胞肥大的类型以及反应性和替代性纤维化的数量很好地将HFpEF与HFrEF区分开来。
LV 充盈受损和心脏重塑
在 HFpEF 中,LV 向心性肥厚和舒张僵硬度增加在高血压和肥胖症中很常见。 大约三分之一的患者可能患有糖尿病,10% 至 15% 的患者可能患有浸润性疾病,例如心脏淀粉样变性,然而,正如最近的 HFA 所表明的那样,这是一种需要诊断并排除在典型 HFpEF 表型之外的疾病 -PEFF 分数。 合并症会对心肌产生负面影响,刺激氧化应激和肥大途径。
在 HFrEF 中,LV 形态和肌细胞适应是由过度的壁应力驱动的,在大多数情况下是由于缺血和有利于腔室扩张和离心肥大的肌细胞遗传背景。心肌细胞丢失改变了胶原蛋白沉积和降解之间的平衡,并且通过替换死心肌细胞形成纤维化斑块区域。
LAP 和肺血流动力学表型增加
LAP 的任何增加,即使是轻微的增加,都会扰乱肺血流动力学并加重症状。 肺血流动力学在不同 LAP 阶段的纵向变化是不确定的; 然而,比较肺血流动力学以响应 PH-HFrEF 和 PH-HFpEF 中 LAP 的长期升高提供了有趣的差异。 对于相似的平均 PAWP,PH-HFpEF 具有更高的 DPG 和 PVR、相似的动脉顺应性和更低的 MR 率,表明在相似的脉动负荷下血管疾病更明显,并且可能反映了继发于炎症的更严重的肺微血管病变。运动期间对肺血流动力学的彻底评估定义了不同的病理生理学特征,有助于揭示特殊的血流动力学模式。
肺血管疾病与重塑的病理生物学
不考虑 LVEF,内皮损伤是 PH 微血管功能障碍的核心。 对人类肺血管系统的研究有限,但临床前证据和遗传/表观遗传血液组学分析产生了大量数据。
静脉
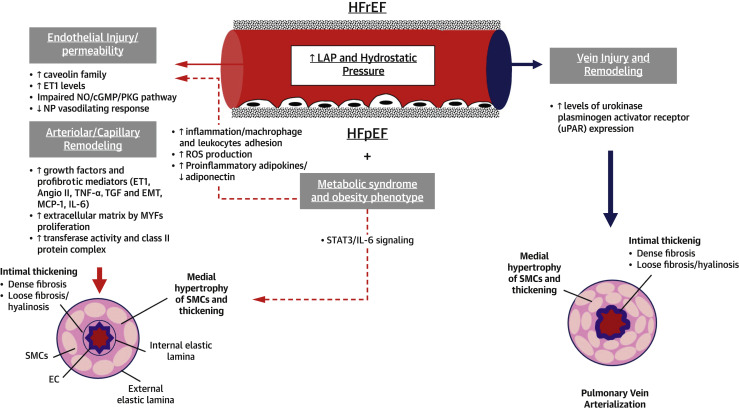
HFpEF 和 HFrEF 的静脉都经历了显着的重塑过程,包括管腔变窄、新内膜增厚和中层肥厚。 即使在调整了动脉内侧和内膜增厚后,内膜增厚和 PASP 仍存在相关性,并且报告了气体扩散的损失。 在移除 LVAD 时进行连续肺活检的少数患者中,检测到高水平的尿激酶纤溶酶原激活剂受体表达,这是迄今为止在静脉重塑过程中确定的唯一途径。
毛细血管和小动脉
向后压力升高会导致肺毛细血管和小动脉应力衰竭,这是一种气压伤,会破坏内皮层并促进间质中的液体和蛋白质肿胀。流体触发一系列血管重塑的分子介质,其发病机制对新的靶向治疗干预很有吸引力。水肿激活炎症介质,抑制一氧化氮和利钠肽的活性,并增加内皮素 (ET)-1 的表达,导致成纤维细胞/肌成纤维细胞增殖、管腔闭塞和肺泡隔增厚。从肺泡-毛细血管应力衰竭到重塑的转变至关重要,在临床实践中,肺泡膜气体扩散减少和 B 型表面活性蛋白水平高反映了这一转变。
PH-HFrEF 血管重塑的遗传分析表明,与细胞骨架结构和免疫功能相关的基因富集,涉及生物学上合理的途径,包括肌动蛋白结合、细胞外基质、基底膜、转移酶活性、前核糖体结构和主要组织相容性 II 类蛋白质复合物。
血流动力学表型分析和靶向治疗 PH 的新途径
PH-LHD没有既定的治疗方法,指南警告不要使用肺血管扩张剂。然而,考虑到 HF 患者 PH 的负担,寻找新的靶向疗法的难度很大,药理学试验正在进行中。在这种情况下使用 PAH 疗法的早期经验令人失望,因为它们的目的是降低肺压,而不是针对生物血管特性。 许多人提倡通过机器学习进行血流动力学表型分析,将其作为识别可能受益于治疗的患者子集的最可能方法。
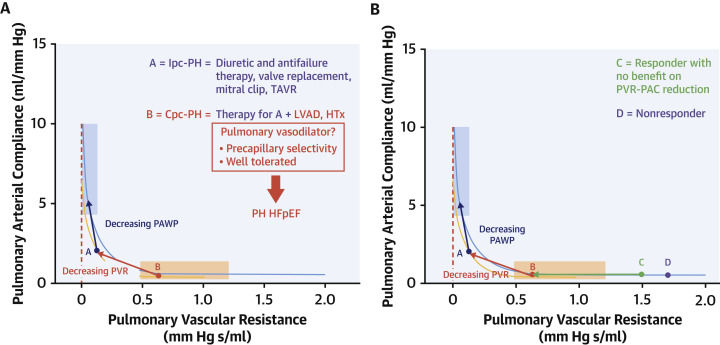
研究结论:
尽管它们的血流动力学分类相似,但人们越来越认识到 PH-HFrEF 和 PH-HFpEF 之间不断变化的差异。 PH-HFrEF 的左血流动力学驱动因素是 LV 扩张、继发性二尖瓣关闭不全和左心房扩大。PH-HFpEF 的主要机制是舒张期僵硬、心房肌病更容易演变为房颤和左心房功能性二尖瓣关闭不全。 血管应力衰竭和重塑类似地影响静脉、毛细血管和小动脉,但一个主要的区别特征是代谢损伤叠加在压力诱导的代谢损伤上,典型的 HFpEF 与代谢综合征。 在 PH-HFrEF 中经常观察到固有的 RV 病理,使 RV 与 Pc 解偶联更早发生。
参考文献:
Guazzi M, Ghio S, Adir Y. Pulmonary Hypertension in HFpEF and HFrEF: JACC Review Topic of the Week. J Am Coll Cardiol. 2020 Sep 1;76(9):1102-1111. doi: 10.1016/j.jacc.2020.06.069. PMID: 32854845.


