祸不单行!肝癌患者全血细胞减少,竟合并了最凶险的……
时间:2021-12-17 19:01:33 热度:37.1℃ 作者:网络
【前言】
原发性肝癌是指发生于肝细胞或肝内胆管细胞的癌肿,其中肝细胞癌(HCC)占原发性肝癌中的绝大多数,胆管细胞癌不足5%。本病恶性程度高,浸润和转移性强,远期疗效取决于能否早期诊断及早期治疗。我国是肝癌高发国家,肝癌病例约占全球的55%。
全血细胞减少在恶性肿瘤患者中相当常见,肝细胞癌也不例外;除了肿瘤本身的致病性,还与放化疗相关。然而,我们最近遇到一例患者肝癌复发、全血细胞减少,竟是合并了急性白血病,让我们和临床都大为惊讶。下面就来看看这个案例。
【案例经过】
患者男性,68岁,诊断为肝恶性肿瘤
血常规及散点图:

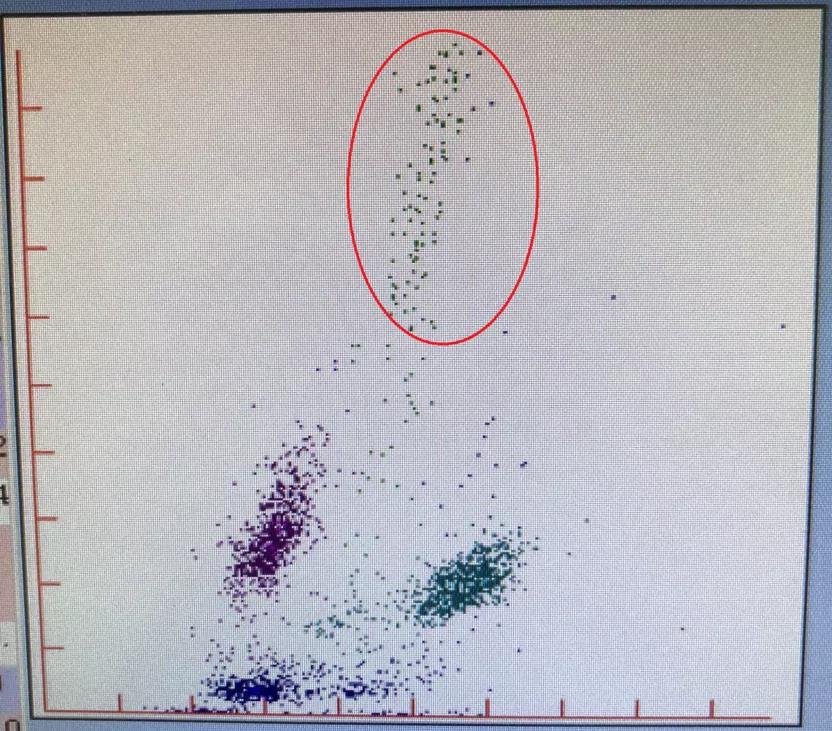
尽管患者诊断明确,白细胞又极低,但白细胞四分群散点图中还是能见到一些位于原始细胞区域的异常散点(以红色圈出),我们不敢大意,推片染色后在镜下寻找有无可疑细胞。由于细胞数极少,浏览全片后找到如下细胞:
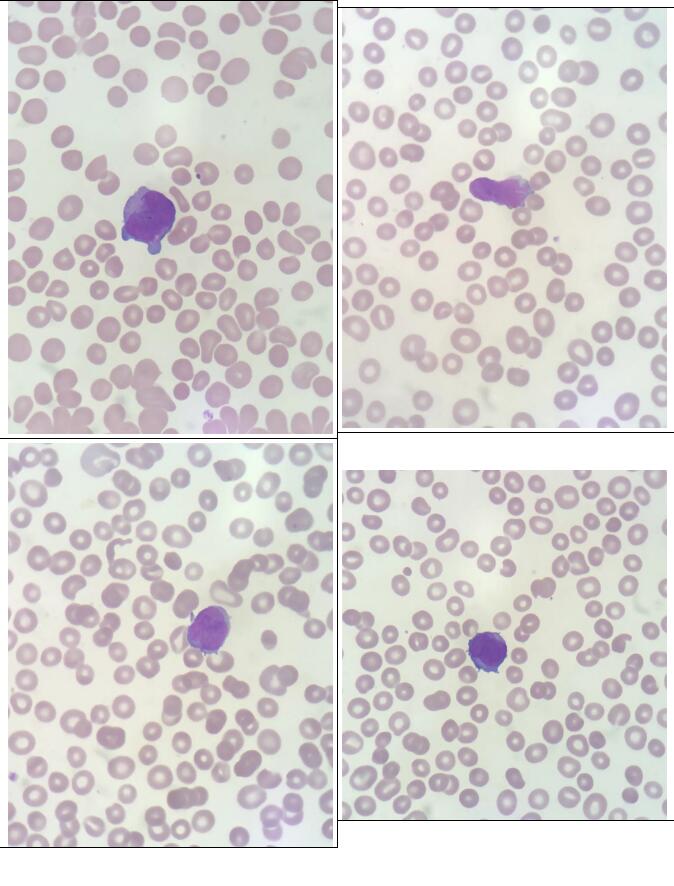
这四个毫无疑问是原幼细胞,胞体中等大小,多不规则,可见指状/瘤状凸起;胞核也不规则,折叠、扭曲、分叶,染色质细致;胞质量中等,蓝色。
虽然乍看上去像原幼单核细胞,但结合血常规全血细胞减少,笔者心里咯噔了一下:不会是急性早幼粒细胞白血病(APL)吧?!立即与临床医师取得了联系,得知了以下情况:
患者2017年诊断为原发性肝癌并进行了手术,后定期复查病情稳定,有“肝功能不全,脾功能亢进、乙型肝炎”病史,3天前出现全身乏力,余无明显异常。
查体:T 36.5℃,P82次/分,R16次/分,BP147/75mmHg,肝区叩击痛阳性。右上腹MRI:肝S4段及S8段异常信号灶;胸部CT:左肺上叶阴影。临床医师目前考虑的是肝癌复发和肺转移,因白细胞极度减少,刚使用了升白药。
在听到使用升白药之前,笔者还有些犹豫要不要报告,因为还从没听说过肝癌合并急性早幼粒细胞白血病的情况,但在听到使用升白药后,笔者顾不了那么多了:急性髓系白血病患者使用升白药是相当危险的;如果是急性早幼粒细胞白血病,使用升白药是致命的!
立即告诉临床医师,看到一些异常细胞,急性早幼粒细胞白血病不能除外,应立即进行干预,并完善骨髓细胞形态学、免疫分型、染色体及分子生物学检查以明确诊断。临床医师听说以后,吃惊的同时也十分重视,患者很快就用上了维甲酸(ATRA),骨髓涂片也很快送来了:
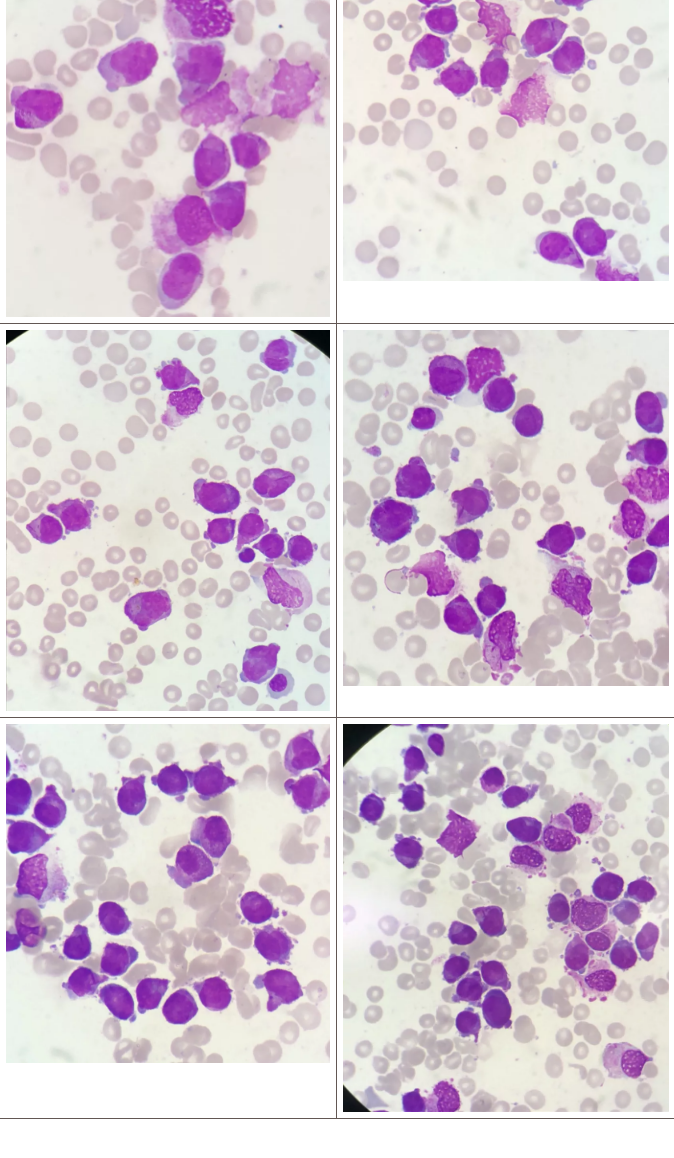
异常细胞多伪足,胞质中含细小、密集的紫红色颗粒,棒状小体多见,部分为柴捆状,胞核扭曲、折叠、分叶,核染色质细致,为典型的异常早幼粒细胞形态。
骨髓报告:
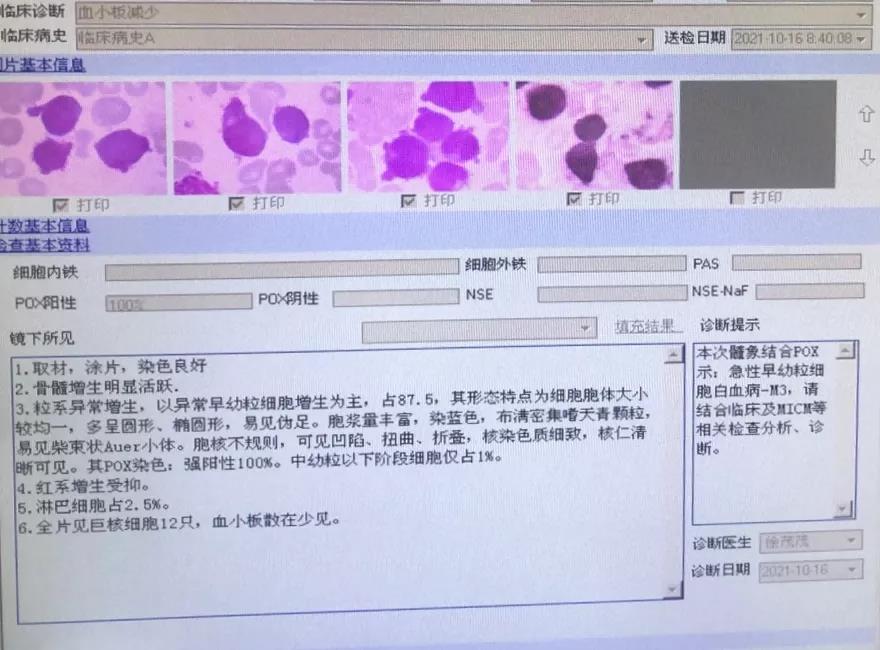
骨髓活检:
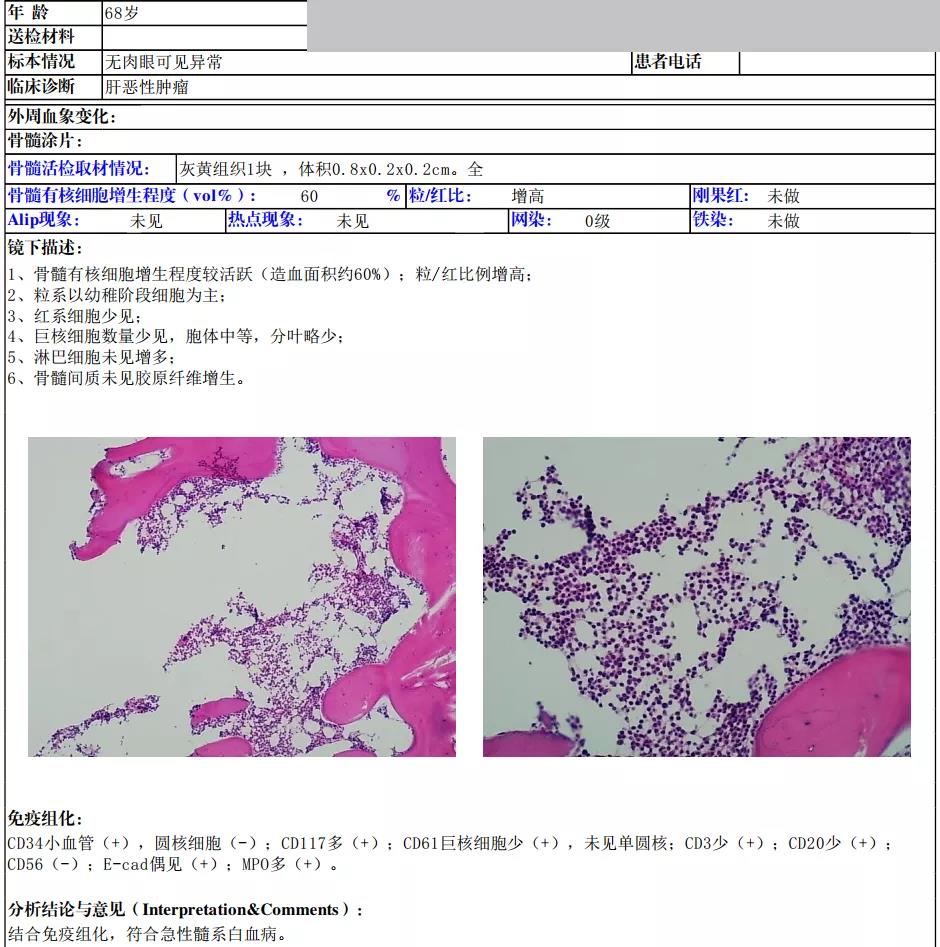
急性髓系白血病
免疫分型:
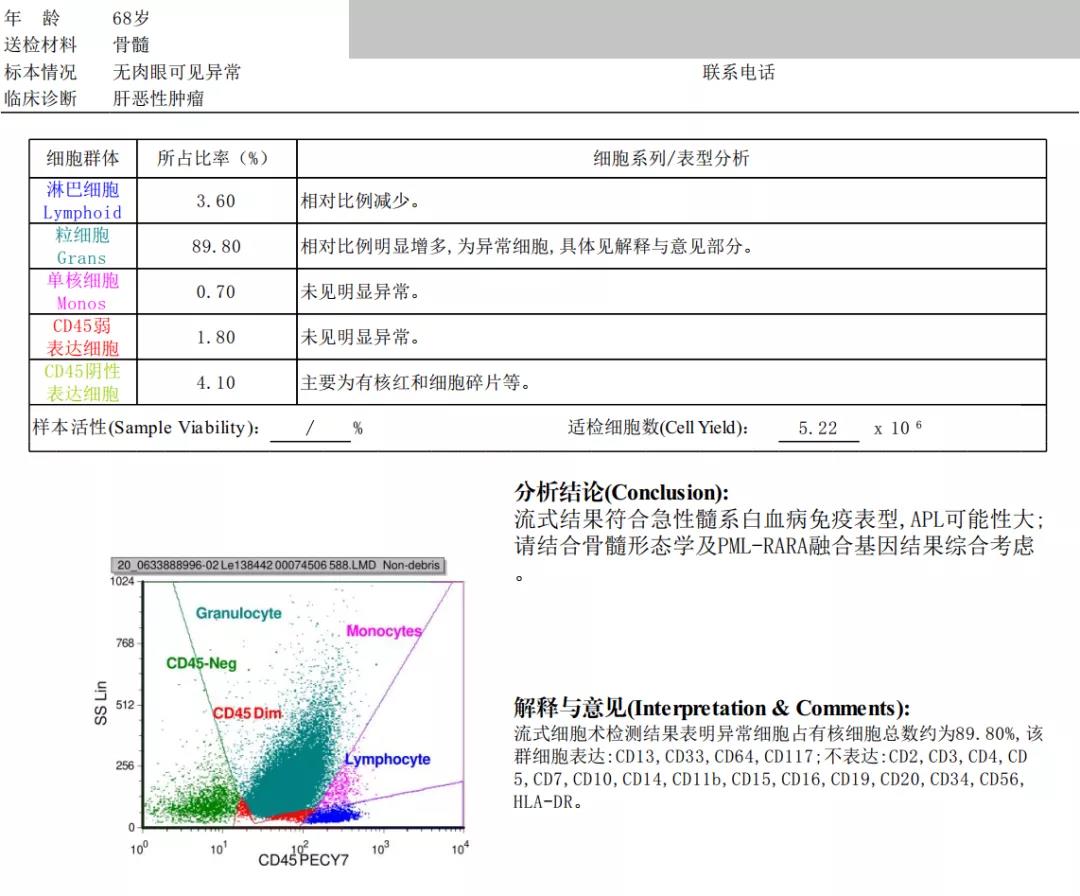
急性髓系白血病,急性早幼粒细胞白血病(APL)可能性大。
分子生物学检测:
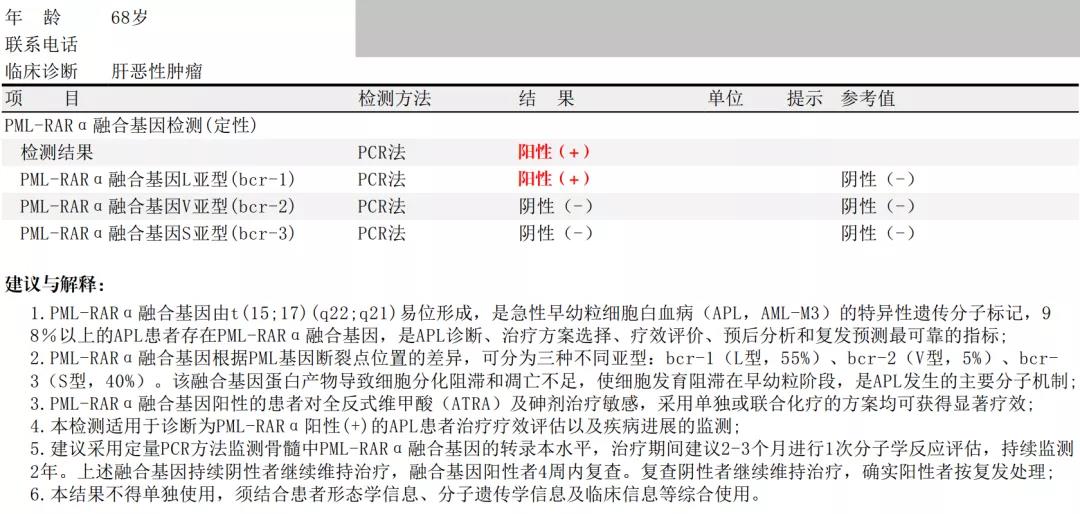
PML-RARA融合基因L亚型为阳性。
患者同时还送检了腹腔积液,确实发现了恶性肿瘤细胞:
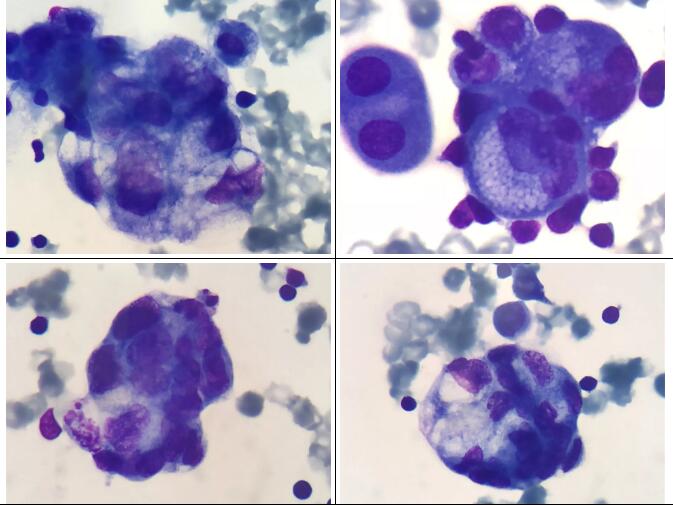
临床最终给该患者的诊断为:肝细胞癌复发+急性早幼粒细胞白血病。目前患者仍在接受治疗。
【案例分析】
一、诊断
2016版WHO造血与淋巴组织肿瘤分类明确指出,急性髓系白血病患者若具有:
t(8;21)(q22;q22.1); RUNX1-RUNX1T1
inv(16)(p13.1;q22)或t(16;16)(p13;q22); CBFB-MYH11
PML-RARA
这三种重现性遗传学异常可直接确立诊断,无需考虑原始细胞比例。
本例检出了PML-RARA融合基因,故急性早幼粒细胞白血病(APL)的诊断明确。
我们还查阅了国内文献,没有查到肝细胞癌合并急性早幼粒细胞白血病的案例报道。
二、分型
《中国急性早幼粒细胞白血病诊疗指南(2018年版)》根据颗粒的大小和数量将APL分为:①M3a(粗颗粒型);②M3b(细颗粒型);③M3c(微颗粒型)。
本例的患者缺少颗粒粗大的异常早幼粒细胞,大部分只是含有细小、密集的紫红色颗粒,应该属于M3b。
三、治疗相关的髓系肿瘤
治疗相关的髓系肿瘤(t-MN)包括:
1、治疗相关的急性髓系白血病(t-AML)
2、治疗相关的骨髓增生异常综合征(t-MDS)
3、治疗相关的骨髓增生异常/骨髓增殖性肿瘤(t-MDS/MPN)
与t-MN有关的细胞毒性因素:

从临床角度来说,t-MN分为两类:
1、最常见的类型是接受烷化剂和/或电离辐射后5~10年。患者常表现为t-MDS和一系乃至多系血细胞减少的骨髓衰竭的证据,多伴有遗传物质的非平衡丢失,往往涉及5号和/或7号染色体。
2、第二类包含20%~30%的患者,潜伏期要短(1~5年),发生于DNA拓扑异构酶Ⅱ抑制剂治疗之后。患者一般没有骨髓增生异常期,起病时就是急性白血病,并伴有平衡染色体易位。
不过,现实中有很多病人接受了包括以上所有细胞毒因素的多种治疗方案,因此这两类情况的界限并不清楚。
具体到这位患者,由于他和他的家属都没能提供明确、详细的治疗、用药史,故本例无法确定是否为t-APL。
【心得体会】
如今,一个患者同时罹患两种甚至更多种癌症的报道越来越多,文献没报道过的组合在微信群里也时有出现。所以,笔者认为要对同时罹患多种癌症保持开放的态度,不应抱着一元论不放。
根据浙江省人民医院吴茅教授团队的研究,浆膜腔积液肿瘤的四大检查技术中,常规细胞形态学检查的总阳性率是最高的(55%),优于CT(37.8%)、B超(6.6%)和病理液基细胞学(20%),这可能颠覆了很多人的认知。所以我们应当重视浆膜腔积液常规细胞形态学检查。
浆膜腔积液中肿瘤细胞的特点,可参考周道银教授的总结:

还可以加上“三深”:即胞质、胞核与核仁深染。
急性早幼粒细胞白血病(APL)易发生严重的出凝血紊乱(包括弥散血管内凝血,DIC),早期十分凶险,但若能及时发现并给予特效药(维甲酸和砷剂,ATRA+ATO),绝大多数患者无需造血干细胞移植就能治愈。
异常早幼粒细胞是形态学工作者的必修课,其最主要的特点是内外浆、不规则核形和柴捆样棒状小体,大家都很熟悉。真正的难点在于能否找到异常早幼粒细胞,尤其是初诊时多为低白的M3a和M3b。
典型APL的血常规多为三系减少,机器分类单核细胞增高,这可与AA鉴别,AA也是三系减少,但机器分类以淋巴细胞增高为主。此外MDS与MA也表现为三系减少,但二者往往为大细胞性贫血,可见MCV增高,MDS可见病态造血,MA可见中性粒细胞分叶过多,RBC可见大卵圆形红细胞。
总之,起病急且全血细胞减少的出血患者,必须考虑到本病的可能,此时要多与临床沟通。
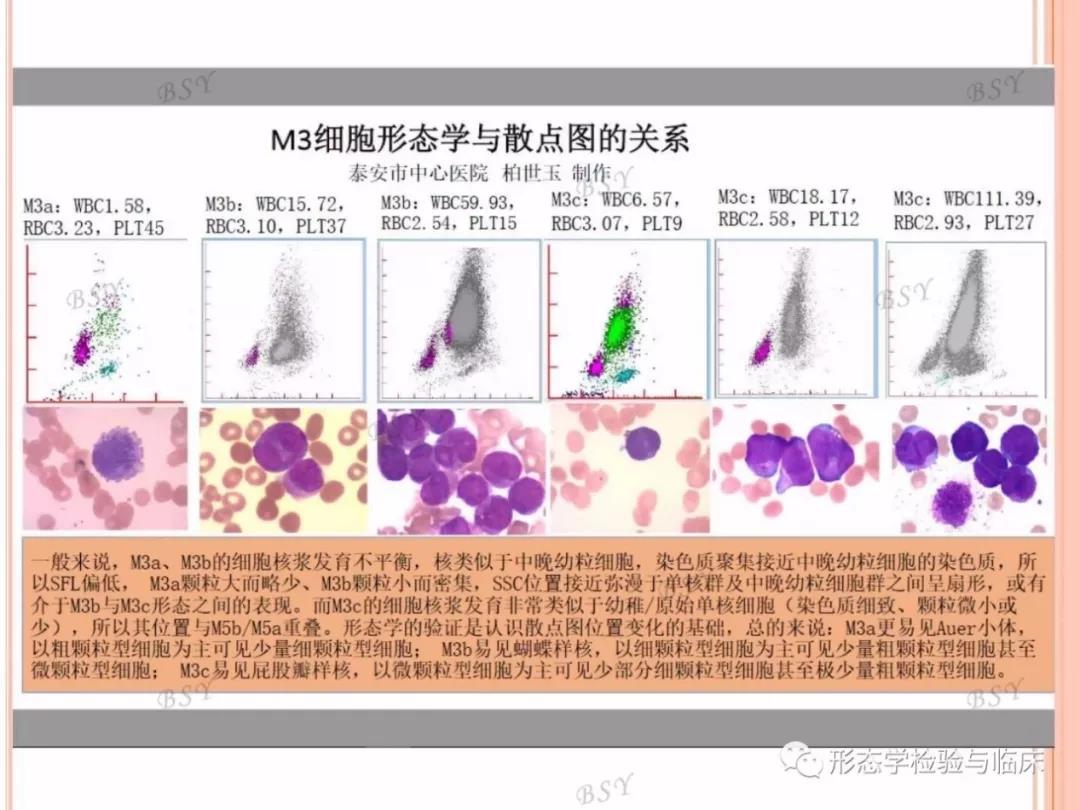
我们抓到这例APL,白细胞散点图发挥了重要的作用;大家可参考上图中柏世玉教授的总结。低白APL的散点图往往可见粒单融合,低值白细胞检测模式能分析更多粒子,有助于散点图表现得更典型。如果WBC数较低,血涂片可推稍厚一些,并在低倍镜下浏览全片(而非仅作分类),尤其要注意边缘及尾部(海岸线),异常细胞由于胞体偏大,往往会推于片尾,可先在低倍镜下找到可疑细胞,再转油镜确认,最好能找到柴捆细胞,更具说服力。Buffycoat涂片法和自然沉降法也有助于寻找异常早幼粒细胞(详见参考资料7)。
疑似APL的病人也可结合凝血功能检查,是否存在纤维蛋白原降低,纤维蛋白降解产物(FDP)和/或D-二聚体(D-D)升高。
急性早幼粒细胞白血病(APL)是血液科常见的急危重症,也是急性白血病诊断的重中之重。外周血细胞形态学检查对APL的诊断至关重要,必须引起重视;不少专家认为,异常早幼粒细胞应作为形态学危急值报告。希望我们的总结对大家日常捕捉APL有帮助!


