抗肿瘤治疗中肝炎病毒再激活的预防和治疗策略
时间:2024-11-07 16:00:13 热度:37.1℃ 作者:网络
乙型肝炎病毒(HBV)再激活是导致慢性乙型肝炎患者病情恶化的重要因素之一。近年来,在肿瘤领域,由于化疗药物、靶向药物、免疫检查点抑制剂等的广泛应用,抗肿瘤药物所致HBV再激活受到越来越多的关注。
近期,上海交通大学医学院附属瑞金医院谢青教授分享了抗肿瘤治疗中病毒性肝炎再激活的管理。肝癌在线特将精华整理成文,以飨读者。
一 肝炎病毒感染与肿瘤的关系
1、HBsAg阳性与肿瘤发生风险增加相关
中国一项慢性病前瞻性研究[1]于2004年6月至2008年7月期间,纳入中国10个地区的年龄为30至79岁的512891名参与者。经多变量调整后的分析表明,HBsAg血清阳性与总体肿瘤及肝细胞癌、胃癌、结直肠癌、口腔癌、胰腺癌和淋巴瘤的发生风险增加相关。
2、肿瘤合并HBV感染率远高于普通人
Polaris国际流行病学合作组织推算2016年我国一般人群中HBsAg阳性率为6.1%[2],乳腺癌患者中HBsAg阳性率为8.3%,胃癌中为17.2%,非小细胞肺癌中为15.3%,非霍奇金淋巴瘤患者中HBsAg阳性率最高,可达23.5%。
因此,在对各种实体肿瘤或血液系统肿瘤治疗过程中,HBV再激活的临床问题应引起高度重视。
二 抗肿瘤治疗中的肝炎病毒再激活
1、HBV再激活的定义
HBV再激活的定义,不同指南略有差异,但是基本都是通过HBV DNA升高≥2 logIU/ml以及HBsAg由阴性转为阳性界定判断。
1)慢性乙型肝炎防治指南(2022版)[3]:HBsAg阳性/抗-HBc阳性,或HBsAg阴性/抗-HBc阳性患者接受免疫抑制治疗或化学治疗时,HBV DNA较基线升高≥2logIU/ml,或基线HBV DNA阴性者转为阳性,或HBsAg由阴性转为阳性。
2)淋巴瘤免疫化疗HBV再激活预防和治疗中国专家共识(2013版)[4]:
如果出现以下情况之一,即可定义为HBV再激活:
①在免疫化疗或免疫抑制剂治疗期间或之后,血清HBV DNA 由不可测转为可测;
②HBV DNA载量比基线水平升高10倍以上,如从103拷贝/ml升至104拷贝/ml;
③以ALT升高为主要表现的肝脏炎症损伤加重,例如ALT由正常变为异常,并可排除原发病、药物性肝损伤等其他原因导致的肝功能损害。
3)APASL clinical practice guideline(2021版)[5]:
①慢性HBV感染恶化(HBsAg阳性):HBV DNA水平较基线水平增加≥2log;在基线时无法检测到HBV DNA的人中检测到>100IU/ml水平的HBV DNA。
②在免疫抑制治疗开始后,既往HBV感染再激活(HBsAg阴性/抗-HBc阳性):HBsAg血清转化,HBsAg阴性转为阳性;HBsAg阴性时HBV DNA阴性转为HBV DNA阳性。
4)ASCO Provislonal Clinical Opinion Update(2020版)[6]:
①慢性HBV感染:HBV DNA较基线增加≥2log(10倍),或以前未检测到HBV DNA者,HBV DNA≥3log(1000)IU/mL;
②既往HBV感染:可检测到HBV DNA;HBsAg阴性转为阳性。
5)Australian consensus statement(2019版)[7]:在HBsAg阳性患者中HBV DNA水平较基线水平增加10倍,及在HBsAg阴性和抗-HBc阳性个体中HBsAg转阳。
2、HBV再激活的表现和机制
HBV再激活可表现为短暂性、无症状肝炎,但常常导致肝炎暴发,甚至可进展为急性肝衰竭。化疗后HBV再激活的典型病程:第一阶段,患者血清HBV DNA较基线显著上升。如果没有很好的处理,则进入第二阶段,肝细胞损伤及炎症坏死,伴随ALT水平升高和临床症状出现,肝功能损伤范围从轻度肝炎到肝衰竭。在第三阶段,通过抗病毒治疗或停止免疫抑制剂治疗,肝脏炎症反应自发停止。
宿主的免疫应答在对抗HBV感染中发挥着重要作用。HBV感染的患者,宿主细胞免疫和体液免疫共同抑制肝内HBV共价闭合环状DNA(cccDNA)。但当免疫抑制药物使用后,可耗尽B细胞产生的抗体,或损害机体固有免疫,从而导致宿主免疫系统控制HBV复制的能力被破坏。作为HBV复制模版的肝细胞核内HBV cccDNA重新开始转录,产生病毒颗粒并释放入血,继而发生HBV再激活[8]。
3、HBV再激活的风险评估
HBV再激活风险评估主要取决于HBV标志物状态及抗肿瘤治疗药物的类型。
不同HBV感染状态的再激活风险存在差异。在化疗过程中,HBsAg(-)的患者再激活风险低,约为1.0%-2.7%,HBsAg(+)患者再激活风险则较高,可达24%-53%。利妥昔单抗联合化疗方案是临床上常用的淋巴瘤治疗方案,其中利妥昔单抗易导致HBV再激活,即使在HBsAg(-)/抗-HBc(+)的患者中,再激活风险也可达到12.2%-23.8%。造血干细胞移植或器官移植也是HBV再激活的高风险人群,因为患者需要使用大量的免疫抑制剂。在HBsAg(-)患者中,再激活风险为14-20%,HBsAg(+)患者则>50%。
不同抗肿瘤药物及HBV标志物状态所致HBV再激活风险总结如表1。
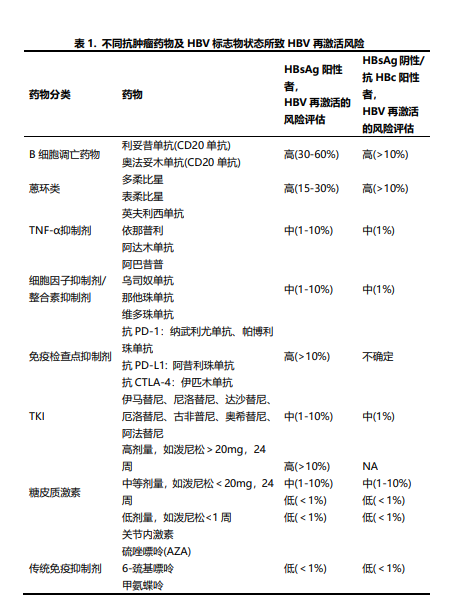
三 肝炎病毒再激活预防和治疗策略
1、预防HBV再激活的管理流程
目前国内外指南推荐意见基本一致,所有接受化疗、免疫抑制剂治疗的患者都应该在抗肿瘤治疗起始前筛查HBV。对于HBsAg阳性患者,开始化学治疗、靶向药物及免疫抑制剂前至少1周(特殊情况可同时)进行抗病毒治疗,应用ETV、TDF或TAF,持续至化疗或免疫抑制治疗结束后6-12个月。对于HBsAg阴性/抗-HBc阳性患者,若HBV DNA阳性、使用B细胞单克隆抗体或造血干细胞移植,或伴进展期肝纤维化/肝硬化,建议应用ETV、TDF或TAF抗病毒治疗。
2019年澳大利亚共识对抗病毒人群及时机给出的意见则更为具体。
1)建议抗病毒预防应在癌症治疗开始前尽快开始,但不应延迟癌症治疗。抗病毒预防应至少在启动化疗前1周或启动化疗时进行。
2)所有HBsAg阳性的血液学或恶性实体肿瘤患者应进行抗病毒预防。
3)对于HBsAg阴性和抗-HBc阳性的患者,其HBV再激活风险由肿瘤治疗方案决定(高风险或低风险)。
①接受高风险肿瘤治疗患者(造血干细胞移植;B淋巴细胞消耗、B淋巴细胞激活剂或抗CD20药物;急性白血病和高等级淋巴瘤治疗)应接受抗病毒预防。
②接受低风险肿瘤治疗患者不需要抗病毒预防。
2、抗病毒治疗可带来的获益
在许多前瞻性和回顾性研究中证实,强效核苷(酸)类似物可有效预防HBV再激活(图1)。
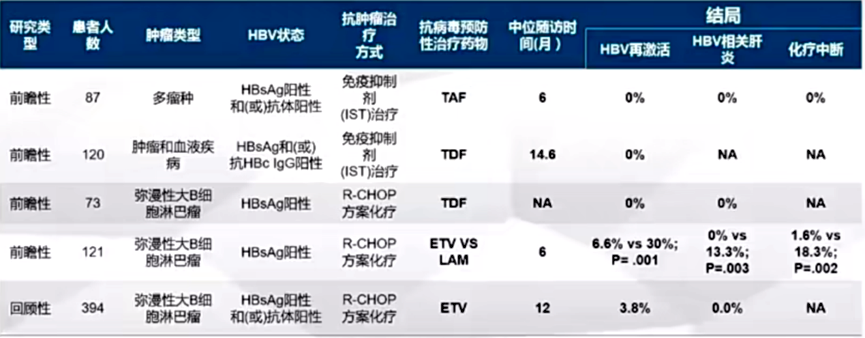
图1. 抗病毒治疗可有效预防HBV再激活
3、抗病毒药物的选择
建议使用强效、高耐药屏障的核苷或核苷酸类似物药物(如恩替卡韦或替诺福韦)进行抗病毒预防。TAF、TMF作为一线NA药物目前也已在这些人群中使用。
《慢性乙型肝炎防治指南(2022年版)》中推荐HBeAg阳性CHB患者首选NAs(ETV、TDF、TAF或TMF)治疗(A1),大多数患者需要长期用药。如因各种原因希望停药,治疗1年HBV DNA低于检测下限、ALT复常和HBeAg血清学转换,再巩固治疗至少3年(每隔6个月复查1次)仍保持不变,且HBsAg<200IU/mL,可尝试停药,但应严密监测,延长疗程可减少复发(B1)。HBeAg阴性CHB患者首选NAs(ETV、TDF、TAF或TMF)治疗(A1)。建议HBsAg消失和/或出现抗HBs,且HBV DNA检测不到,巩固治疗6个月仍检测不到者,可停药随访(B1)。
4、关于停药和继续治疗及监测的问题
1)对于慢性HBV携带状态或HBsAg阴性、抗-HBc阳性且采用NAs预防治疗者,在化学治疗、靶向药物及免疫抑制剂治疗结束后,应继续抗病毒治疗6-12个月。
2)以下人群应在免疫抑制治疗结束后6个月考虑终止NAs:
①HBsAg阳性,没有晚期肝纤维化或肝硬化的患者;
②使用NAs前HBV DNA水平较低(<2000IU/ml)的HBsAg阳性患者;
③HBsAg阴性/抗-HBc阳性患者。
3)在使用B淋巴细胞消耗、B淋巴细胞激活剂或抗CD20药物或造血干细胞移植后,建议患者继续进行抗病毒治疗18-24个月。
4)NAs停用后有可能会出现HBV复制反弹,甚至病情恶化,应随访12个月,期间每1-3个月监测HBV DNA及肝脏生物化学指标。
5、《慢性乙型肝炎防治指南(2022年版)》中的推荐管理流程
《慢性乙型肝炎防治指南(2022年版)》中推荐所有接受化学治疗、靶向药物及免疫抑制剂治疗的患者,开始治疗前均应常规筛查HBsAg、抗HBc和/或HBV DNA。对于HBsAg和/或HBV DNA阳性者,在开始化学治疗、靶向药物及免疫抑制剂治疗前至少1周、特殊情况可同时应用ETV、TDF或TAF抗病毒治疗。对于HBsAg阴性、抗HBc阳性患者,若使用B淋巴细胞单克隆抗体或进行造血干细胞移植,或伴进展期肝纤维化/肝硬化,建议应用ETV、TDF或TAF抗病毒治疗。
四 丙型肝炎病毒再激活的管理
静止的丙肝病毒感染定义为HCV感染,血清HCV RNA阳性,血清肝酶水平正常。丙肝病毒再激活定义为化疗期间HCV RNA水平较基线水平增加≥1log10IU/ml。丙肝肝炎暴发为化疗期间ALT升高至正常上限的3倍,HCV RNA水平较基线升高≥1log10IU/ml。
接受化疗的所有肿瘤患者均须筛查HCV感染,筛查方法为在肿瘤治疗前检测抗-HCV抗体。抗-HCV抗体阳性患者需进一步检测HCV RNA,如检测为HCV RNA阳性,则需要对接受化疗且无DAA治疗禁忌证的HCV感染癌症患者进行DAA治疗,DAA治疗可在化疗前、化疗中或化疗后进行。如果需要同时使用化疗和抗病毒药物,可考虑选择药物-药物相互作用较少的DAA,并密切监测肝功能。
五 总结
HBV感染和肿瘤的发生与发展存在一定的因果关系,可能是肿瘤发生、发展的促进因素或致病因素。肿瘤合并HBV感染率远高于普通人群,特别是在淋巴瘤患者中。合并HBV感染(包括已临床治愈)的患者,化疗、免疫抑制剂治疗及靶向治疗等抗肿瘤治疗均会导致HBV再激活。HBV再激活严重影响患者的治疗、生活质量和长期生存,甚至会引起肝衰竭而导致死亡。对于肿瘤合并HBV感染患者进行预防性抗病毒治疗,国内外目前已达成共识,强效低耐药的一线NAs抗病毒治疗可降低HBV再激活风险,改善预后。
参考文献
[1] Song C, Lv J, Liu Y, et al. Associations Between Hepatitis B Virus Infection and Risk of All Cancer Types[J]. JAMA Netw Open, 2019, 2(6): e195718.
[2] Global prevalence, treatment, and prevention of hepatitis B virus infection in 2016: a modelling study[J]. Lancet Gastroenterol Hepatol, 2018, 3(6): 383-403.
[3] 中华医学会肝病学分会. 慢性乙型肝炎防治指南(2022年版)[J]. 中华传染病杂志,2023,41(1):3-28.
[4] .中国临床肿瘤学会 中华医学会血液学分会 中国医师协会肿瘤医师考核委员会. 淋巴瘤免疫化疗HBV再激活预防和治疗中国专家共识[J]. 临床肿瘤学杂志,2013,18(10):935-942.
[5] Lau G, Yu M L, Wong G, et al. APASL clinical practice guideline on hepatitis B reactivation related to the use of immunosuppressive therapy[J]. Hepatol Int, 2021, 15(5): 1031-1048.
[6] Hwang J P, Feld J J, Hammond S P, et al. Hepatitis B Virus Screening and Management for Patients With Cancer Prior to Therapy: ASCO Provisional Clinical Opinion Update[J]. J Clin Oncol, 2020, 38(31): 3698-3715.
[7] Doyle J, Raggatt M, Slavin M, et al. Hepatitis B management during immunosuppression for haematological and solid organ malignancies: an Australian consensus statement[J]. Med J Aust, 2019, 210(10): 462-468.
[8] Wursthorn K, Wedemeyer H, Manns M P. Managing HBV in patients with impaired immunity[J]. Gut, 2010, 59(10): 1430-1445.


